Clear Sky Science · he
שימוש בתכונות 침וש תלת־ממדיות של שורות תאי RCC בתרבית כדי לחזות את פוטנציאל התפשטותן במודל חי
מדוע המחקר הזה חשוב
כאשר סרטן הכליה מתפשט לאיברים אחרים, הטיפול בו נעשה הרבה יותר קשה. רופאים היו רוצים לדעת מוקדם אילו גידולים צפויים להישאר במקום ואילו נוטים לנוע ולהתפשט. במחקר זה מראים כי גידול תאי סרטן הכליה לתוך מיני־גידולים תלת־ממדיים במעבדה מאפשר לחזות עד כמה בגוף החי הסרטן יתפשט. העבודה מצביעה על מבחנים מעבדתיים שעשויים בעתיד לחסוך לחלק מהחולים טיפולים מיותרים ולסמן אחרים שזקוקים לטיפול מהיר ואינטנסיבי.
בניית מיני־גידולים איכותיים יותר
רוב מחקרי הסרטן עדיין מבוססים על שכבות תאים שטוחות שגודלו על צלחות פלסטיק. אלה נוחים לעבודה אך אינם מעתקים היטב את התנהגות הגידול בתוך הגוף, שם התאים חודרים דרך הרקמה הסובבת בתלת־ממד. במחקר זה עבדו המדענים עם שלוש שורות תאי סרטן כליה ידועות, שכבר ידעו שנושאות תכונות גנטיות ואיתות שונות. הם יצרו מכל סוג תאי צברים כדוריים קומפקטיים, והטמיעו צברים אלה בג'ל רך עשוי קולגן ופיברונקטין התואם לקשיחות רקמת הכליה האמיתית. במשך שבוע עקבו אחר המרחק ומהירות שבאמצעותן תאי הסרטן נפרדו מהספירואיד וחדרו לג'ל, ומיפו את מסלולי התנועה של תאים בודדים. 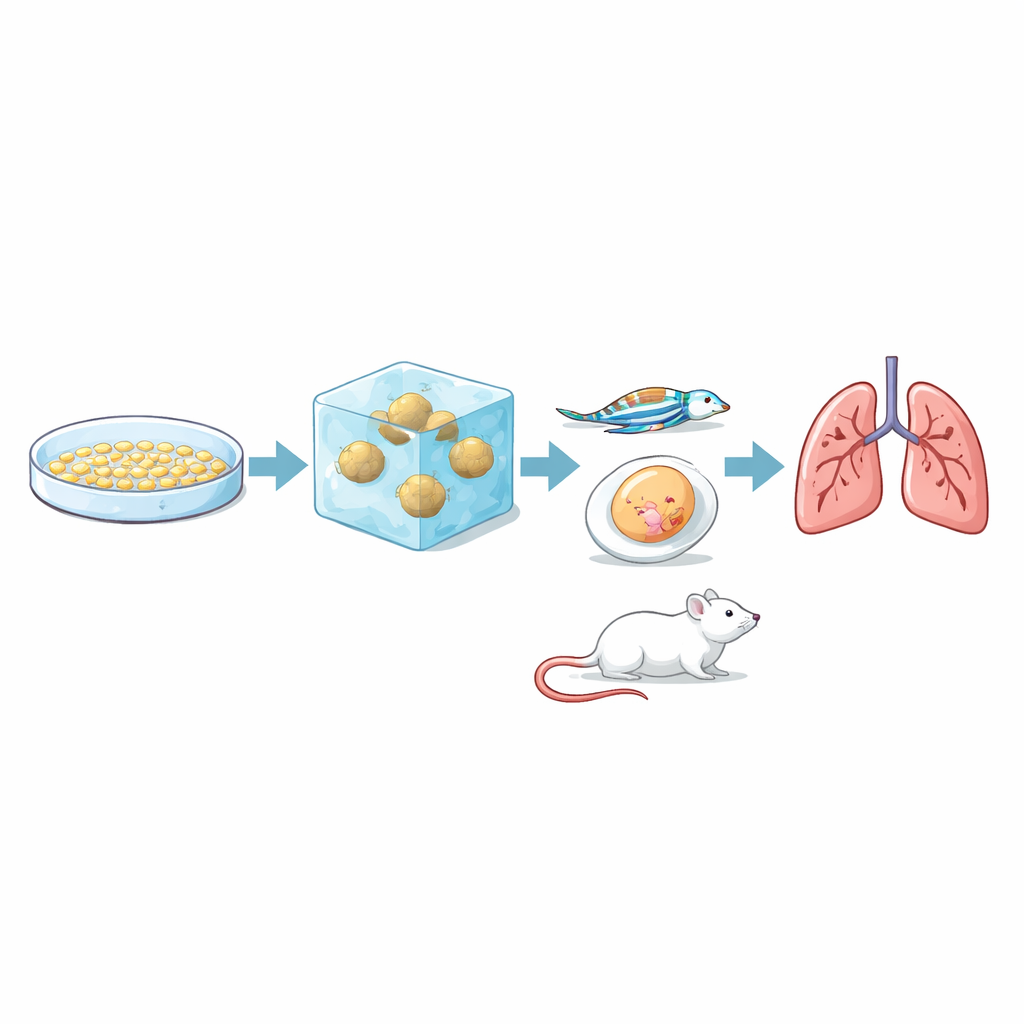
דירוג תאי הסרטן לפי הדחף שלהם לחדור
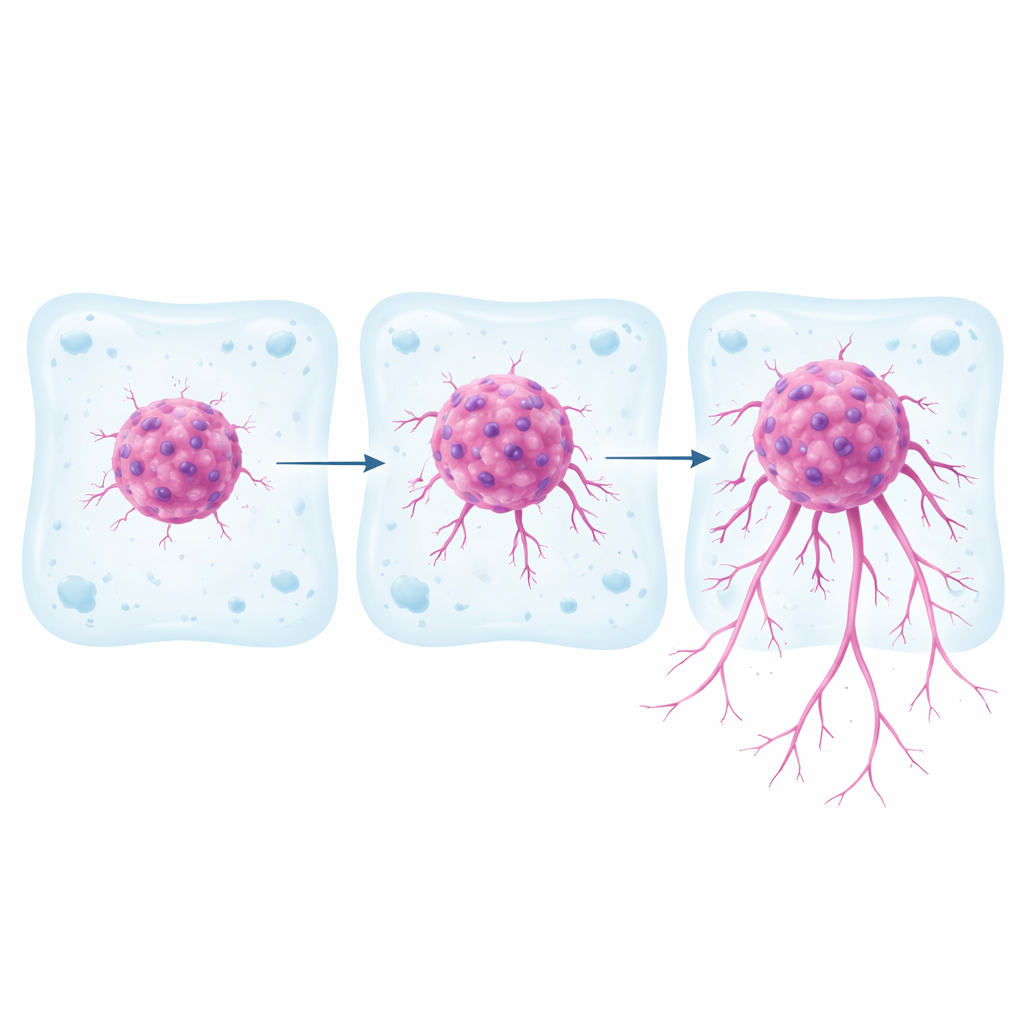
שלוש שורות התאים הראו התנהגויות שונות בולטות בהגדרה התלת־ממדית הזו. שורה אחת, הנקראת RCC10, נשארה בעיקר ככדור צפוף עם תנועה חיצונית מזערית בלבד. שורה שנייה, 786-O, שלחה תאים לתוך הג'ל, אך במידה מתונה. השורה השלישית, RCC7, הייתה הכי תוקפנית: תאים ממנה זרמו לעומק הג'ל, כיסו שטח גדול יותר ונעו במהירויות גבוהות יותר. הנתיבים שציירו תאי RCC7 ו־786-O היו מתפתלים וחוקרים, עם שינויים כיוון תכופים, בעוד שתאי RCC10 נטו לנוע באופן ישר יותר ומוגבל יותר. חסימת מסלול איתות מפתח (דרך TGFβ) בספירואידים הפלשוּתיים יותר הקטינה משמעותית את יכולתם להימלט לתוך הג'ל, ואישרה שהמודל מגיב לתרופות המכוונות למנגנוני חדירה.
בדיקת הניבויים בחיות חיות
השאלה המרכזית היתה האם מבחן החדירה במעבדה משקף בפועל את התנהגות הגידולים באורגניזמים ממשיים. כדי לבדוק זאת, הצוות הזריק את שלוש שורות התאים לאותה סדרת מודלים חייתיים המייצגים שלבים שונים של מטסטזיס. בממברנות ביצת תרנגולת שלוש השורות יצרו גידולים, אך RCC7 יצר מסות גדולות יותר, מלאות דם ומגוונות יותר. בעוברי דג זברה שקופים עקבו החוקרים אחרי תאים מסומנים בפלואורוסנציה שנעו בכלי הדם: תאי RCC7 ו־786-O נדבקו לדפנות הכלים וניצלו החוצה אל הרקמה הסובבת בתדירות גבוהה יותר מאשר תאי RCC10. בעכברים, תאי RCC7 ו־786-O יצרו באופן אמין גרורות בריאות, כאשר RCC7 עשה זאת מהר יותר ובהיקף גדול יותר, בעוד RCC10 לא יצר גרורות ריאתיות ניתנות לזיהוי במהלך תקופת המחקר. בסך הכל, הדירוג שנראה בג'ל התלת־ממדי — RCC7 הכי פלשוּתית, 786-O בינונית, RCC10 הכי פחות — תאם את ההתנהגות בחיות.
הרחבת הגישה לגידולי מטופלים
כדי להתקרב למציאות קלינית, החוקרים גם יצרו "טומורואידים" תלת־ממדיים מדגימות גידול טריות שנלקחו משני חולי כליה שלגביהם היו דרגות פתולוגיות סטנדרטיות שונות. שגדלו במערכת הג'לית זהה, טומורואידים מהגידול בעל הדרגה הגבוהה חדרו במהירות ושלחו הרבה ענפים חוקרים, בעוד אלה מהגידול בעל הדרגה הנמוכה נשארו קומפקטיים ואיטיים יותר. רוב התאים הפלשוּתיים נשאו סמן ידוע לסרטן הכליה, ואישרו שהם באו מהגידול ולא מהרקמה התקינה הסובבת. אמנם מדגם החולים קטן, אך התוצאות מרמזות כי התנהגות החדירה בתלת־ממד של טומורואידים של מטופל עשויה לשקף את חומרת המחלה שלו.
מה זה אומר עבור חולים
העבודה מראה שמבחן מעבדתי תלת־ממדי יחסית פשוט יכול לשקף איך תאי סרטן הכליה מתפשטים בחיות חיות. באמצעות מעקב אחר כמה רחוק ובאיזו דינמיקה תאים נמלטים ממיני־גידולים בג'ל ריאליסטי, מדענים יכולים להבחין בין סרטן עם פוטנציאל גרורתי נמוך, בינוני או גבוה. בעתיד, מבחני טומורואיד תלת־ממדיים כאלה, בצירוף דרוג מיקרוסקופי סטנדרטי ובדיקות גנטיות, עשויים לסייע לרופאים לחזות טוב יותר אילו גידולי כליה צפויים לעשות גרורות ולהתאים את הטיפול בהתאם. הם גם יכולים לספק פלטפורמה מהירה ואתית לבדיקת תרופות חדשות שמטרתן לעצור את התפשטות הסרטן לפני שהיא מתחילה.
ציטוט: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
מילות מפתח: סרטן הכליה, טומורואידים, גידול תאי תלת־ממדי, גרורות, קרצינומה של הכליה