Clear Sky Science · fr
Utiliser les propriétés d’invasion 3D de lignées cellulaires du carcinome rénal in vitro pour prédire leur potentiel métastatique in vivo
Pourquoi cette recherche est importante
Lorsque le cancer du rein se propage à d’autres organes, son traitement devient beaucoup plus difficile. Les médecins aimeraient savoir dès le départ quelles tumeurs sont susceptibles de rester localisées et lesquelles risquent de se disséminer. Cette étude montre qu’en cultivant des cellules de cancer du rein dans des mini‑tumeurs tridimensionnelles soigneusement conçues en laboratoire, les chercheurs peuvent prévoir à quel point ces cancers se propageront agressivement chez des animaux vivants. Ce travail ouvre la voie à des tests de laboratoire qui pourraient un jour éviter des traitements inutiles à certains patients tout en signalant ceux qui ont besoin de soins rapides et intensifs.
Construire de meilleurs mini‑tumeurs
La plupart des recherches sur le cancer reposent encore sur des couches cellulaires plates cultivées sur des boîtes en plastique. Faciles à manipuler, elles reproduisent mal le comportement des tumeurs dans l’organisme, où les cellules progressent en trois dimensions à travers les tissus environnants. Dans cette étude, les scientifiques ont travaillé avec trois lignées cellulaires bien connues du cancer du rein, dont ils savaient déjà qu’elles présentaient des caractéristiques génétiques et des voies de signalisation différentes. Ils ont formé chaque type cellulaire en amas sphériques compacts, puis ont encapsulé ces amas dans un gel mou composé de collagène et de fibronectine, dont la rigidité correspond à celle du tissu rénal réel. Sur une semaine, ils ont suivi jusqu’où et à quelle vitesse les cellules cancéreuses se détachaient du sphéroïde et envahissaient le gel environnant, et ont cartographié les trajectoires de cellules individuelles. 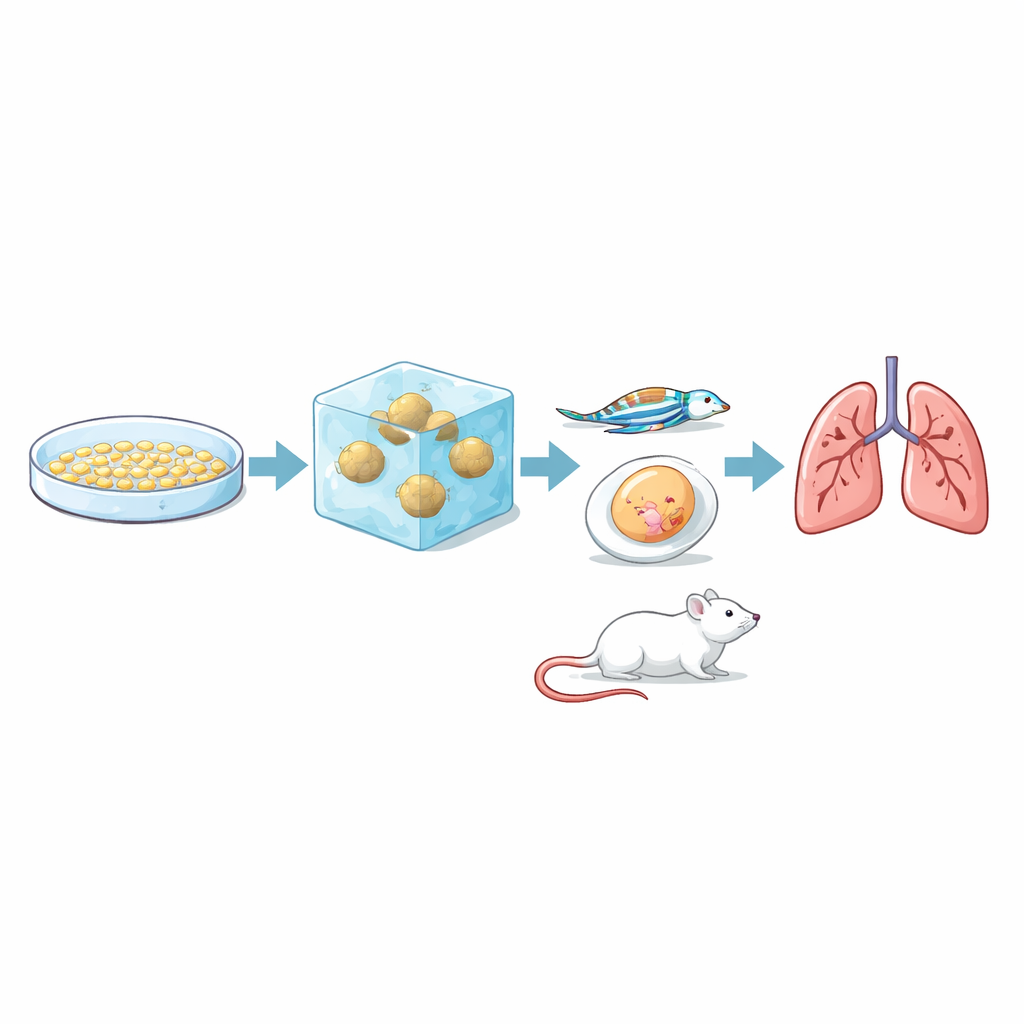
Classer les cellules cancéreuses selon leur propension à envahir
Les trois lignées cellulaires ont montré des comportements très différents dans ce contexte 3D. Une lignée, appelée RCC10, est restée principalement en boule compacte avec seulement un mouvement extérieur minimal. Une seconde, 786‑O, a envoyé des cellules dans le gel, mais dans une mesure modérée. La troisième, RCC7, était la plus agressive : ses cellules se sont infiltrées profondément dans le gel, ont couvert une plus grande surface et se sont déplacées à des vitesses plus élevées. Les trajectoires des cellules individuelles de RCC7 et 786‑O étaient sinueuses et exploratoires, avec des changements fréquents de direction, tandis que les cellules RCC10 avaient tendance à se mouvoir de façon plus rectiligne et limitée. Le blocage d’une voie de signalisation clé (la voie TGFβ) dans les sphéroïdes les plus invasifs a réduit de manière significative leur capacité à s’échapper dans le gel, confirmant que le modèle répond aux médicaments ciblant des mécanismes liés à l’invasion.
Tester les prédictions chez des animaux vivants
La question cruciale était de savoir si ce test d’invasion en laboratoire reflète réellement le comportement des tumeurs chez des organismes vivants. Pour le vérifier, l’équipe a injecté les mêmes trois lignées cellulaires dans plusieurs modèles animaux qui reproduisent différentes étapes de la métastase. Dans les membranes d’œuf de poule, les trois ont formé des tumeurs, mais RCC7 a produit des masses plus volumineuses, remplies de sang et plus hétérogènes. Chez des embryons de poisson zèbre transparents, les chercheurs ont observé des cellules cancéreuses marquées par fluorescence circuler dans les vaisseaux sanguins : les cellules RCC7 et 786‑O se sont accrochées aux parois vasculaires et sont sorties dans le tissu environnant plus souvent que les cellules RCC10. Chez la souris, les cellules RCC7 et 786‑O ont formé de façon fiable des métastases pulmonaires, RCC7 le faisant plus rapidement et de manière plus étendue, tandis que RCC10 n’a produit aucune métastase pulmonaire détectable pendant la durée de l’étude. Pris ensemble, le classement observé dans le gel 3D — RCC7 le plus invasif, 786‑O intermédiaire, RCC10 le moins invasif — correspondait à leur comportement chez les animaux. 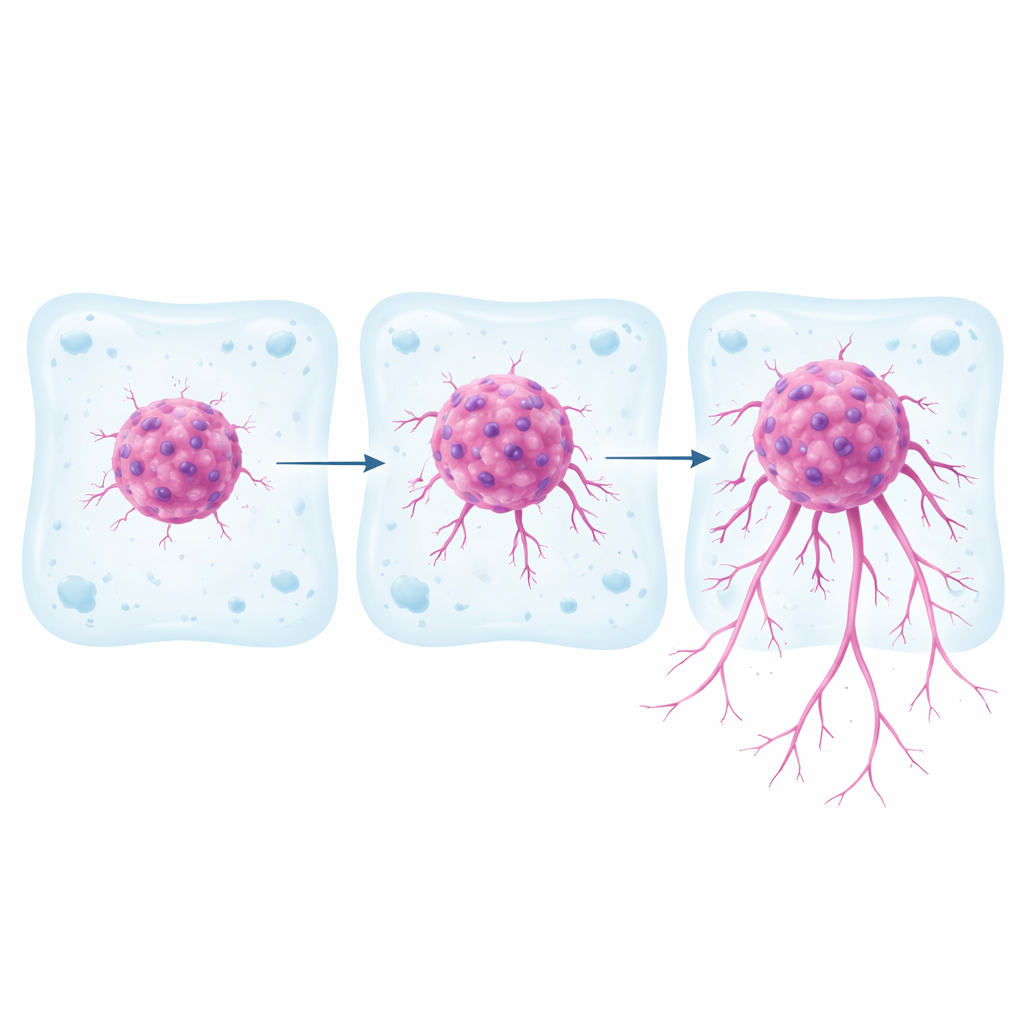
Étendre l’approche aux tumeurs de patients
Pour se rapprocher de la réalité clinique, les chercheurs ont également créé des tumoroïdes 3D à partir d’échantillons de tumeur frais prélevés chez deux patients atteints d’un cancer du rein présentant des grades anatomopathologiques différents. Cultivés dans le même système de gel, les tumoroïdes issus de la tumeur de grade élevé ont envahi rapidement et ont émis de nombreuses branches exploratoires, tandis que ceux issus de la tumeur de grade inférieur sont restés plus compacts et lents. La plupart des cellules envahissantes portaient un marqueur connu du cancer du rein, confirmant qu’elles provenaient de la tumeur et non des cellules normales avoisinantes. Bien que l’échantillon patient soit restreint, les résultats suggèrent que le comportement d’invasion 3D des tumoroïdes d’un patient pourrait refléter la gravité de sa maladie.
Qu’est‑ce que cela signifie pour les patients
Ce travail montre qu’un test de laboratoire 3D relativement simple peut refléter la façon dont les cellules du cancer du rein se propagent chez les animaux vivants. En observant à quelle distance et avec quelle dynamique les cellules s’échappent des mini‑tumeurs dans un gel réaliste, les scientifiques peuvent distinguer des cancers à potentiel métastatique faible, moyen ou élevé. À l’avenir, de tels essais de tumoroïdes 3D, combinés à la classification microscopique standard et aux tests génétiques, pourraient aider les médecins à mieux prédire quels cancers du rein sont susceptibles de métastaser et à adapter les traitements en conséquence. Ils pourraient aussi fournir une plateforme éthique et plus rapide pour tester de nouveaux médicaments visant à stopper la dissémination du cancer avant qu’elle ne commence.
Citation: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
Mots-clés: cancer du rein, tumoroïdes, culture cellulaire 3D, métastase, carcinome rénal