Clear Sky Science · it
Uso delle proprietà di invasione 3D di linee cellulari RCC in vitro per prevedere il loro potenziale metastatico in vivo
Perché questa ricerca è importante
Quando il cancro del rene si diffonde ad altri organi, diventa molto più difficile da trattare. I medici vorrebbero sapere tempestivamente quali tumori sono destinati a restare localizzati e quali invece sono propensi a metastatizzare. Questo studio mostra che facendo crescere cellule di carcinoma renale in mini-tumori tridimensionali ben progettati in laboratorio, i ricercatori possono prevedere quanto aggressivamente quei tumori si diffonderanno in organismi viventi. Il lavoro indica la strada verso test di laboratorio che un giorno potrebbero risparmiare ad alcuni pazienti trattamenti non necessari, segnalando al contempo chi necessita di cure rapide e intensive.
Costruire mini-tumori migliori
La maggior parte della ricerca sul cancro si basa ancora su strati cellulari piatti coltivati su piastre di plastica. Questi sono facili da gestire ma riproducono male il comportamento dei tumori nell’organismo, dove le cellule si spingono attraverso il tessuto circostante in tre dimensioni. In questo studio, gli scienziati hanno lavorato con tre note linee cellulari di carcinoma renale, di cui si sapeva già fossero caratterizzate da differenti caratteristiche genetiche e di segnalazione. Hanno formato ciascun tipo cellulare in ammassi sferici compatti, quindi hanno incorporato questi ammassi in un gel morbido di collagene e fibronectina con rigidità simile a quella del tessuto renale reale. Per una settimana hanno monitorato quanto lontano e quanto velocemente le cellule tumorali si staccavano dal sferoide e invadevano il gel circostante, tracciando i percorsi delle singole cellule. 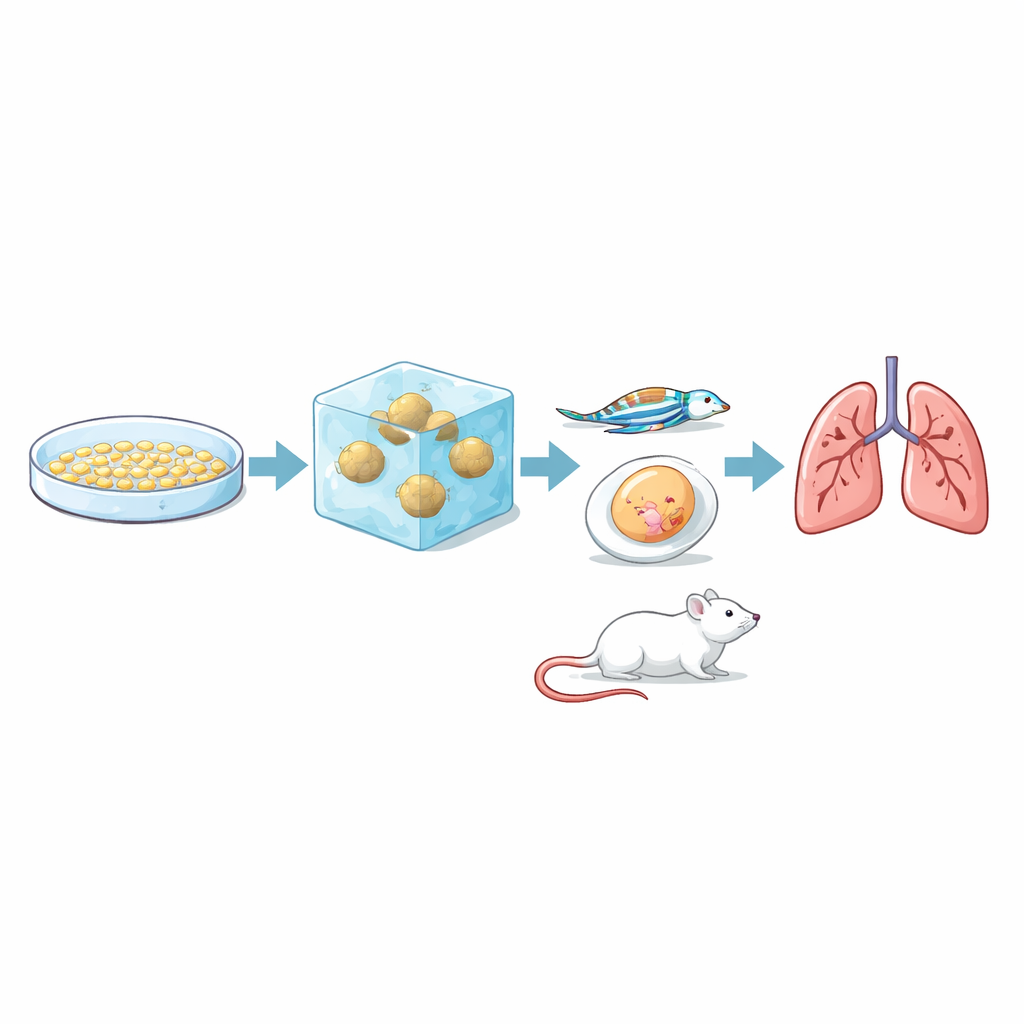
Classificare le cellule tumorali in base alla loro propensione a invadere
Le tre linee cellulari hanno mostrato comportamenti nettamente diversi in questo ambiente 3D. Una linea, chiamata RCC10, è rimasta per lo più come una palla compatta con solo un movimento esterno minimo. Una seconda linea, 786-O, ha inviato cellule nel gel, ma solo in misura moderata. La terza linea, RCC7, è stata la più aggressiva: le sue cellule si sono spinte profondamente nel gel, hanno occupato un’area maggiore e si sono mosse a velocità più elevate. I percorsi tracciati dalle singole cellule di RCC7 e 786-O erano tortuosi ed esplorativi, con frequenti cambi di direzione, mentre le cellule RCC10 tendevano a muoversi in modo più lineare e limitato. Il blocco di una via di segnalazione chiave (la via TGFβ) negli sferoidi più invasivi ha ridotto significativamente la loro capacità di fuggire nel gel, confermando che il modello risponde a farmaci che mirano ai meccanismi associati all’invasione.
Testare le previsioni in organismi viventi
La domanda cruciale era se questo test di invasione in laboratorio rispecchiasse realmente il comportamento dei tumori in organismi viventi. Per verificarlo, il team ha iniettato le stesse tre linee cellulari in diversi modelli animali che catturano fasi differenti della metastasi. Nei membrane dell’uovo di gallina, tutte e tre hanno formato tumori, ma RCC7 ha prodotto masse più grandi, piene di sangue e più eterogenee. In embrioni di zebrafish trasparenti, i ricercatori hanno osservato cellule tumorali marcate fluorescentemente viaggiare nei vasi sanguigni: le cellule RCC7 e 786-O si sono attaccate alle pareti vascolari e sono fuoriuscite nel tessuto circostante più spesso rispetto alle cellule RCC10. Nei topi, le cellule RCC7 e 786-O hanno formato metastasi ai polmoni in modo affidabile, con RCC7 che lo ha fatto più rapidamente e in modo più esteso, mentre RCC10 non ha prodotto metastasi polmonari rilevabili nel periodo dello studio. Complessivamente, la classifica vista nel gel 3D—RCC7 più invasivo, 786-O intermedio, RCC10 meno invasivo—coincideva con il loro comportamento negli animali. 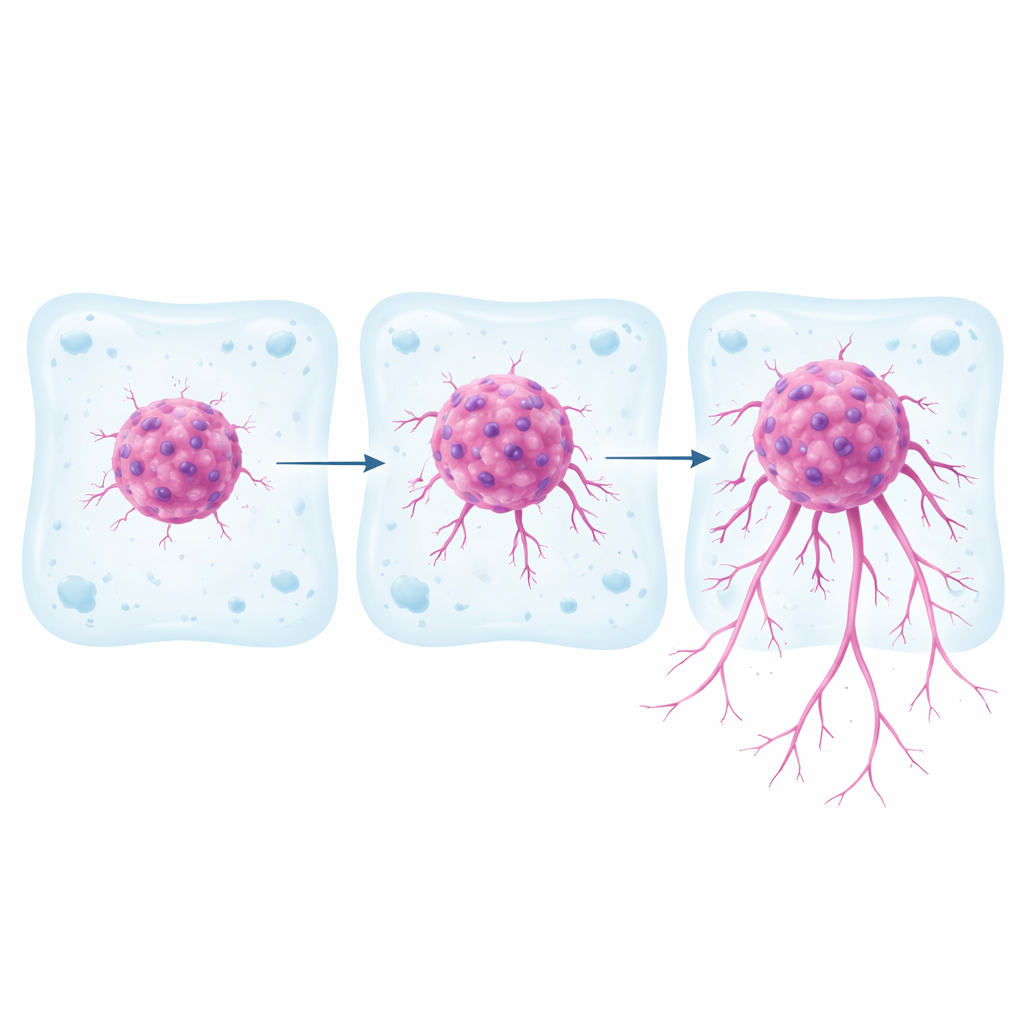
Estendere l’approccio ai tumori dei pazienti
Per avvicinarsi alla realtà clinica, i ricercatori hanno anche creato tumoroidi 3D a partire da campioni tumorali freschi prelevati da due pazienti affetti da carcinoma renale con differenti gradi patologici standard. Coltivati nello stesso sistema a gel, i tumoroidi derivati dal tumore di grado più elevato hanno invaso rapidamente e hanno inviato molti rami esplorativi, mentre quelli derivati dal tumore di grado inferiore sono rimasti più compatti e lenti nei movimenti. La maggior parte delle cellule invasive presentava un noto marcatore del carcinoma renale, confermando che provenivano dal tumore e non dalle cellule normali circostanti. Sebbene il campione di pazienti sia piccolo, i risultati suggeriscono che il comportamento di invasione 3D dei tumoroidi di un paziente potrebbe riflettere la gravità della sua malattia.
Cosa significa questo per i pazienti
Questo lavoro mostra che un test di laboratorio 3D relativamente semplice può rispecchiare come le cellule del carcinoma renale si diffondono in organismi viventi. Osservando quanto lontano e quanto dinamicamente le cellule fuggono dai mini-tumori in un gel realistico, gli scienziati possono distinguere tra tumori con potenziale metastatico basso, medio e alto. In futuro, tali saggi di tumoroidi 3D, combinati con la classificazione microscopica standard e i test genetici, potrebbero aiutare i medici a prevedere meglio quali carcinomi renali sono destinati a metastatizzare e a personalizzare di conseguenza il trattamento. Potrebbero inoltre offrire una piattaforma etica e più veloce per testare nuovi farmaci mirati a fermare la diffusione del cancro prima che cominci.
Citazione: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
Parole chiave: cancro al rene, tumoroidi, coltura cellulare 3D, metastasi, carcinoma a cellule renali