Clear Sky Science · es
Uso de propiedades de invasión 3D de líneas celulares de CCR in vitro para predecir su potencial metastásico in vivo
Por qué importa esta investigación
Cuando el cáncer de riñón se disemina a otros órganos, su tratamiento se complica mucho más. Los médicos querrían saber desde temprano qué tumores probablemente permanecerán localizados y cuáles tienen más propensión a viajar. Este estudio demuestra que, al cultivar células de cáncer de riñón en mini-tumores tridimensionales diseñados en el laboratorio, los investigadores pueden prever con qué agresividad se diseminarán esos cánceres en animales vivos. El trabajo apunta hacia pruebas de laboratorio que algún día podrían evitar tratamientos innecesarios a ciertos pacientes y, a la vez, identificar a quienes necesitan atención rápida e intensiva.
Construir mejores mini-tumores
La mayor parte de la investigación sobre cáncer aún depende de capas celulares planas cultivadas en placas de plástico. Son fáciles de manejar, pero reproducen de forma pobre el comportamiento tumoral dentro del cuerpo, donde las células avanzan a través del tejido circundante en tres dimensiones. En este estudio, los científicos trabajaron con tres líneas celulares de cáncer de riñón bien conocidas, que ya sabían que presentaban distintas características genéticas y de señalización. Formaron cada tipo celular en cúmulos esféricos compactos y luego incrustaron esos cúmulos en un gel blando hecho de colágeno y fibronectina que coincide con la rigidez del tejido renal real. Durante una semana, siguieron la distancia y la velocidad con que las células cancerosas se separaban del esferoide e invadían el gel circundante, y trazaron las trayectorias de células individuales. 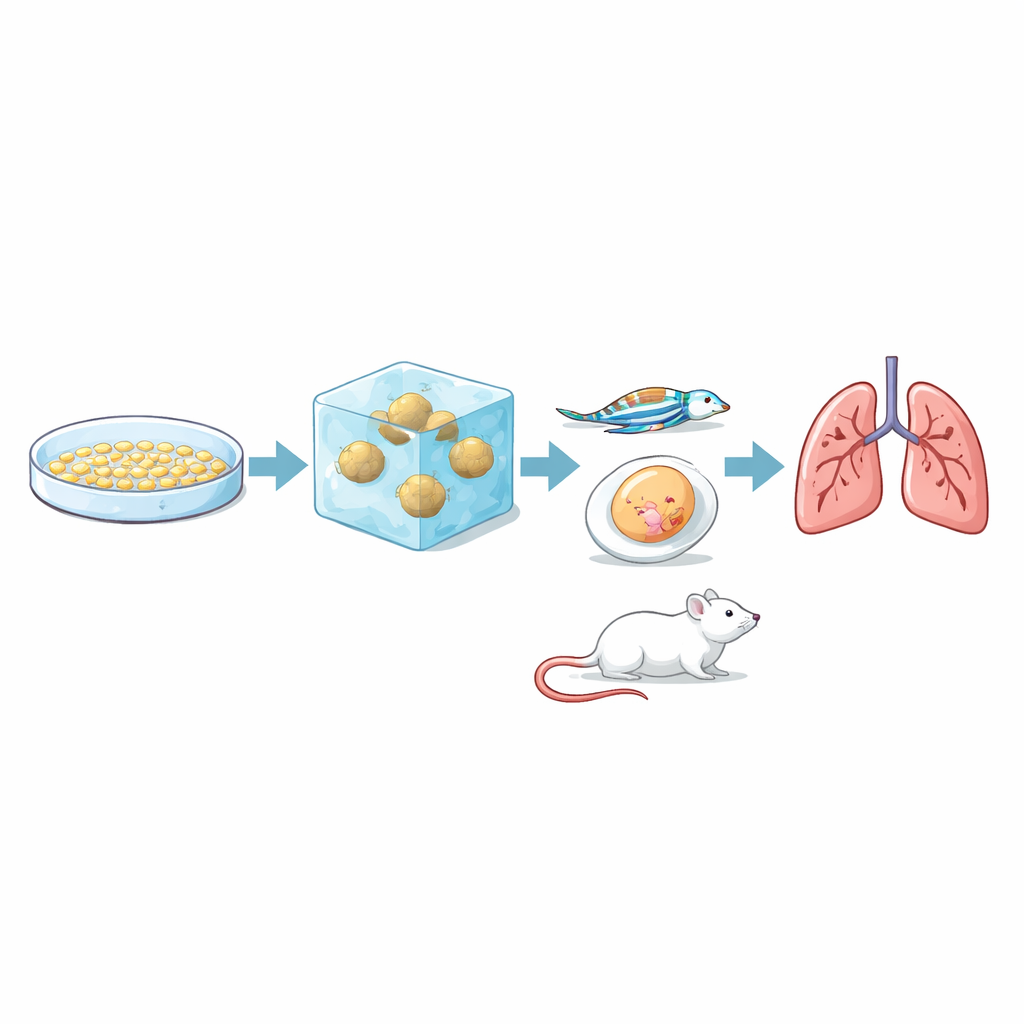
Clasificando las células cancerosas por su impulso de invadir
Las tres líneas celulares mostraron comportamientos marcadamente diferentes en este entorno 3D. Una línea, llamada RCC10, permaneció mayormente como una bola compacta con solo un movimiento exterior mínimo. Una segunda línea, 786-O, envió células al gel, pero solo en grado moderado. La tercera línea, RCC7, fue la más agresiva: sus células penetraron profundamente en el gel, ocuparon una área mayor y se movieron a velocidades superiores. Las trayectorias trazadas por células individuales de RCC7 y 786-O fueron errantes y exploratorias, con cambios frecuentes de dirección, mientras que las células de RCC10 tendieron a moverse de forma más recta y limitada. Bloquear una vía clave de señalización (la vía TGFβ) en los esferoides más invasivos redujo significativamente su capacidad para escapar al gel, lo que confirma que el modelo responde a fármacos que atacan mecanismos relacionados con la invasión.
Probar las predicciones en animales vivos
La pregunta crucial era si esta prueba de invasión en laboratorio realmente refleja cómo se comportan los tumores en organismos reales. Para comprobarlo, el equipo inyectó las mismas tres líneas celulares en varios modelos animales que reproducen distintas etapas de la metástasis. En membranas de huevo de gallina, las tres formaron tumores, pero RCC7 produjo masas más grandes, llenas de sangre y más heterogéneas. En embriones transparentes de pez cebra, los investigadores observaron células cancerosas marcadas con fluorescencia desplazarse por los vasos sanguíneos: las células RCC7 y 786-O se adhirieron a las paredes vasculares y salieron al tejido circundante con mayor frecuencia que las RCC10. En ratones, las células RCC7 y 786-O formaron metástasis pulmonares de forma consistente, siendo RCC7 más rápida y extensa, mientras que RCC10 no produjo metástasis pulmonares detectables durante el periodo del estudio. En conjunto, la clasificación vista en el gel 3D —RCC7 más invasiva, 786-O intermedia, RCC10 menos invasiva— coincidió con su comportamiento en animales. 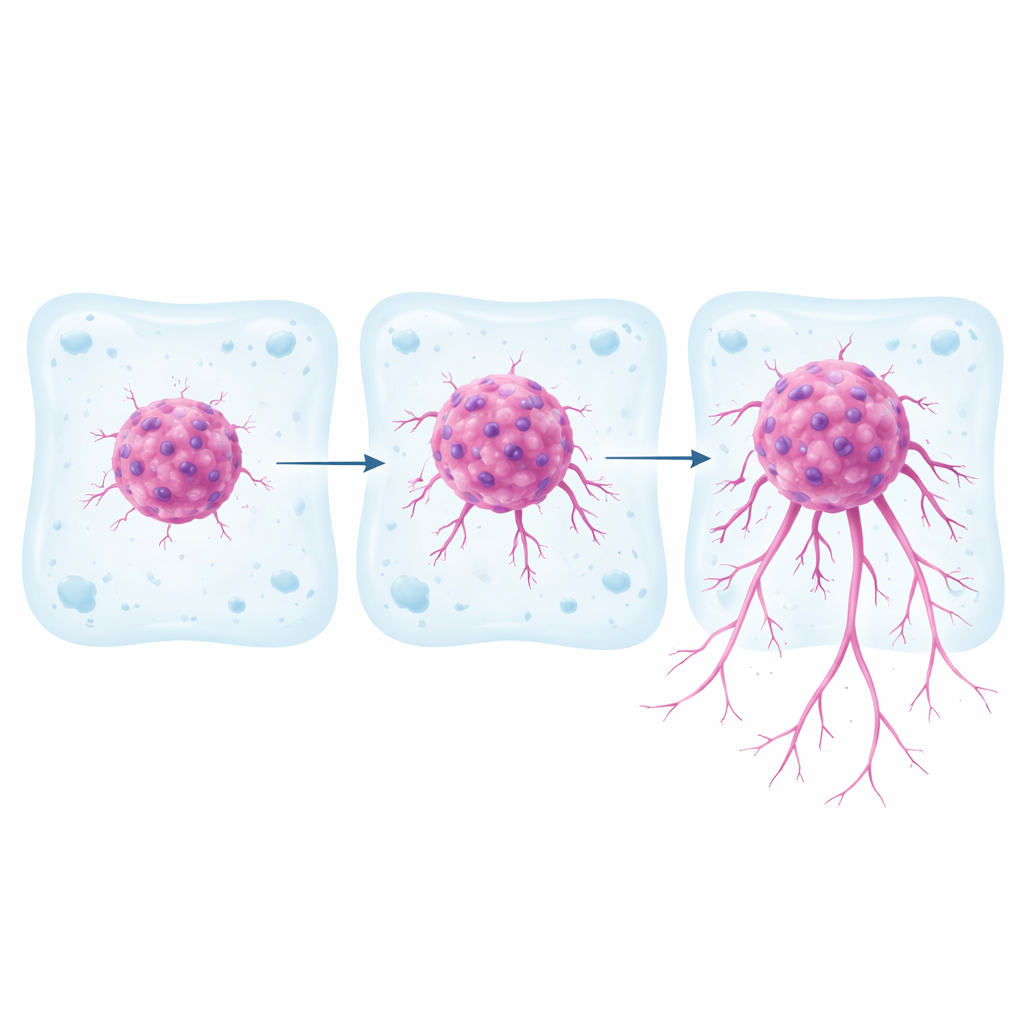
Extender el enfoque a tumores de pacientes
Para acercarse a la realidad clínica, los investigadores también crearon "tumoroides" 3D a partir de muestras frescas de tumor tomadas de dos pacientes con cáncer de riñón cuyos tumores tenían grados patológicos estándar diferentes. Cultivados en el mismo sistema de gel, los tumoroides del tumor de mayor grado invadieron rápidamente y enviaron muchas ramas exploratorias, mientras que los del tumor de menor grado permanecieron más compactos y se movieron con lentitud. La mayoría de las células invasoras portaban un marcador conocido del cáncer renal, confirmando que provenían del tumor y no de las células normales circundantes. Aunque la muestra de pacientes es pequeña, los resultados sugieren que el comportamiento de invasión 3D de los tumoroides de un paciente podría reflejar la gravedad de su enfermedad.
Qué significa esto para los pacientes
Este trabajo muestra que una prueba de laboratorio 3D relativamente simple puede reflejar cómo las células de cáncer de riñón se diseminan en animales vivos. Al observar hasta qué distancia y con qué dinamismo las células escapan de mini-tumores en un gel realista, los científicos pueden distinguir entre cánceres con bajo, medio y alto potencial metastásico. En el futuro, ensayos de tumoroides 3D como este, combinados con la gradación microscópica estándar y pruebas genéticas, podrían ayudar a los médicos a predecir mejor qué cánceres de riñón son más propensos a metastatizar y adaptar el tratamiento en consecuencia. También podrían proporcionar una plataforma ética y más rápida para probar nuevos fármacos dirigidos a detener la diseminación del cáncer antes de que comience.
Cita: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
Palabras clave: cáncer de riñón, tumoroides, cultivo celular 3D, metástasis, carcinoma de células renales