Clear Sky Science · nl
Gebruik van 3D-invasie-eigenschappen van RCC-cellijnen in vitro om hun metastatische potentieel in vivo te voorspellen
Waarom dit onderzoek telt
Wanneer nierenkanker zich naar andere organen verspreidt, wordt de behandeling veel moeilijker. Artsen willen vroeg kunnen inschatten welke tumoren waarschijnlijk op de plaats blijven en welke de neiging hebben zich te verspreiden. Deze studie laat zien dat door nierkankercellen in zorgvuldig ontworpen driedimensionale mini‑tumoren in het laboratorium te kweken, onderzoekers kunnen voorspellen hoe agressief die kankers zich in levende dieren zullen verspreiden. Het werk wijst op laboratoriumtests die op een dag sommige patiënten mogelijk kunnen behoeden voor onnodige behandelingen, terwijl anderen die snelle, intensieve zorg nodig hebben eerder worden geïdentificeerd.
Betere mini‑tumoren bouwen
Het merendeel van het kankeronderzoek berust nog steeds op platte cellagen gekweekt op plastic schaaltjes. Die zijn makkelijk te hanteren maar bootsen slecht na hoe tumoren zich in het lichaam gedragen, waar cellen zich driedimensionaal door omliggend weefsel heen bewegen. In deze studie werkten wetenschappers met drie goed onderzochte nierkankercellijnen, waarvan ze al wisten dat ze verschillende genetische en signaalkenmerken dragen. Ze vormden van elk celltype compacte bolvormige clusters en ingebedde deze clusters vervolgens in een zachte gel van collageen en fibronectine met een stijfheid die overeenkomt met echt nierweefsel. Gedurende een week volgden ze hoe ver en hoe snel kankercellen zich losmaakten van het spheroid en het omliggende gel infiltreerden, en ze brachten de trajecten van individuele cellen in kaart. 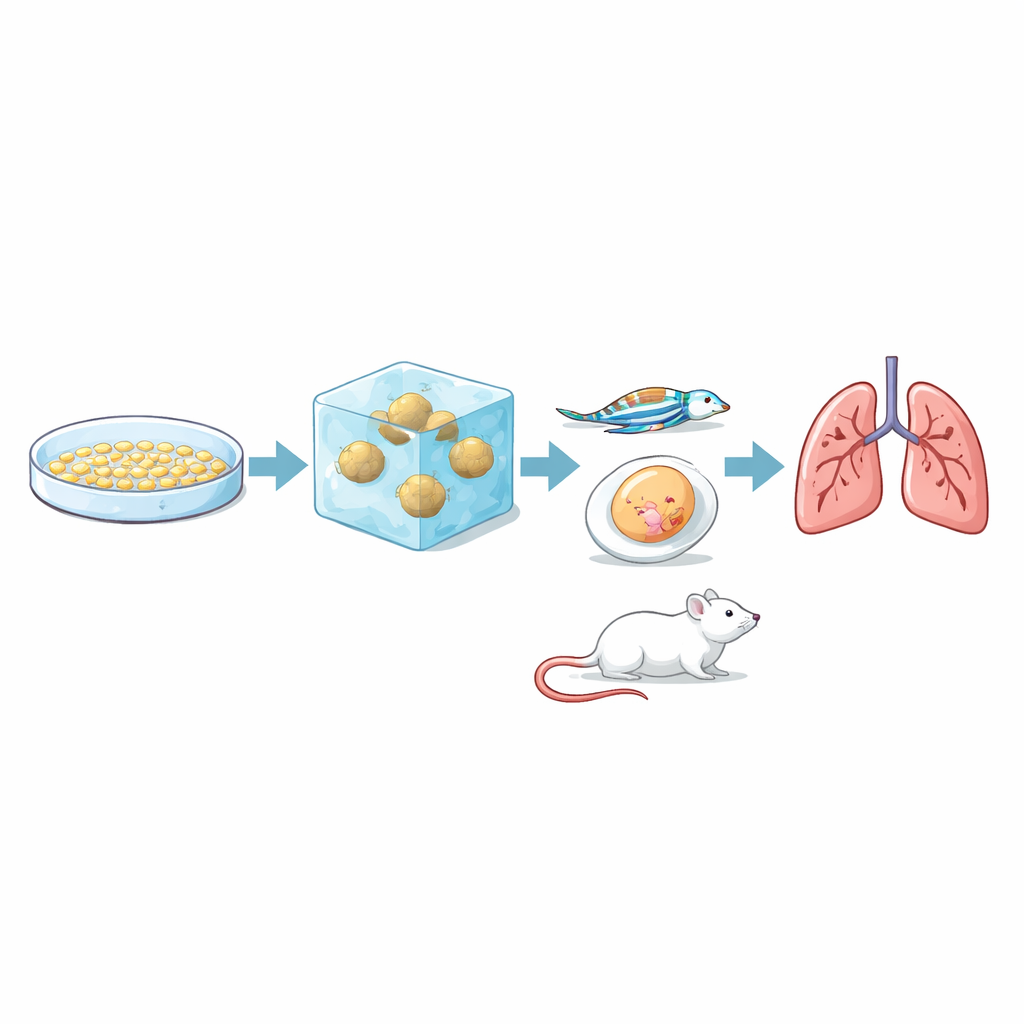
Cellen rangschikken op hun neiging tot invasie
De drie cellijnen vertoonden duidelijk verschillende gedragingen in deze 3D‑omgeving. Eén lijn, RCC10 genoemd, bleef grotendeels een compacte bol met slechts minimale uitwaartse beweging. Een tweede lijn, 786‑O, stuurde cellen het gel in, maar slechts in beperkte mate. De derde lijn, RCC7, was het meest agressief: de cellen stroomden ver het gel in, bedekten een groter oppervlak en bewoog met hogere snelheden. De door individuele RCC7‑ en 786‑O‑cellen getraceerde paden waren kronkelig en verkennend, met frequente koerswisselingen, terwijl RCC10‑cellen de neiging hadden rechtlijniger en beperkter te bewegen. Het blokkeren van een belangrijk signaalpad (het TGFβ‑pad) in de meer invasieve spheroïden verminderde hun vermogen om in het gel te ontsnappen aanzienlijk, wat bevestigt dat het model reageert op middelen die invasiegerelateerde mechanismen remmen.
Voorspellingen testen in levende dieren
De cruciale vraag was of deze in het lab uitgevoerde invasietest daadwerkelijk weerspiegelt hoe tumoren zich in echte organismen gedragen. Om dat te achterhalen, injecteerde het team dezelfde drie cellijnen in verschillende diermodellen die uiteenlopende stadia van metastase vangen. In membranen van kippenembryo’s vormden alle drie tumoren, maar RCC7 produceerde grotere, met bloed gevulde en meer variërende massa’s. In transparante zebravis‑embryo’s observeerden de onderzoekers fluorescerend gelabelde kankercellen die door bloedvaten reisden: RCC7‑ en 786‑O‑cellen hechtten vaker aan vaatwanden en verlieten vaker de vaten naar omliggend weefsel dan RCC10‑cellen. In muizen vormden RCC7‑ en 786‑O‑cellen betrouwbaar longmetastasen, waarbij RCC7 dit sneller en uitgebreider deed, terwijl RCC10 binnen de studieduur geen detecteerbare longmetastasen gaf. Gecombineerd kwam de rangorde in de 3D‑gel—RCC7 meest invasief, 786‑O intermediair, RCC10 minst—overeen met hun gedrag in dieren. 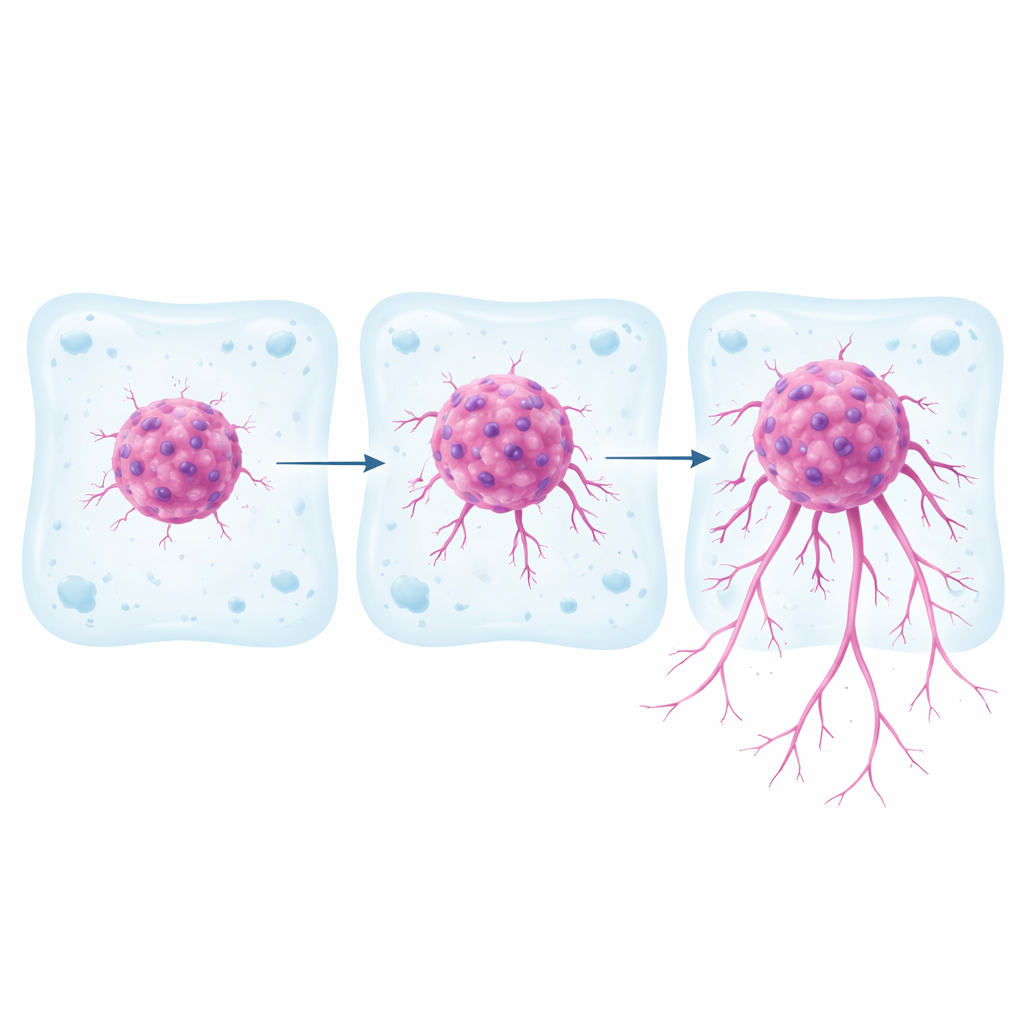
De aanpak uitbreiden naar patiënstumoren
Om dichter bij de klinische praktijk te komen, maakten de onderzoekers ook 3D‑"tumoroïden" van verse tumormonsters van twee nierkankerpatiënten met verschillende standaard pathologierapporten. In hetzelfde gelsysteem gekweekt, drongen tumoroïden van de hooggradige tumor snel naar buiten en stuurden veel verkennende uitlopers, terwijl die van de laaggradige tumor compacter en langzamer bleven. De meeste invaderende cellen droegen een bekende marker voor nierkanker, wat bevestigt dat ze uit de tumor afkomstig waren en niet uit omliggend normaal weefsel. Hoewel dit patiëntmonster klein is, suggereren de resultaten dat het 3D‑invasiegedrag van iemands tumoroïden de ernst van de ziekte zou kunnen weerspiegelen.
Wat dit betekent voor patiënten
Dit werk toont aan dat een relatief eenvoudige 3D‑labtest kan weergeven hoe nierkankercellen zich in levende dieren verspreiden. Door te observeren hoe ver en hoe dynamisch cellen zich uit mini‑tumoren in een realistisch gel verwijderen, kunnen wetenschappers onderscheid maken tussen kankers met laag, middelhoog en hoog metastatisch potentieel. In de toekomst zouden zulke 3D‑tumoroïde‑assays, gecombineerd met standaard microscopische gradatie en genetische tests, artsen beter kunnen helpen voorspellen welke nierkankers waarschijnlijk zullen uitzaaien en de behandeling daarop afstemmen. Ze zouden ook een ethisch verantwoorde, snellere testplatform kunnen bieden om nieuwe middelen te beoordelen die gericht zijn op het stoppen van kankerspreiding nog voordat die begint.
Bronvermelding: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
Trefwoorden: nierkanker, tumoroïden, 3D-celkweek, metastase, renale celcarcinoom