Clear Sky Science · de
Verwendung 3D-invasiver Eigenschaften von RCC-Zelllinien in vitro zur Vorhersage ihres metastatischen Potenzials in vivo
Warum diese Forschung wichtig ist
Wenn Nierenkrebs in andere Organe streut, wird die Behandlung deutlich schwieriger. Ärzte möchten möglichst früh wissen, welche Tumoren lokal bleiben und welche zur Metastasierung neigen. Diese Studie zeigt, dass man durch das Wachstum von Nierenkrebszellen in sorgfältig gestalteten dreidimensionalen Mini-Tumoren im Labor vorhersagen kann, wie aggressiv diese Tumoren in lebenden Tieren streuen werden. Die Arbeit weist auf Labortests hin, die eines Tages einigen Patienten unnötige Behandlungen ersparen und andere identifizieren könnten, die schnelle, intensive Betreuung benötigen.
Bessere Mini-Tumoren erzeugen
Die meiste Krebsforschung beruht noch immer auf flachen Zellschichten, die auf Kunststoffschalen gezüchtet werden. Diese sind einfach zu handhaben, ahmen aber schlecht nach, wie Tumoren im Körper funktionieren, wo Zellen dreidimensional durch umgebendes Gewebe dringen. In dieser Studie arbeiteten Wissenschaftler mit drei bekannten Nierenkrebs-Zelllinien, von denen bereits bekannt war, dass sie unterschiedliche genetische und Signalmerkmale tragen. Sie formten jeden Zelltyp zu kompakten sphärischen Clustern und betteten diese Cluster in ein weiches Gel aus Kollagen und Fibronectin ein, das in seiner Steifigkeit echtem Nierengewebe ähnelt. Über eine Woche verfolgten sie, wie weit und wie schnell Krebszellen sich vom Sphäroid lösten und in das umgebende Gel eindrangen, und zeichneten die Bahnen einzelner Zellen auf. 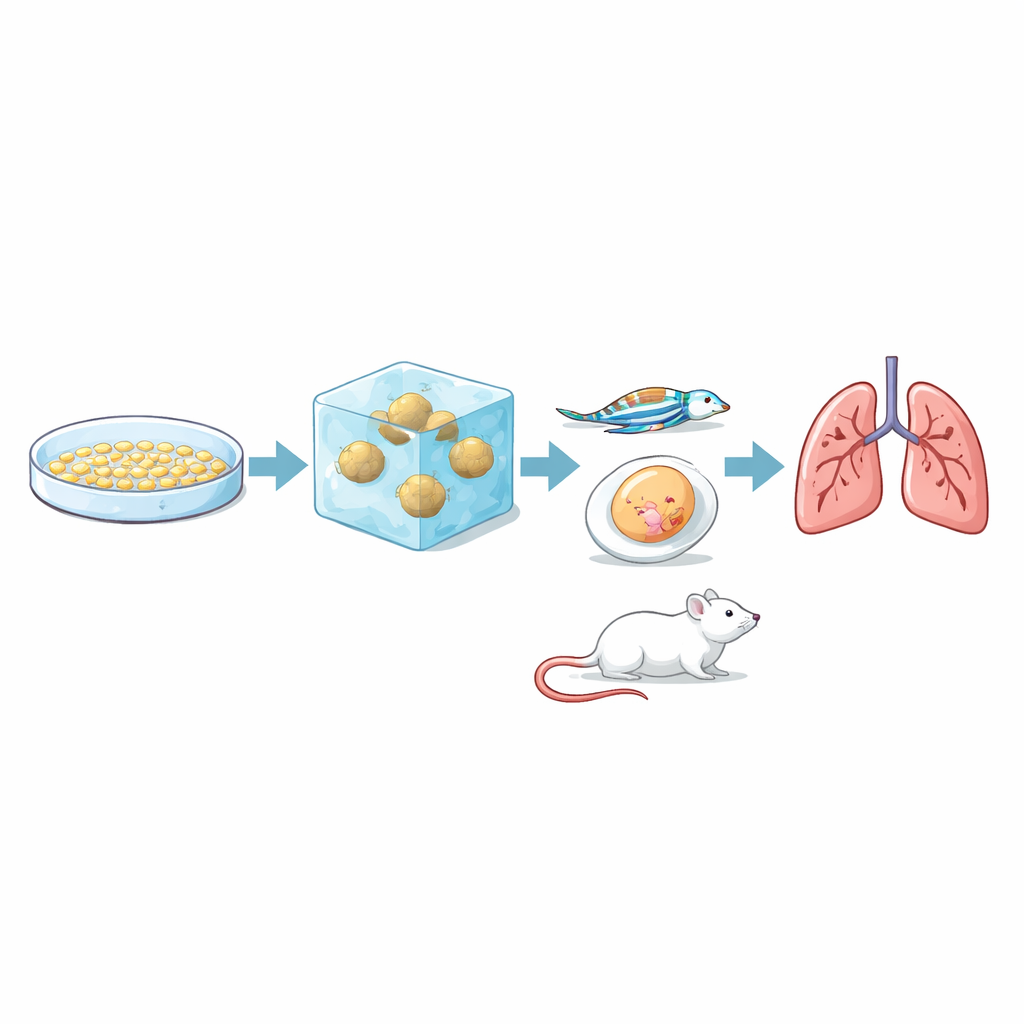
Einstufung von Krebszellen nach Invasionsdrang
Die drei Zelllinien zeigten in diesem 3D-Setting stark unterschiedliche Verhaltensweisen. Eine Linie, genannt RCC10, blieb größtenteils als dichter Ball mit nur minimaler Auswärtsbewegung erhalten. Eine zweite Linie, 786-O, sandte Zellen ins Gel, jedoch nur in mittlerem Ausmaß. Die dritte Linie, RCC7, war am aggressivsten: Ihre Zellen strömten weit ins Gel, bedeckten eine größere Fläche und bewegten sich mit höheren Geschwindigkeiten. Die von einzelnen RCC7- und 786-O-Zellen gezeichneten Bahnen wirkten verschlungen und erkundend, mit häufigen Richtungswechseln, während RCC10-Zellen eher geradlinig und begrenzter unterwegs waren. Die Blockade einer wichtigen Signalroute (dem TGFβ-Signalweg) in den stärker invasiven Sphäroiden verringerte deren Fähigkeit, ins Gel zu entkommen, deutlich und bestätigte, dass das Modell auf Wirkstoffe reagiert, die invasionsbezogene Mechanismen angreifen.
Vorhersagen in lebenden Tieren testen
Die entscheidende Frage war, ob dieser laborbasierte Invasionstest tatsächlich widerspiegelt, wie Tumoren in realen Organismen verhalten. Um das herauszufinden, injizierte das Team dieselben drei Zelllinien in mehrere Tiermodelle, die verschiedene Stadien der Metastasierung abbilden. In Hühner-Ei-Membranen bildeten alle drei Tumoren, doch RCC7 erzeugte größere, blutgefüllte und vielfältigere Massen. In transparenten Zebrafisch-Embryonen beobachteten die Forscher fluoreszenzmarkierte Krebszellen, die sich durch Blutgefäße bewegten: RCC7- und 786-O-Zellen hafteten häufiger an Gefäßwänden und traten öfter in das umgebende Gewebe aus als RCC10-Zellen. In Mäusen bildeten RCC7- und 786-O-Zellen zuverlässig Metastasen in der Lunge, wobei RCC7 dies schneller und ausgedehnter tat, während RCC10 innerhalb des Untersuchungszeitraums keine nachweisbaren Lungenmetastasen erzeugte. Insgesamt entsprach die im 3D-Gel beobachtete Rangfolge — RCC7 am invasivsten, 786-O mittel, RCC10 am wenigsten — ihrem Verhalten in Tieren. 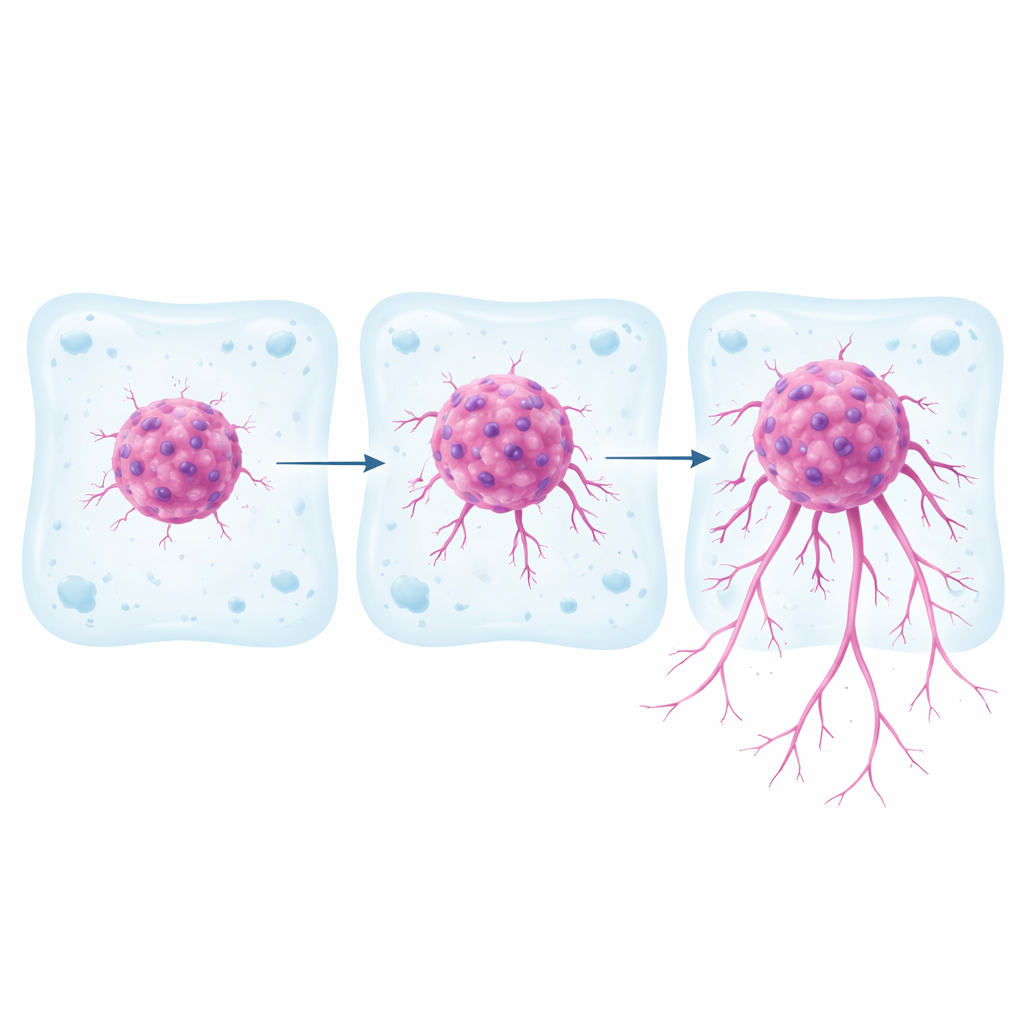
Ansatz auf Patiententumoren ausdehnen
Um der klinischen Realität näherzukommen, erzeugten die Forscher außerdem 3D-Tumoroide aus frischen Tumorproben von zwei Nierenkrebspatienten, deren Tumoren unterschiedliche Standard-Pathologiegrade aufwiesen. In demselben Gelsystem kultiviert, drangen Tumoroide aus dem höhergradigen Tumor schnell ein und bildeten viele erkundende Verzweigungen, während die Tumoroide des niedergradigeren Tumors kompakter und langsamer blieben. Die meisten der invasiven Zellen trugen einen bekannten Nierenkrebsmarker, was bestätigte, dass sie vom Tumor stammten und nicht von umgebendem Normalgewebe. Auch wenn die Patientenstichprobe klein ist, deuten die Ergebnisse darauf hin, dass das 3D-Invasionsverhalten der Tumoroide eines Patienten die Ernsthaftigkeit seiner Erkrankung widerspiegeln könnte.
Was das für Patienten bedeutet
Diese Arbeit zeigt, dass ein relativ einfacher 3D-Labortest das Verhalten von Nierenkrebszellen in lebenden Tieren abbilden kann. Indem man beobachtet, wie weit und wie dynamisch Zellen aus Mini-Tumoren in einem realistischen Gel entkommen, können Forscher zwischen Tumoren mit niedrigem, mittlerem und hohem metastatischem Potenzial unterscheiden. Künftige 3D-Tumoroid-Assays könnten in Kombination mit standardmäßiger mikroskopischer Einstufung und Gentests Ärzten helfen, besser vorherzusagen, welche Nierenkrebserkrankungen wahrscheinlich metastasieren, und die Behandlung entsprechend zu individualisieren. Sie könnten zudem eine ethisch vertretbarere und schnellere Plattform bieten, um neue Medikamente zu testen, die darauf abzielen, die Ausbreitung von Krebs schon im Frühstadium zu stoppen.
Zitation: Cesana, B., Nemoz-Billet, L., Azemard, V. et al. Using 3D Invasion properties of RCC Cell Lines In Vitro to predict their Metastatic Potential In Vivo. Cell Death Discov. 12, 122 (2026). https://doi.org/10.1038/s41420-026-02966-7
Schlüsselwörter: Nierenkrebs, Tumoroide, 3D-Zellkultur, Metastase, Nierenzellkarzinom