Clear Sky Science · zh
依维莫司抑制葡萄糖转运蛋白3的膜转运以改善脐血来源间充质干细胞移植在糖尿病视网膜病变中的治疗效果
为何在糖尿病中保护视力至关重要
长期患糖尿病的人常常担心视力丧失。糖尿病视网膜病变是一种常见的眼部并发症,高血糖会逐步损害视网膜中脆弱的血管和神经细胞。目前的药物注射可以减缓病情进展,但无法完全恢复眼内精细组织。本研究探讨了一种再生疗法:使用来自脐带血的干细胞,并展示了一种名为依维莫司的抗癌药如何使这些细胞在类似糖尿病眼内的高糖环境中更好地存活。
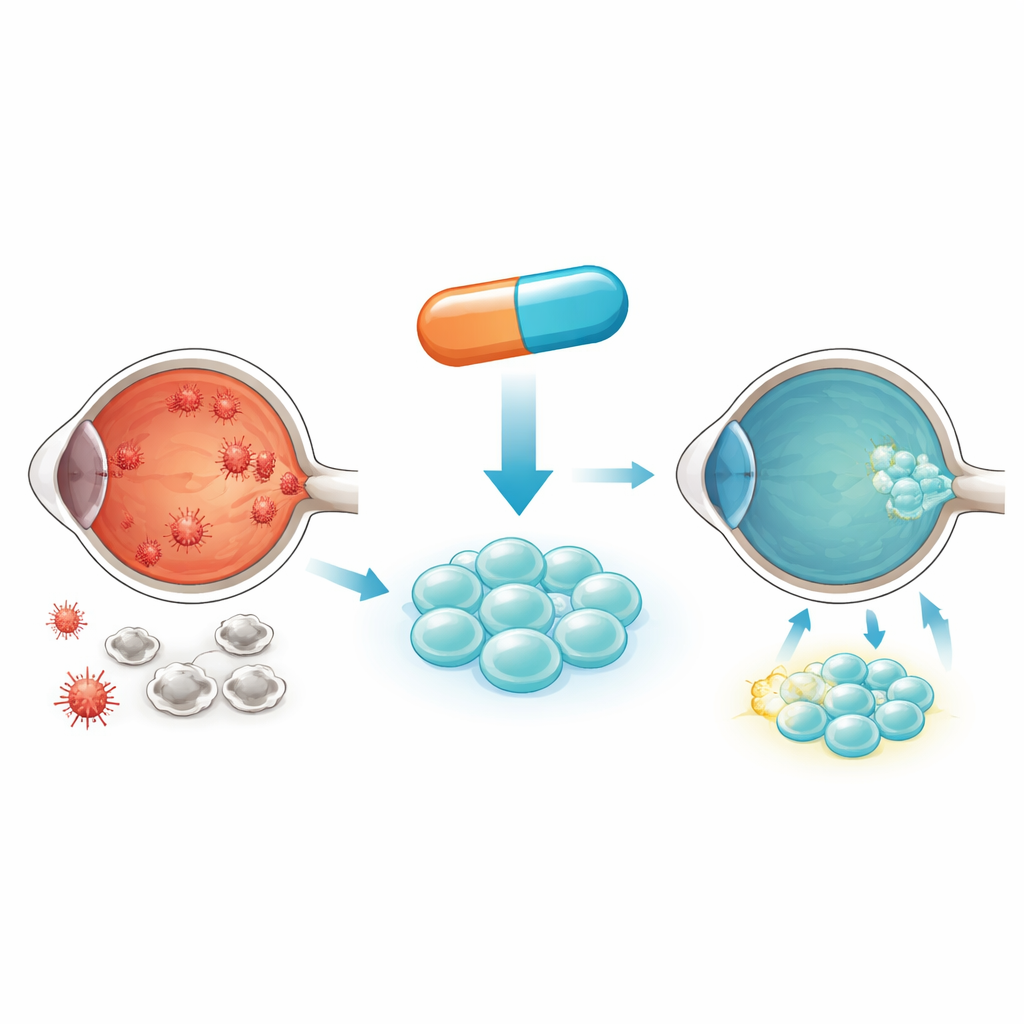
糖尿病如何伤害眼睛及移入的干细胞
在糖尿病中,多余的糖不断浸泡细胞。细胞内,这些糖在称为线粒体的微小能量工厂中被燃烧,当负荷过重时会释放有害的活性氧种。随着时间推移,这种氧化应激促使细胞过早衰老并死亡。作者关注的是脐带血来源的间充质干细胞,这类细胞可以支持并修复受损的视网膜组织。不幸的是,当这些干细胞被置于类似糖尿病血液的高糖条件下时,它们会摄取过多葡萄糖,产生过度的线粒体应激并开始死亡,从而导致能够帮助修复视网膜的健康细胞数量减少。
造成最大损害的“糖门”
细胞在膜上使用专门的通道,即葡萄糖转运蛋白,来让糖进入。研究团队检查了这些干细胞上两种主要类型:GLUT1 和 GLUT3。当研究者将细胞暴露在高糖环境数小时后,两种转运蛋白的表达均上升,葡萄糖摄取增加。但通过使用遗传工具有选择性地沉默每一种通道,他们发现 GLUT3 在驱动线粒体应激方面起主导作用。阻断 GLUT3 明显减少有害氧种的积累,稳定线粒体功能,并降低总体葡萄糖摄取。当这些被沉默 GLUT3 的干细胞移植到患有糖尿病视网膜病变的大鼠眼中时,视网膜的电生理信号和光感受器层厚度的改善比未改造的干细胞更为显著。
将抗癌药重新用于保护干细胞
研究者接着询问是否可以用小分子药物模拟对 GLUT3 的控制带来的益处。他们选择了依维莫司,它可以阻断细胞内一个关键的生长与代谢中心——mTOR。在高糖条件下,干细胞的 mTOR 信号显著激活。依维莫司抑制了该信号,减少了葡萄糖进入,并比旧药拉帕霉素更有效地降低线粒体氧化应激。在低纳摩尔剂量下,依维莫司维持了线粒体膜电位,恢复细胞的抗氧化防御,并降低了程序性细胞死亡的标志物。在糖尿病视网膜病变的大鼠中,使用依维莫司预处理的干细胞进行结膜下注射后,视网膜电生理反应恢复更强,视网膜结构保护也优于未处理的干细胞。
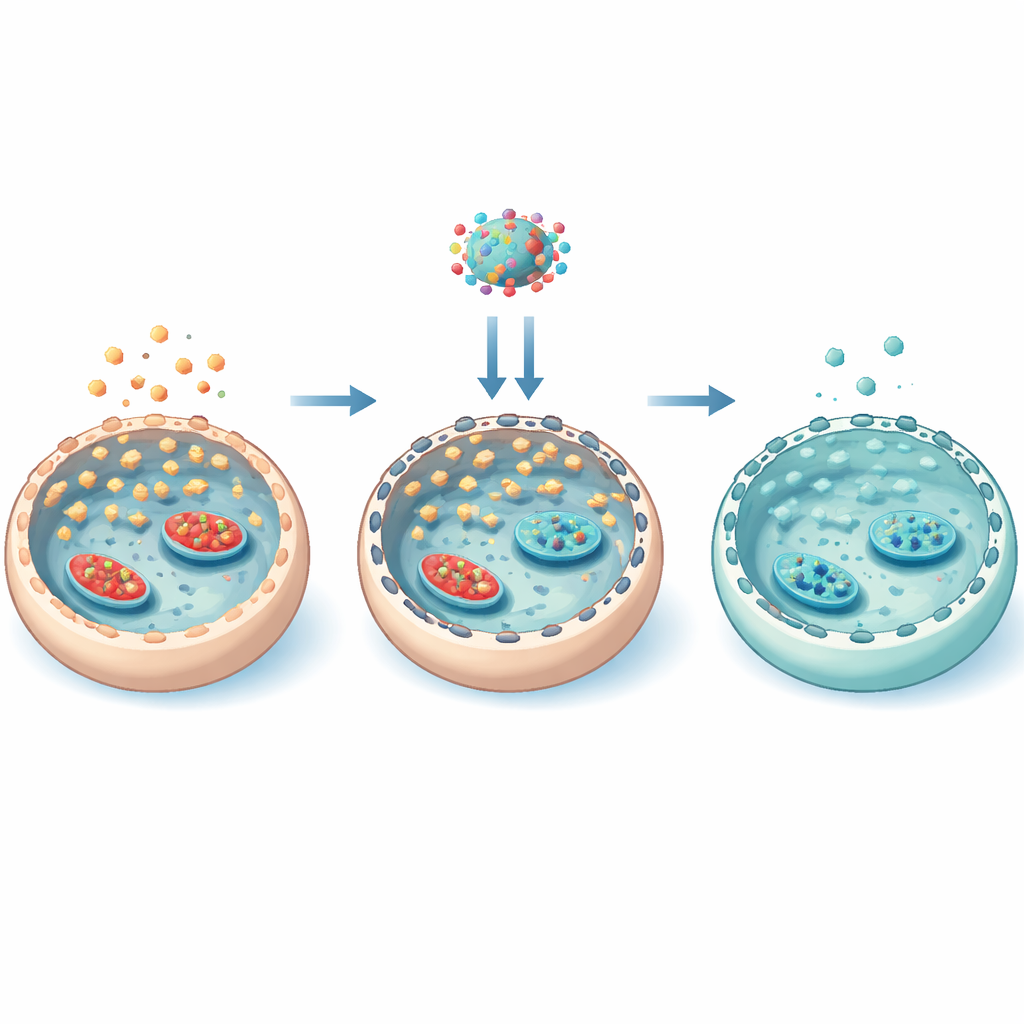
控制糖进入的隐蔽支架
为了解依维莫司为何具有如此特异性的作用,团队将视角放在细胞内的肌动蛋白丝骨架上。在高糖条件下,mTOR 活性增加导致一种名为 cofilin 的蛋白被磷酸化,这会将肌动蛋白锁定为更稳定的丝状结构。这个稳定的骨架有助于将 GLUT3 通道移动到细胞表面,从而增加糖的进入。依维莫司逆转了这一链条:它降低了 mTOR 活性,减少了 cofilin 的磷酸化,放松了肌动蛋白网络,并将 GLUT3 从膜上撤回。通过稳定或破坏肌动蛋白的实验证实,这种骨架的物理重排对于控制 GLUT3 的定位至关重要。值得注意的是,依维莫司并没有广泛重编程所有葡萄糖代谢酶;相反,它主要通过转运蛋白的位置来调控糖的进入量。
这些发现对未来眼部治疗的意义
对非专业读者来说,结论是:研究表明预处理干细胞可以帮助它们在糖尿病眼内这种苛刻的高糖环境中存活。通过在移植前使用依维莫司,研究者能够关闭细胞上的部分“糖门”,缓解过度工作的线粒体并防止早期细胞死亡。在动物模型中,这些更强韧的干细胞在保护与重建视网膜组织、改善视网膜功能方面表现更好。尽管在将该方法用于患者之前仍需更多工作,但这项研究指向了一个务实的策略:在输送前调整细胞的糖摄入和应激反应,让它们准备好修复糖尿病视网膜,而不是被其压垮。
引用: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
关键词: 糖尿病视网膜病变, 间充质干细胞, 依维莫司, 氧化应激, 葡萄糖转运蛋白