Clear Sky Science · es
Everolimus suprime el tráfico de membrana del transportador de glucosa 3 para mejorar la eficacia terapéutica del trasplante de células madre mesenquimales derivadas de sangre de cordón umbilical en la retinopatía diabética
Por qué es importante proteger la visión en la diabetes
Las personas con diabetes de larga evolución a menudo temen perder la vista. La retinopatía diabética es una complicación ocular común en la que los frágiles vasos sanguíneos y las células nerviosas de la retina se dañan de forma progresiva por la glucosa elevada. Las inyecciones medicamentosas actuales pueden ralentizar la enfermedad, pero no restauran por completo los delicados tejidos del ojo. Este estudio explora un enfoque regenerativo: el uso de células madre procedentes de sangre de cordón umbilical, y muestra cómo un fármaco oncológico llamado everolimus puede mejorar la supervivencia de estas células en un entorno empapado de azúcar, como el ojo diabético.
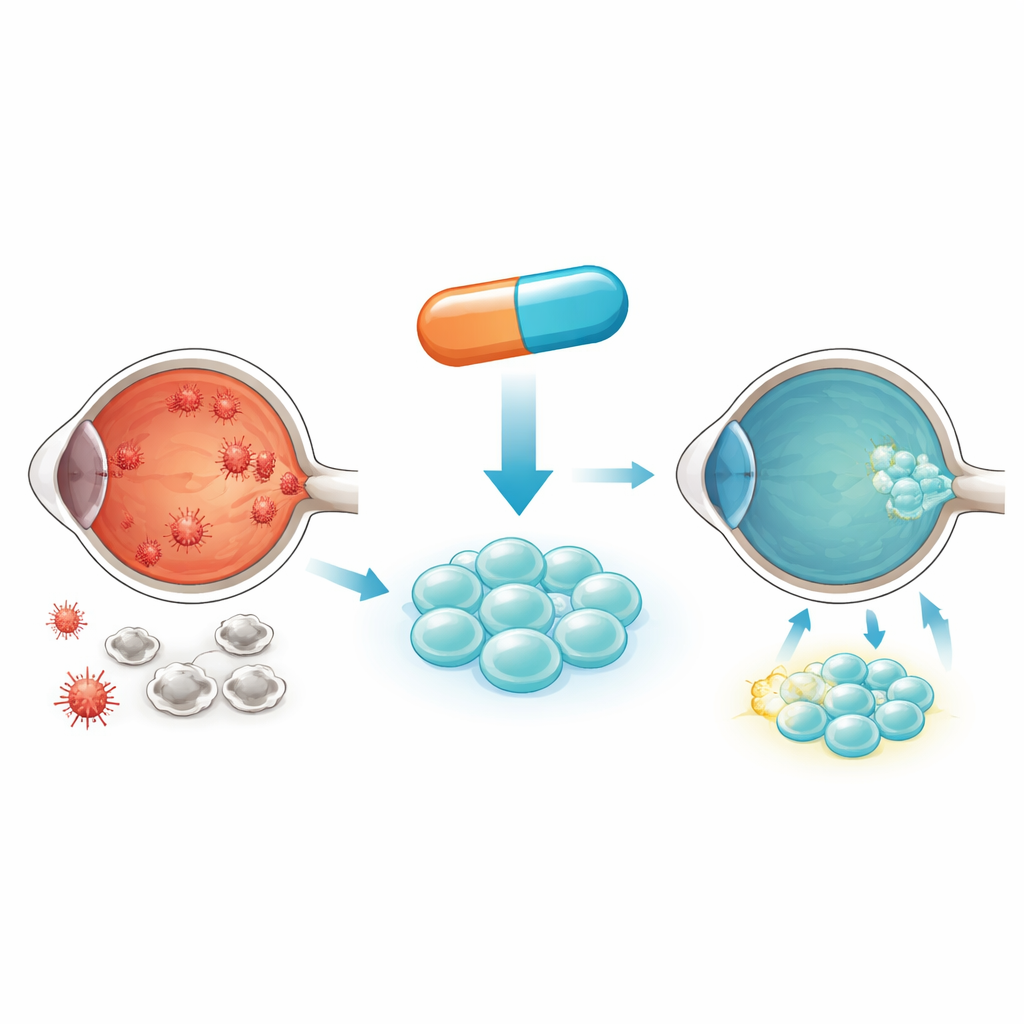
Cómo la diabetes daña el ojo y a las células madre trasplantadas
En la diabetes, el exceso de azúcar baña constantemente a las células. En su interior, este azúcar se quema en pequeñas centrales llamadas mitocondrias, que pueden liberar especies reactivas de oxígeno dañinas cuando se sobrecargan. Con el tiempo, este estrés oxidativo empuja a las células hacia un envejecimiento prematuro y la muerte. Los autores se centran en las células madre mesenquimales derivadas de sangre de cordón umbilical, que pueden apoyar y reparar el tejido retiniano dañado. Desafortunadamente, cuando estas células se colocan en condiciones de alta glucosa similares a la sangre diabética, captan demasiado glucógeno, generan un estrés mitocondrial excesivo y empiezan a morir. Eso significa que quedan menos células sanas para ayudar a rescatar la retina.
La puerta del azúcar que causa más daño
Las células usan pasadizos especializados en sus membranas, conocidos como transportadores de glucosa, para dejar entrar el azúcar. El equipo examinó dos tipos principales presentes en estas células madre: GLUT1 y GLUT3. Cuando los investigadores expusieron las células a altas concentraciones de azúcar durante muchas horas, ambos transportadores aumentaron y la captación de glucosa se elevó. Pero al silenciar selectivamente cada pasadizo con herramientas genéticas, descubrieron que GLUT3 desempeñaba el papel principal en impulsar el estrés mitocondrial. Bloquear GLUT3 redujo drásticamente la acumulación de especies reactivas de oxígeno, estabilizó la función mitocondrial y disminuyó la captación total de azúcar. Cuando estas células madre con GLUT3 silenciado se trasplantaron en ratas con retinopatía diabética, las señales eléctricas retinianas y el grosor de la capa de fotorreceptores mejoraron más que con células madre sin modificar.
Un fármaco contra el cáncer reconvertido para proteger células madre
Los científicos se preguntaron entonces si una molécula pequeña podría imitar los beneficios del control de GLUT3. Se fijaron en everolimus, que bloquea un centro clave de crecimiento y metabolismo celular llamado mTOR. En condiciones de alta glucosa, la señalización mTOR se activó de forma marcada en las células madre. Everolimus atenuó esta señal, redujo la entrada de glucosa y disminuyó el estrés oxidativo mitocondrial con mayor eficacia que el fármaco anterior rapamicina. En dosis bajas nanomolares, everolimus preservó el potencial de membrana mitocondrial, normalizó las defensas antioxidantes de la célula y redujo marcadores de muerte celular programada. En ratas con retinopatía diabética, inyecciones subconjuntivales de células tratadas previamente con everolimus condujeron a una recuperación más sólida de las respuestas eléctricas retinianas y a una mejor preservación de la estructura retiniana que las células no tratadas.
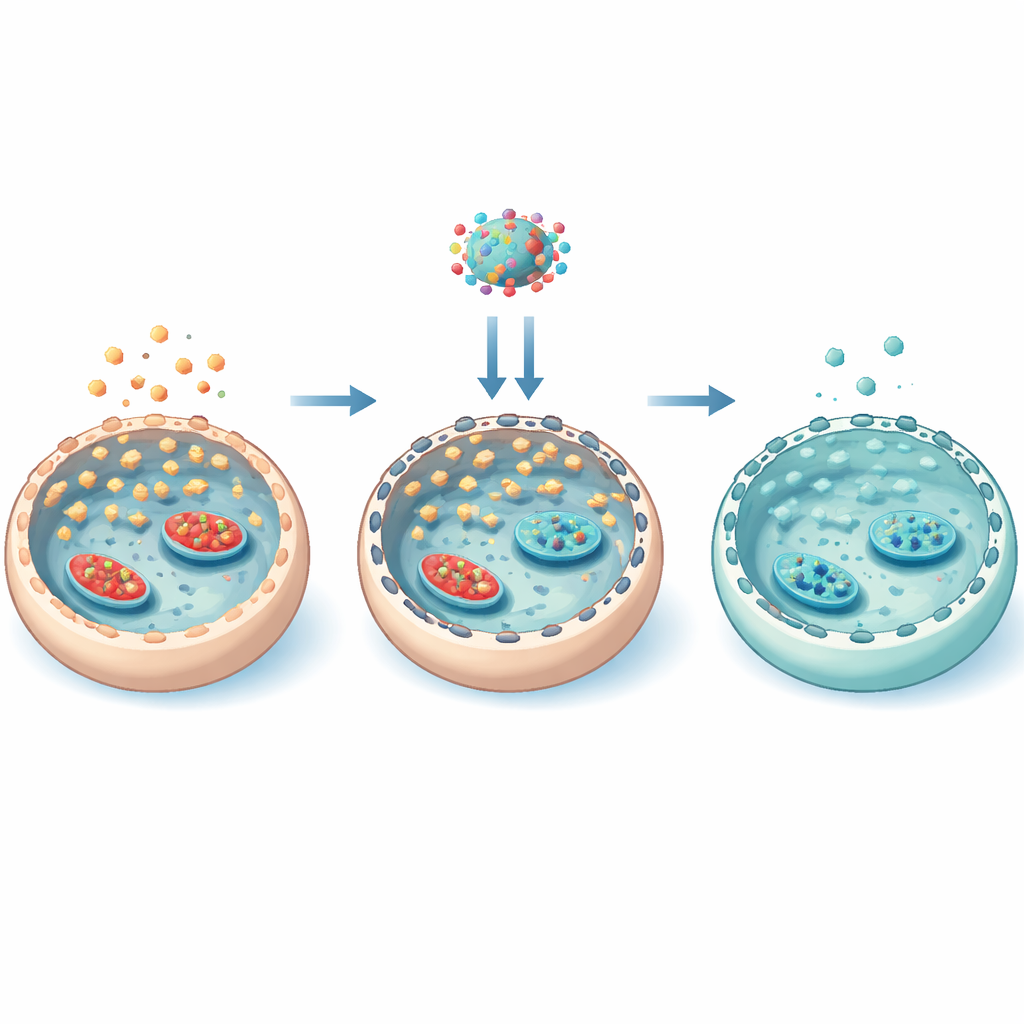
Un andamiaje oculto que controla la entrada de azúcar
Para entender cómo funcionaba tan específicamente everolimus, el equipo observó de cerca el andamiaje interno de la célula compuesto por filamentos de actina. Bajo alta glucosa, la actividad de mTOR aumentó la fosforilación de una proteína llamada cofilina, que inmoviliza la actina en filamentos más estables. Este andamiaje estabilizado facilitó el transporte de los pasadizos GLUT3 hasta la superficie celular, aumentando la entrada de azúcar. Everolimus invirtió esta cadena: redujo la actividad de mTOR, bajó la fosforilación de la cofilina, aflojó la red de actina y retiró GLUT3 de la membrana. Experimentos que estabilizaron o deshicieron la actina confirmaron que esta reorganización física del andamiaje era esencial para controlar la localización de GLUT3. Es importante destacar que everolimus no reprogramó de forma amplia todas las enzimas del procesamiento de la glucosa; en cambio, gobernó principalmente cuánto azúcar podía entrar mediante la posición de los transportadores.
Qué significan estos hallazgos para tratamientos oculares futuros
Para un lector no especializado, la conclusión es que el estudio muestra cómo el preacondicionamiento de las células madre puede ayudarles a sobrevivir en el entorno hostil y azucarado del ojo diabético. Al usar everolimus antes del trasplante, los investigadores pudieron cerrar algunas de las “puertas” de glucosa en las células, calmar sus mitocondrias sobrecargadas y prevenir la muerte celular temprana. En modelos animales, estas células madre más resistentes hicieron un mejor trabajo protegiendo y reconstruyendo el tejido retiniano y mejorando la función retiniana. Aunque se necesita más trabajo antes de probar este enfoque en pacientes, los resultados apuntan a una estrategia práctica: ajustar la entrada de azúcar y las respuestas al estrés de las células antes de su administración, para que estén preparadas para reparar la retina diabética en lugar de verse abrumadas por ella.
Cita: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
Palabras clave: retinopatía diabética, células madre mesenquimales, everolimus, estrés oxidativo, transportadores de glucosa