Clear Sky Science · de
Everolimus unterdrückt die Membran‑Trafficking von Glukosetransporter 3, um die therapeutische Wirksamkeit der Transplantation von Nabelschnurblut‑abgeleiteten mesenchymalen Stammzellen bei diabetischer Retinopathie zu verbessern
Warum der Schutz des Sehvermögens bei Diabetes wichtig ist
Menschen mit langjährigem Diabetes fürchten oft, ihr Sehvermögen zu verlieren. Die diabetische Retinopathie ist eine häufige Augenkomplikation, bei der fragile Blutgefäße und Nervenzellen in der Netzhaut durch chronisch erhöhte Blutzuckerwerte langsam geschädigt werden. Aktuelle Medikamenteninjektionen können das Fortschreiten verlangsamen, stellen das feine Gewebe des Auges jedoch nicht vollständig wieder her. Diese Studie untersucht einen regenerativen Ansatz: die Verwendung von Stammzellen aus dem Nabelschnurblut, und zeigt, wie ein Krebsmedikament namens Everolimus diesen Zellen helfen kann, in einer zuckerübersättigten Umgebung wie dem diabetischen Auge besser zu überleben.
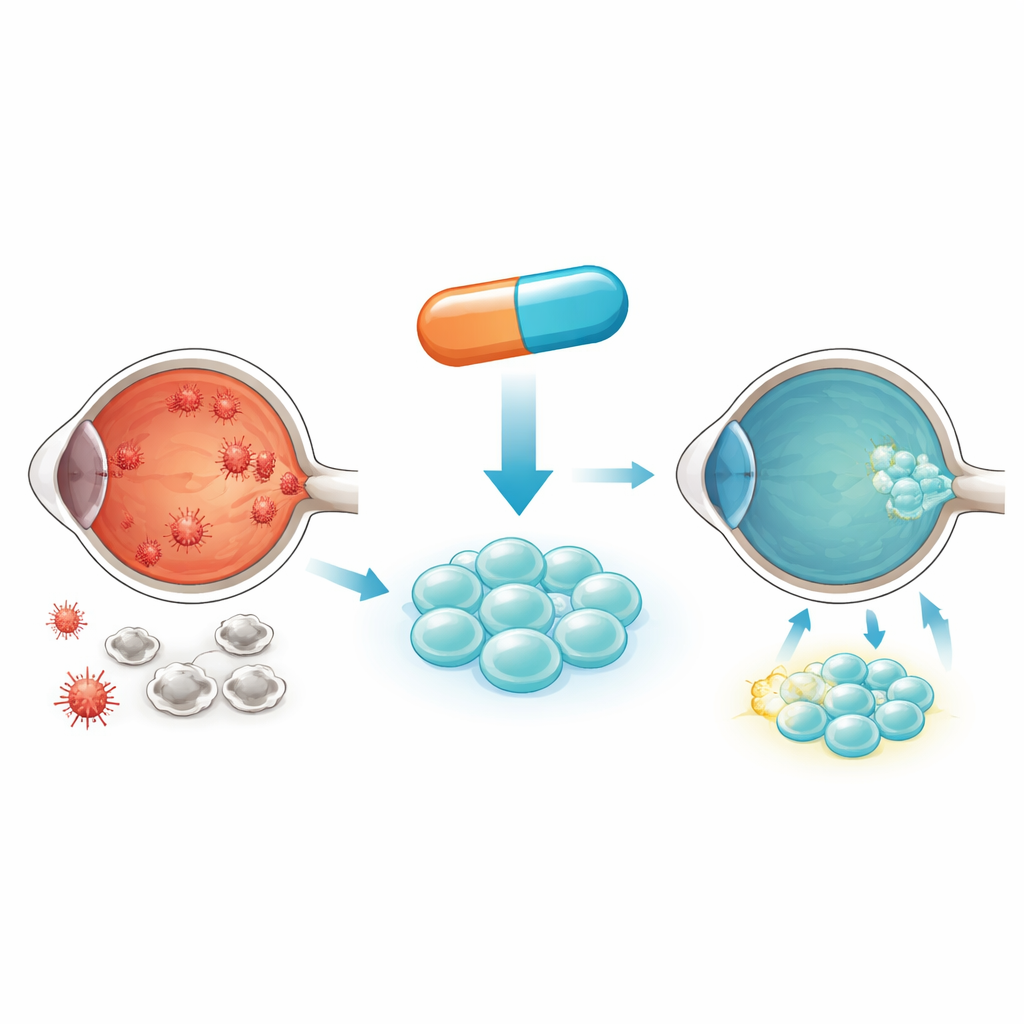
Wie Diabetes das Auge und eingesetzte Stammzellen schädigt
Bei Diabetes sind Zellen ständig einer Überschuss an Zucker ausgesetzt. Innerhalb der Zellen wird dieser Zucker in kleinen Kraftwerken, den Mitochondrien, verbrannt, die bei Überlastung schädliche reaktive Sauerstoffspezies freisetzen können. Mit der Zeit führt dieser oxidative Stress die Zellen in Richtung vorzeitiger Alterung und Zelltod. Die Autoren konzentrieren sich auf mesenchymale Stammzellen aus Nabelschnurblut, die beschädigtes Netzhautgewebe unterstützen und reparieren können. Leider nehmen diese Stammzellen in hochzuckerhaltigen Bedingungen, die dem diabetischen Blut ähneln, zu viel Glukose auf, erzeugen übermäßigen mitochondrialen Stress und beginnen abzusterben. Das bedeutet, dass weniger gesunde Zellen übrigbleiben, um die Netzhaut zu retten.
Die Zuckertür, die den größten Schaden anrichtet
Zellen nutzen spezialisierte „Türen“ in ihren Membranen, sogenannte Glukosetransporter, um Zucker hereinzulassen. Das Team untersuchte zwei Haupttypen, die auf diesen Stammzellen vorkommen: GLUT1 und GLUT3. Als die Forscher die Zellen über viele Stunden hohen Zuckerkonzentrationen aussetzten, stiegen beide Transporter und die Glukoseaufnahme an. Durch selektives Stilllegen jeder Tür mit genetischen Werkzeugen entdeckten sie jedoch, dass GLUT3 die Hauptrolle beim Auslösen des mitochondrialen Stresses spielte. Das Blockieren von GLUT3 reduzierte die Ansammlung schädlicher Sauerstoffspezies deutlich, stabilisierte die Mitochondrienfunktion und verringerte die gesamte Zuckeraufnahme. Wenn diese GLUT3‑stillgelegten Stammzellen in Ratten mit diabetischer Retinopathie transplantiert wurden, verbesserten sich die elektrischen Netzhautsignale und die Dicke der Photorezeptorschicht stärker als bei unveränderten Stammzellen.
Ein umfunktioniertes Krebsmedikament zum Schutz der Stammzellen
Die Wissenschaftler fragten sich dann, ob ein kleines Molekül denselben Nutzen wie die Kontrolle von GLUT3 nachahmen könnte. Sie setzten Everolimus ein, das einen zentralen Wachstums‑ und Stoffwechselknotenpunkt in Zellen namens mTOR blockiert. Unter Hochzuckerbedingungen war die mTOR‑Signalgebung in den Stammzellen stark aktiviert. Everolimus dämpfte dieses Signal, verringerte die Glukoseaufnahme und reduzierte den mitochondrialen oxidativen Stress wirksamer als das ältere Medikament Rapamycin. In niedrigen Nanomol‑Dosen erhielt Everolimus das membranielle Mitochondrienpotenzial, normalisierte die antioxidativen Abwehrmechanismen der Zelle und senkte Marker des programmierten Zelltods. Bei Ratten mit diabetischer Retinopathie führten subkonjunktivale Injektionen von Everolimus‑vorgestreiften Stammzellen zu einer stärkeren Wiederherstellung der elektrischen Netzhautreaktionen und einer besseren Erhaltung der Netzhautstruktur als unbehandelte Stammzellen.
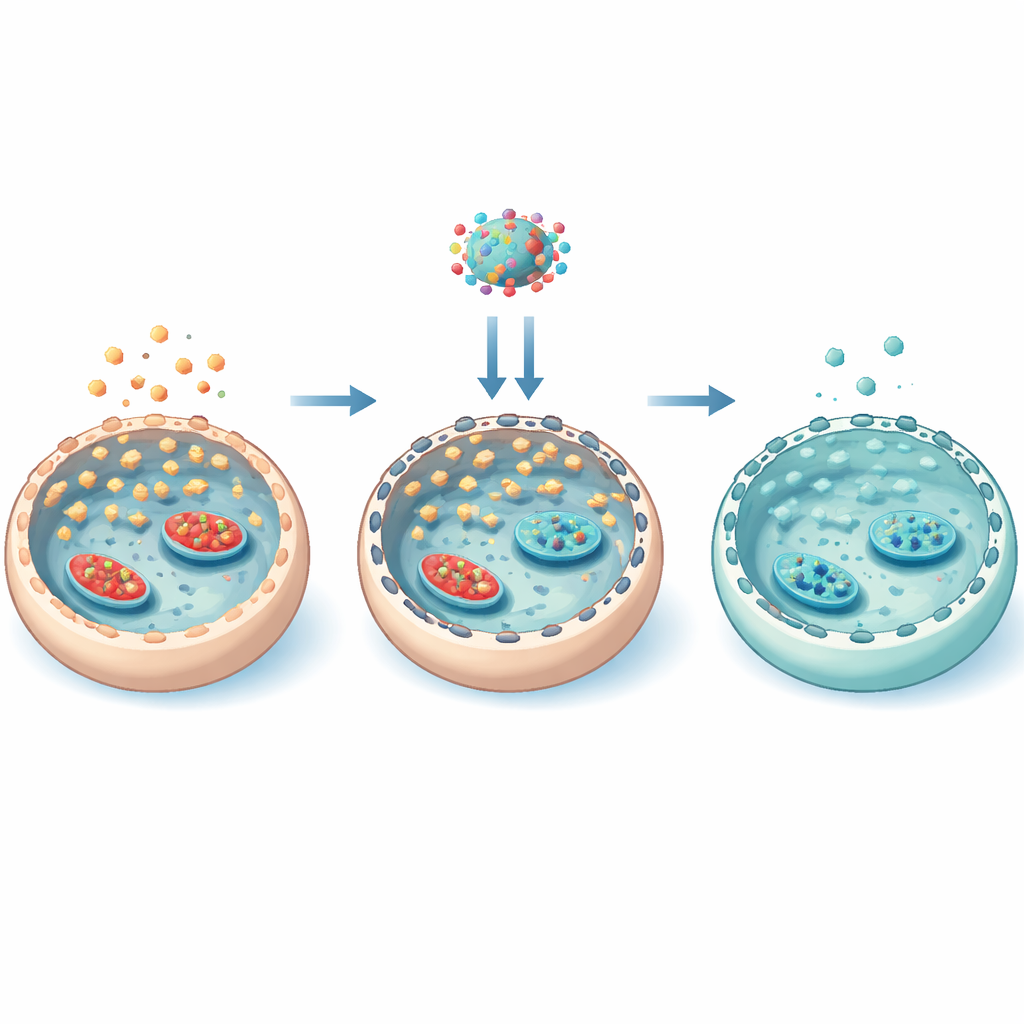
Ein verborgenes Gerüst, das den Zuckereintritt steuert
Um zu verstehen, wie Everolimus so gezielt wirkte, zoomte das Team in das interne Gerüst der Zelle aus Aktinfilamenten hinein. Unter Hochzucker erhöhte mTOR die Phosphorylierung eines Proteins namens Cofilin, das Aktin in stabilere Filamente einsperrt. Dieses stabilisierte Gerüst förderte die Verlagerung der GLUT3‑„Türen“ an die Zelloberfläche und steigerte so den Zuckereintritt. Everolimus kehrte diese Kette um: Es verringerte die mTOR‑Aktivität, senkte die Cofilin‑Phosphorylierung, lockerte das Aktinnetzwerk und zog GLUT3 von der Membran zurück. Experimente, die entweder Aktin stabilisierten oder störten, bestätigten, dass diese physikalische Umordnung des Gerüsts für die Kontrolle der GLUT3‑Lokalisation entscheidend war. Wichtig ist, dass Everolimus nicht umfassend alle Glukose‑verarbeitenden Enzyme umprogrammierte; vielmehr regulierte es hauptsächlich, wie viel Zucker durch die Positionierung der Transporter hereinkommen konnte.
Was diese Ergebnisse für künftige Augenbehandlungen bedeuten
Für Laien lässt sich zusammenfassen: Die Studie zeigt, wie eine Vorbehandlung von Stammzellen deren Überleben in der rauen, zuckerreichen Umgebung des diabetischen Auges verbessern kann. Durch den Einsatz von Everolimus vor der Transplantation gelang es den Forschern, einige der Zucker‑„Türen“ auf den Zellen zu schließen, ihre überlasteten Mitochondrien zu beruhigen und vorzeitigen Zelltod zu verhindern. In Tiermodellen schützten diese robusteren Stammzellen die Netzhaut besser, halfen beim Wiederaufbau des Gewebes und verbesserten die Netzhautfunktion. Obwohl weitere Forschung nötig ist, bevor dieses Vorgehen am Menschen erprobt werden kann, deutet die Arbeit auf eine praktische Strategie hin: Vor der Verabreichung die Zuckeraufnahme und Stressantworten der Zellen zu modulieren, damit sie bereit sind, die diabetische Netzhaut zu reparieren, anstatt von ihr überwältigt zu werden.
Zitation: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
Schlüsselwörter: diabetische Retinopathie, mesenchymale Stammzellen, Everolimus, oxidativer Stress, Glukosetransporter