Clear Sky Science · fr
L’évérolimus supprime le trafic membranaire du transporteur de glucose 3 pour améliorer l’efficacité thérapeutique de la transplantation de cellules souches mésenchymateuses dérivées du sang de cordon ombilical dans la rétinopathie diabétique
Pourquoi la protection de la vision en cas de diabète compte
Les personnes atteintes de diabète de longue date craignent souvent de perdre la vue. La rétinopathie diabétique est une complication oculaire fréquente dans laquelle des vaisseaux sanguins fragiles et des cellules nerveuses de la rétine sont lentement endommagés par l’hyperglycémie. Les injections médicamenteuses actuelles peuvent ralentir la maladie mais ne restaurent pas complètement les tissus délicats de l’œil. Cette étude explore une approche régénérative : l’utilisation de cellules souches issues du sang de cordon ombilical, et montre comment un médicament anticancéreux appelé évérolimus peut améliorer la survie de ces cellules dans un environnement saturé de sucre comme l’œil diabétique.
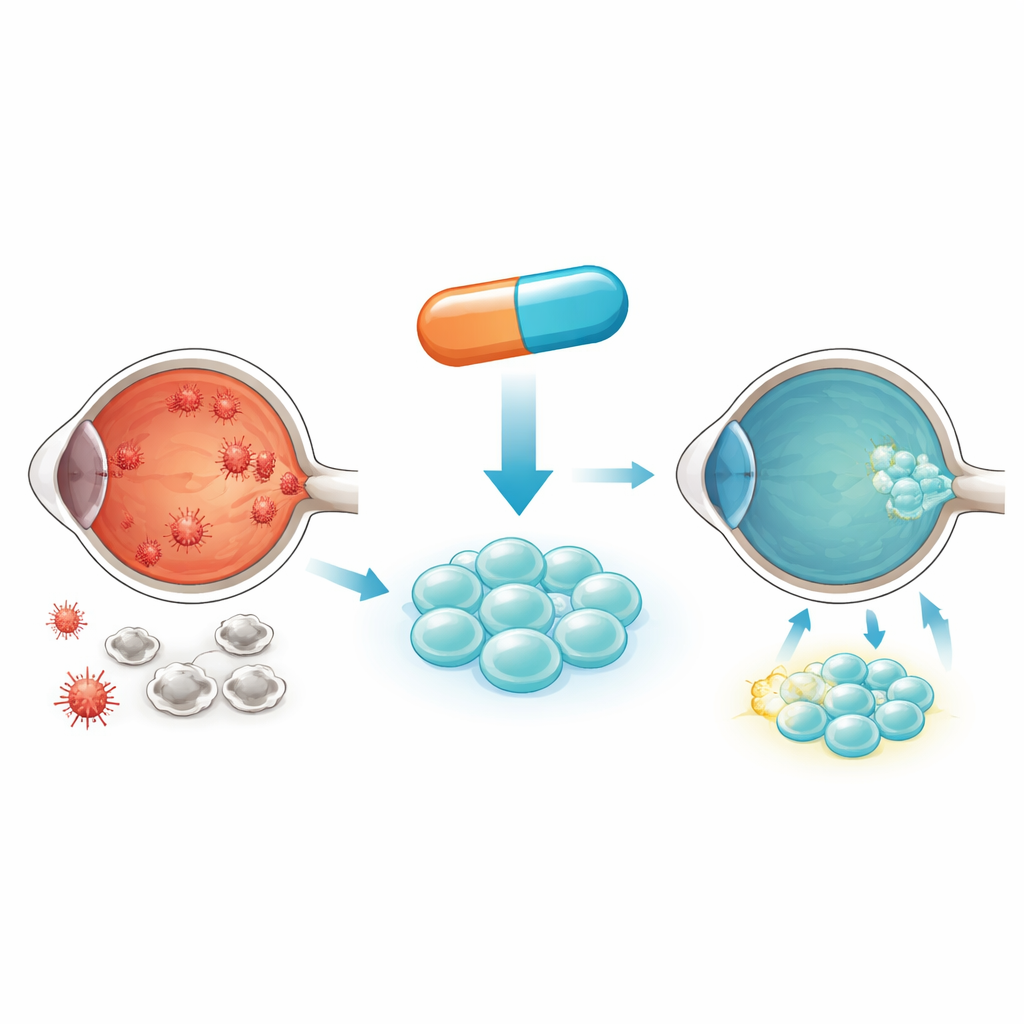
Comment le diabète endommage l’œil et les cellules souches transplantées
Dans le diabète, l’excès de glucose baigne en permanence les cellules. À l’intérieur, ce sucre est brûlé dans de petites centrales appelées mitochondries, qui peuvent libérer des espèces réactives de l’oxygène lorsqu’elles sont surchargées. Avec le temps, ce stress oxydatif pousse les cellules vers un vieillissement prématuré et la mort. Les auteurs se concentrent sur les cellules souches mésenchymateuses dérivées du sang de cordon ombilical, capables de soutenir et de réparer le tissu rétinien endommagé. Malheureusement, lorsque ces cellules sont placées dans des conditions hyperglycémiques similaires au sang diabétique, elles absorbent trop de glucose, génèrent un stress mitochondrial excessif et commencent à mourir. Il reste alors moins de cellules saines pour contribuer à la réparation de la rétine.
La porte d’entrée du sucre qui fait le plus de dégâts
Les cellules utilisent des portes spécialisées dans leur membrane, connues sous le nom de transporteurs de glucose, pour laisser entrer le sucre. L’équipe a examiné deux types principaux présents sur ces cellules souches : GLUT1 et GLUT3. Lorsque les chercheurs ont exposé les cellules à une forte concentration de glucose pendant de longues heures, les deux transporteurs ont augmenté et l’absorption de glucose a augmenté. Mais en silencant sélectivement chaque porte par des outils génétiques, ils ont découvert que GLUT3 jouait le rôle principal dans l’induction du stress mitochondrial. Bloquer GLUT3 a fortement réduit l’accumulation d’espèces réactives de l’oxygène, stabilisé la fonction mitochondriale et diminué l’absorption globale de sucre. Lorsque ces cellules souches avec GLUT3 diminué ont été transplantées chez des rats atteints de rétinopathie diabétique, les signaux électriques rétiniens et l’épaisseur de la couche des photorécepteurs se sont améliorés davantage que lors de l’utilisation de cellules souches non modifiées.
Un médicament anticancéreux réutilisé pour protéger les cellules souches
Les scientifiques se sont ensuite demandé si une petite molécule pouvait reproduire les bénéfices du contrôle de GLUT3. Ils se sont tournés vers l’évérrolimus, qui bloque un nœud clé de croissance et de métabolisme cellulaire appelé mTOR. En conditions hyperglycémiques, la signalisation mTOR était fortement activée dans les cellules souches. L’évérrolimus a atténué ce signal, réduit l’entrée de glucose et limité le stress mitochondrial oxydatif plus efficacement que l’ancien médicament rapamycine. À de faibles doses nanomolaires, l’évérrolimus a préservé le potentiel de membrane mitochondrial, normalisé les défenses antioxydantes de la cellule et diminué les marqueurs d’apoptose. Chez des rats atteints de rétinopathie diabétique, des injections subconjonctivales de cellules souches prétraitées par évérolimus ont conduit à une meilleure récupération des réponses électriques rétiniennes et à une meilleure préservation de la structure rétinienne que les cellules non traitées.
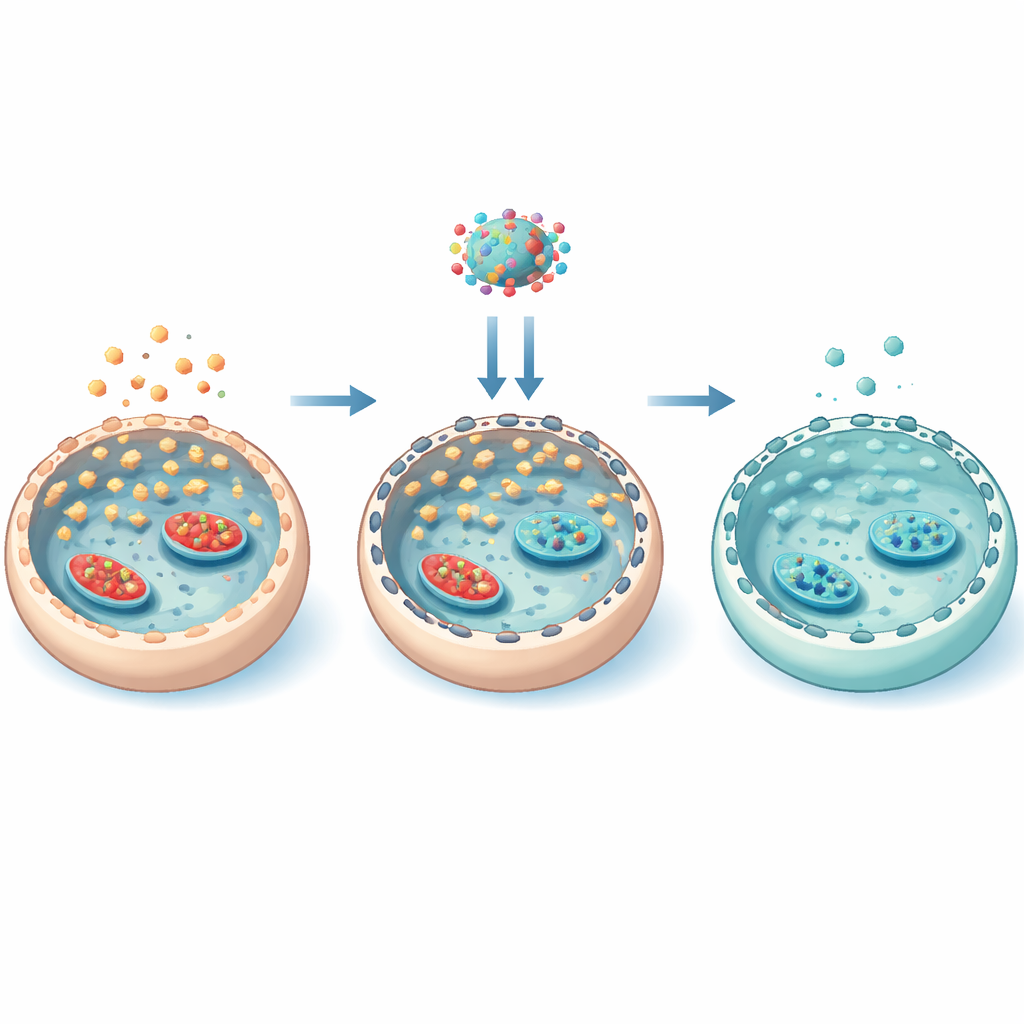
Un échafaudage caché qui contrôle l’entrée du sucre
Pour comprendre comment l’évérrolimus agissait de façon si spécifique, l’équipe s’est penchée sur le cytosquelette interne de la cellule composé de filaments d’actine. Sous forte glycémie, l’activité de mTOR augmentait la phosphorylation d’une protéine appelée cofiline, qui verrouille l’actine dans des filaments plus stables. Cet échafaudage stabilisé favorisait le déplacement des portes GLUT3 à la surface cellulaire, augmentant l’entrée de sucre. L’évérrolimus a inversé cette chaîne : il a réduit l’activité mTOR, abaissé la phosphorylation de la cofiline, desserré le réseau d’actine et retiré GLUT3 de la membrane. Des expériences stabilisant ou perturbant l’actine ont confirmé que cette réorganisation physique de l’échafaudage était essentielle pour contrôler la localisation de GLUT3. Il est important de noter que l’évérrolimus n’a pas réorganisé de manière générale toutes les enzymes du métabolisme du glucose ; il a surtout régulé la quantité de sucre pouvant entrer via le positionnement des transporteurs.
Ce que signifient ces résultats pour les traitements oculaires à venir
Pour un lecteur non spécialiste, l’essentiel est que l’étude montre comment le préconditionnement des cellules souches peut les aider à survivre dans l’environnement dur et sucré de l’œil diabétique. En utilisant l’évérrolimus avant la transplantation, les chercheurs ont pu fermer certaines « portes » à sucre des cellules, calmer leurs mitochondries surmenées et prévenir la mort cellulaire précoce. Dans des modèles animaux, ces cellules souches renforcées ont mieux protégé et reconstruit le tissu rétinien et amélioré la fonction rétinienne. Bien qu’il faille davantage de travaux avant d’essayer cette approche chez l’humain, ces résultats pointent vers une stratégie pratique : régler l’apport en sucre et les réponses au stress des cellules avant leur administration, afin qu’elles soient prêtes à réparer la rétine diabétique plutôt que d’en être submergées.
Citation: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
Mots-clés: rétinopathie diabétique, cellules souches mésenchymateuses, évérolimus, stress oxydatif, transporteurs de glucose