Clear Sky Science · pt
Everolimus suprime o tráfego membranar do transportador de glicose 3 para melhorar a eficácia terapêutica do transplante de células-tronco mesenquimais derivadas do sangue do cordão umbilical na retinopatia diabética
Por que proteger a visão no diabetes é importante
Pessoas com diabetes de longa data frequentemente temem perder a visão. A retinopatia diabética é uma complicação ocular comum em que vasos sanguíneos frágeis e células nervosas da retina são gradualmente danificados pela hiperglicemia. Injeções medicamentosas disponíveis atualmente podem retardar a progressão da doença, mas não restauram totalmente o tecido delicado do olho. Este estudo explora uma abordagem regenerativa: o uso de células-tronco do sangue do cordão umbilical, e mostra como um fármaco usado contra o câncer chamado everolimus pode melhorar a sobrevivência dessas células em um ambiente saturado de glicose, como o olho diabético.
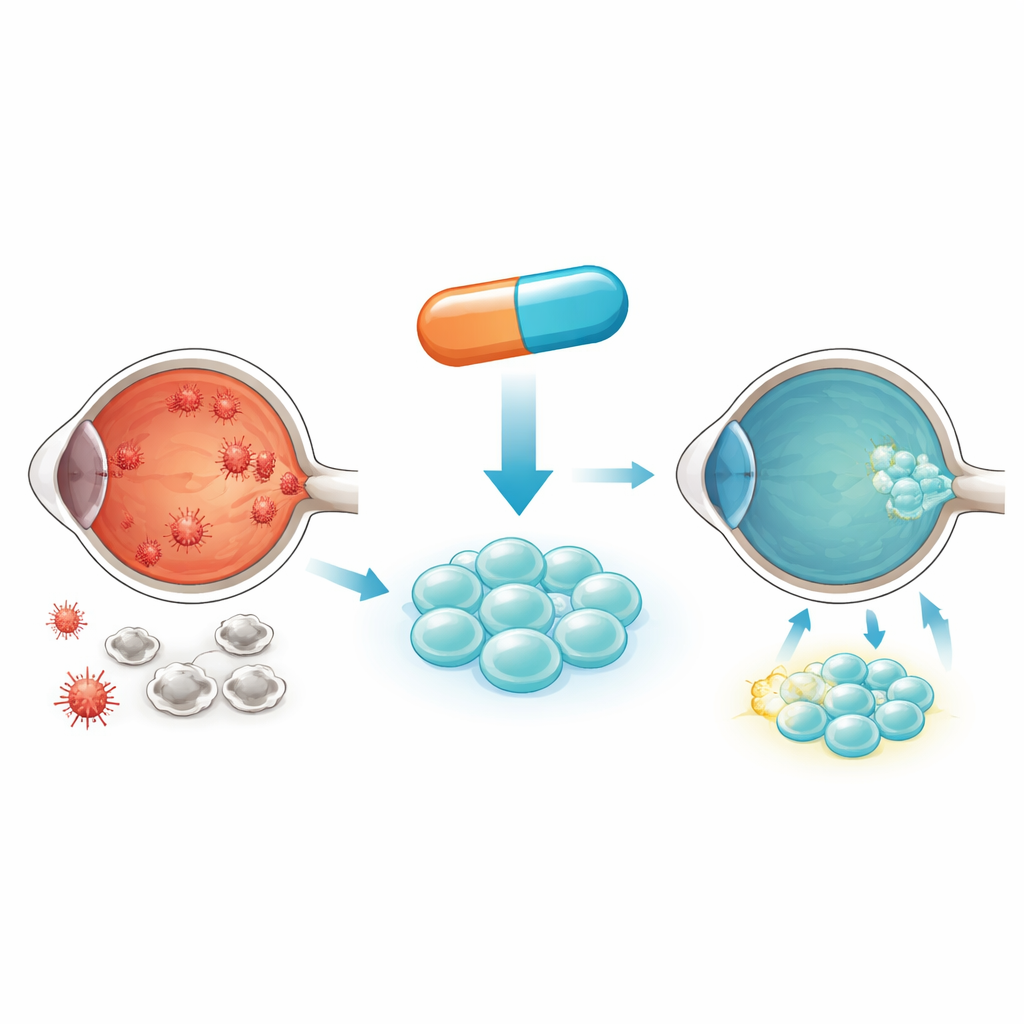
Como o diabetes danifica o olho e as células-tronco transplantadas
No diabetes, o excesso de açúcar banha as células de forma contínua. No interior, essa glicose é queimada em pequenas usinas chamadas mitocôndrias, que podem liberar espécies reativas de oxigênio nocivas quando sobrecarregadas. Com o tempo, esse estresse oxidativo empurra as células para um envelhecimento prematuro e morte. Os autores focam nas células-tronco mesenquimais derivadas do sangue do cordão umbilical, que podem apoiar e reparar o tecido retiniano danificado. Infelizmente, quando essas células são colocadas em condições de alta glicose, semelhantes ao sangue diabético, elas absorvem glicose em excesso, geram estresse mitocondrial excessivo e começam a morrer. Isso significa que menos células saudáveis permanecem para ajudar a resgatar a retina.
A porta da glicose que causa mais dano
As células usam “portas” especializadas em suas membranas, conhecidas como transportadores de glicose, para deixar a glicose entrar. A equipe examinou dois tipos principais presentes nessas células-tronco: GLUT1 e GLUT3. Quando os pesquisadores expuseram as células a alta glicose por muitas horas, ambos os transportadores aumentaram, e a captação de glicose cresceu. Mas ao silenciar seletivamente cada porta com ferramentas genéticas, descobriram que o GLUT3 desempenhava o papel central em induzir o estresse mitocondrial. Bloquear o GLUT3 reduziu fortemente o acúmulo de espécies reativas de oxigênio, estabilizou a função mitocondrial e diminuiu a captação geral de glicose. Quando essas células-tronco com GLUT3 silenciado foram transplantadas em ratos com retinopatia diabética, os sinais elétricos retinais e a espessura da camada de fotoreceptores melhoraram mais do que com células-tronco não modificadas.
Um fármaco contra o câncer reaproveitado para proteger células-tronco
Os cientistas então perguntaram se uma molécula pequena poderia imitar os benefícios do controle do GLUT3. Eles recorreram ao everolimus, que bloqueia um importante centro de crescimento e metabolismo celular chamado mTOR. Em condições de alta glicose, a sinalização mTOR estava fortemente ativada nas células-tronco. O everolimus reduziu esse sinal, diminuiu a entrada de glicose e cortou o estresse oxidativo mitocondrial de maneira mais eficaz que o antigo fármaco rapamicina. Em doses nanomolares baixas, o everolimus preservou o potencial de membrana mitocondrial, normalizou as defesas antioxidantes da célula e reduziu marcadores de morte celular programada. Em ratos com retinopatia diabética, injeções subconjuntivais de células-tronco pré-tratadas com everolimus resultaram em recuperação mais forte das respostas elétricas retinais e melhor preservação da estrutura retiniana do que células-tronco não tratadas.
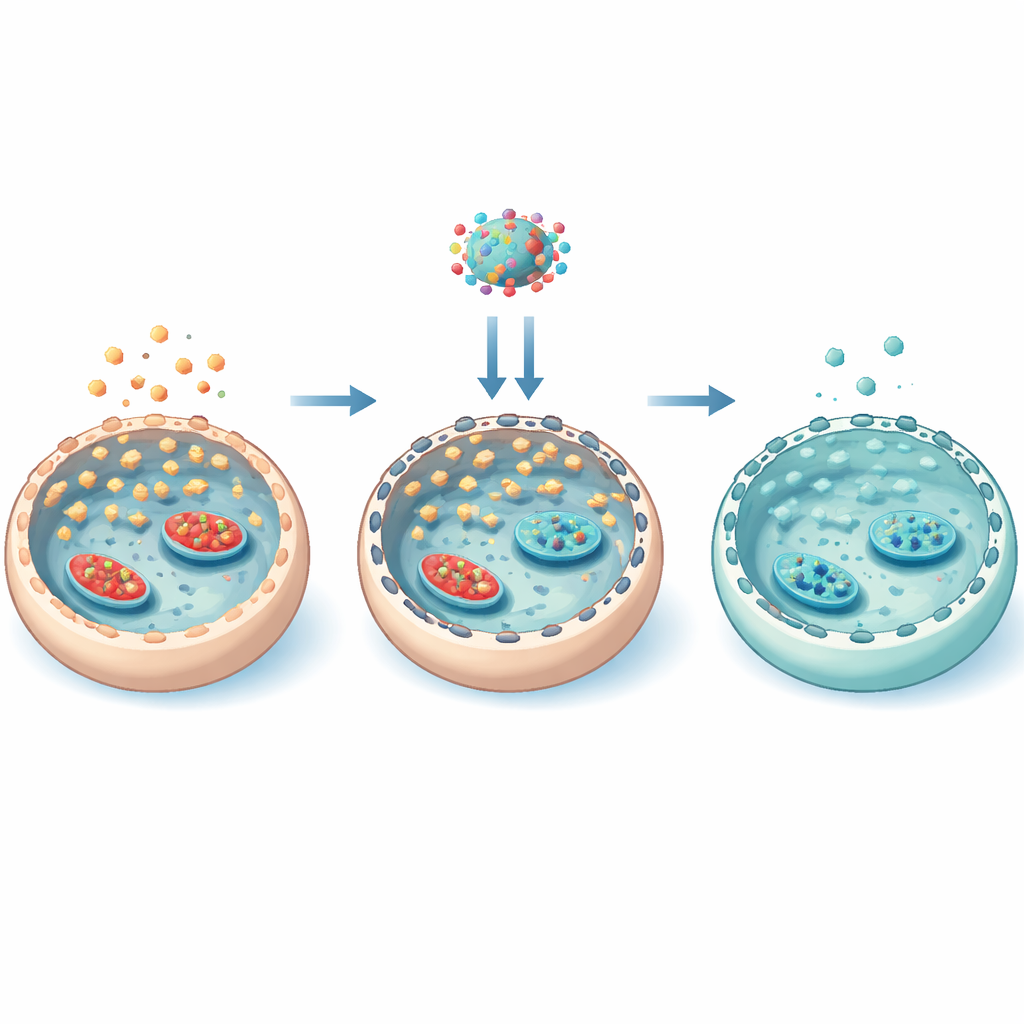
Um andaime oculto que controla a entrada de açúcar
Para entender como o everolimus atuava de forma tão específica, a equipe investigou o andaime interno da célula formado por filamentos de actina. Sob alta glicose, a atividade do mTOR aumentou a fosforilação de uma proteína chamada cofilina, que prende a actina em filamentos mais estáveis. Esse andaime estabilizado ajudou a translocar as “portas” GLUT3 para a superfície celular, aumentando a entrada de açúcar. O everolimus reverteu essa cadeia: reduziu a atividade do mTOR, diminuiu a fosforilação da cofilina, afrouxou a rede de actina e retiraou o GLUT3 da membrana. Experimentos que estabilizaram ou desorganizaram a actina confirmaram que esse rearranjo físico do andaime era essencial para controlar a localização do GLUT3. Importante: o everolimus não reprogramou amplamente todas as enzimas de processamento de glicose; em vez disso, governou principalmente quanto açúcar podia entrar pela posição dos transportadores.
O que essas descobertas significam para tratamentos oculares futuros
Para um leitor leigo, a conclusão é que o estudo mostra como pré-condicionar células-tronco pode ajudá-las a sobreviver ao ambiente hostil e açucarado do olho diabético. Ao usar everolimus antes do transplante, os pesquisadores conseguiram fechar algumas dessas “portas” de glicose nas células, acalmar suas mitocôndrias sobrecarregadas e prevenir morte celular prematura. Em modelos animais, essas células-tronco mais resistentes fizeram um trabalho melhor em proteger e reconstruir o tecido retiniano e em melhorar a função retinal. Embora mais trabalho seja necessário antes que essa abordagem possa ser testada em pacientes, o estudo aponta para uma estratégia prática: ajustar a entrada de açúcar e as respostas ao estresse das células antes de entregá-las, para que estejam prontas para reparar a retina diabética em vez de serem dominadas por ela.
Citação: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
Palavras-chave: retinopatia diabética, células-tronco mesenquimais, everolimus, estresse oxidativo, transportadores de glicose