Clear Sky Science · ru
Эверолимус подавляет мембранный трафик транспортера глюкозы 3, улучшая терапевтическую эффективность пересадки мезенхимальных стволовых клеток из пуповинной крови при диабетической ретинопатии
Почему важно защищать зрение при диабете
Люди с длительно текущим диабетом часто опасаются потери зрения. Диабетическая ретинопатия — распространенное осложнение глаза, при котором хрупкие кровеносные сосуды и нервные клетки сетчатки постепенно повреждаются высоким уровнем сахара в крови. Существующие лекарственные инъекции могут замедлить прогрессирование болезни, но не восстанавливают тонкие ткани глаза полностью. В этом исследовании рассматривается регенеративный подход: использование стволовых клеток из пуповинной крови, и показано, как противораковый препарат эверолимус может помочь этим клеткам лучше выживать в среде с избытком сахара, типичной для диабетического глаза.
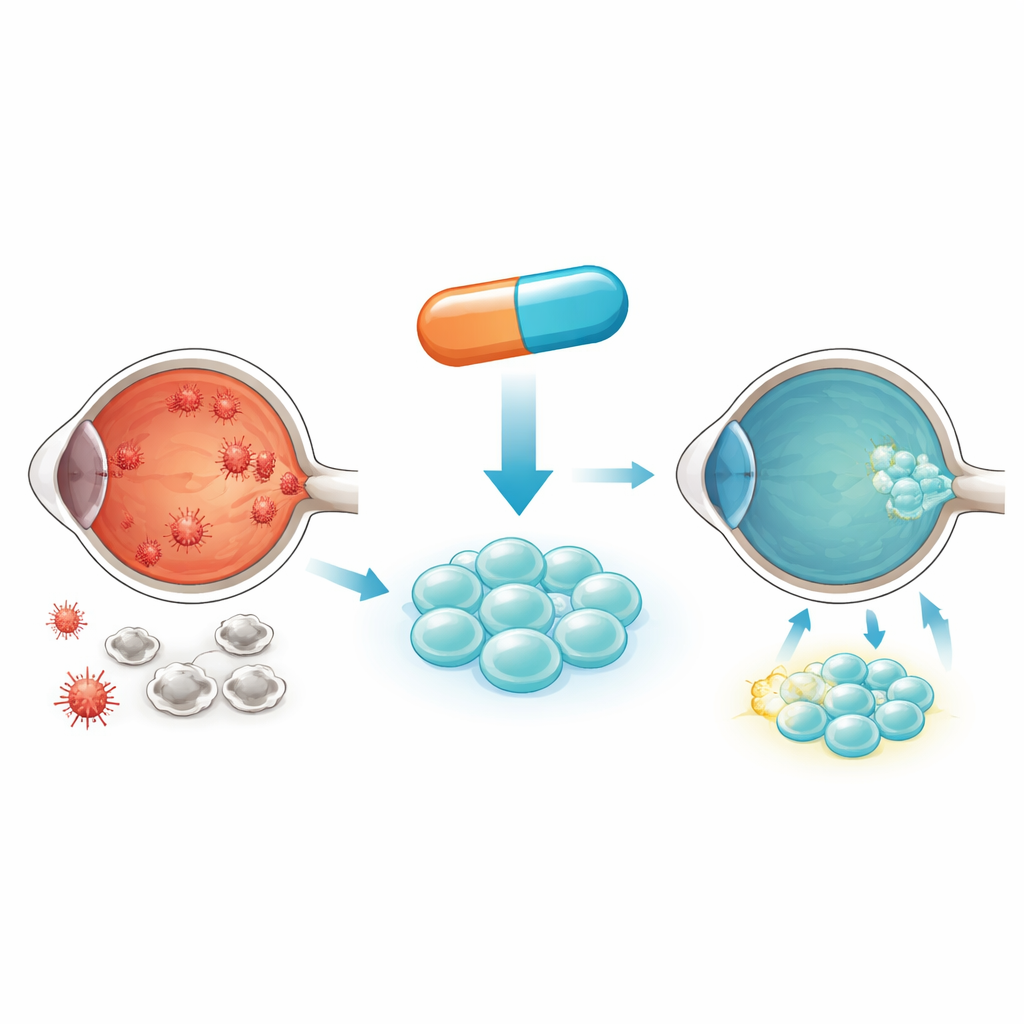
Как диабет вредит глазу и вводимым стволовым клеткам
При диабете клетки постоянно омываются избытком сахара. Внутри он перерабатывается в крошечных электростанциях — митохондриях, которые при перегрузке могут выделять вредные реактивные кислородные формы. Со временем этот оксидативный стресс подтолкнет клетки к преждевременному старению и гибели. Авторы сосредоточились на мезенхимальных стволовых клетках, полученных из пуповинной крови, которые способны поддерживать и восстанавливать поврежденную сетчатку. К сожалению, когда эти клетки помещают в условия с высоким содержанием сахара, аналогичные диабетической крови, они поглощают слишком много глюкозы, испытывают чрезмерный митохондриальный стресс и начинают умирать. В результате остаётся меньше живых клеток, способных помочь восстановить сетчатку.
«Сахарная дверь», наносящая наибольший вред
Клетки используют специализированные «двери» в мембране, известные как транспортеры глюкозы, чтобы пропускать сахар внутрь. Команда изучала два основных типа на этих стволовых клетках: GLUT1 и GLUT3. При экспозиции клеток высокому уровню сахара в течение многих часов оба транспортёра увеличивали свою активность, и поглощение глюкозы возрастало. Но при селективном отключении каждого «проёма» с помощью генетических инструментов выяснилось, что ключевую роль в запуске митохондриального стресса играет GLUT3. Блокировка GLUT3 резко снизила накопление вредных кислородных радикалов, стабилизировала функцию митохондрий и уменьшила общее поглощение сахара. При трансплантации в крысиные модели диабетической ретинопатии стволовые клетки с подавленным GLUT3 улучшали электрические ответы сетчатки и толщину фоторецепторного слоя больше, чем немодифицированные клетки.
Препарат от рака, переназначенный для защиты стволовых клеток
Учёные затем задали вопрос, может ли малое молекулярное соединение имитировать преимущества контроля GLUT3. Они обратились к эверолимусу, который блокирует ключевой узел регуляции роста и метаболизма в клетке — путь mTOR. При высоком уровне сахара mTOR-сигнализация в стволовых клетках была сильно активирована. Эверолимус подавлял этот сигнал, снижал вход глюкозы и уменьшал митохондриальный оксидативный стресс эффективнее, чем старый препарат рапамицин. В низких наномолярных дозах эверолимус сохранял потенциал митохондриальной мембраны, нормализовал антиоксидантную защиту клетки и снижал маркеры запрограммированной гибели. В крысах с диабетической ретинопатией субконъюнктивальные инъекции стволовых клеток, предварительно обработанных эверолимусом, приводили к более сильному восстановлению электрических ответов сетчатки и лучшему сохранению её структуры по сравнению с необработанными клетками.
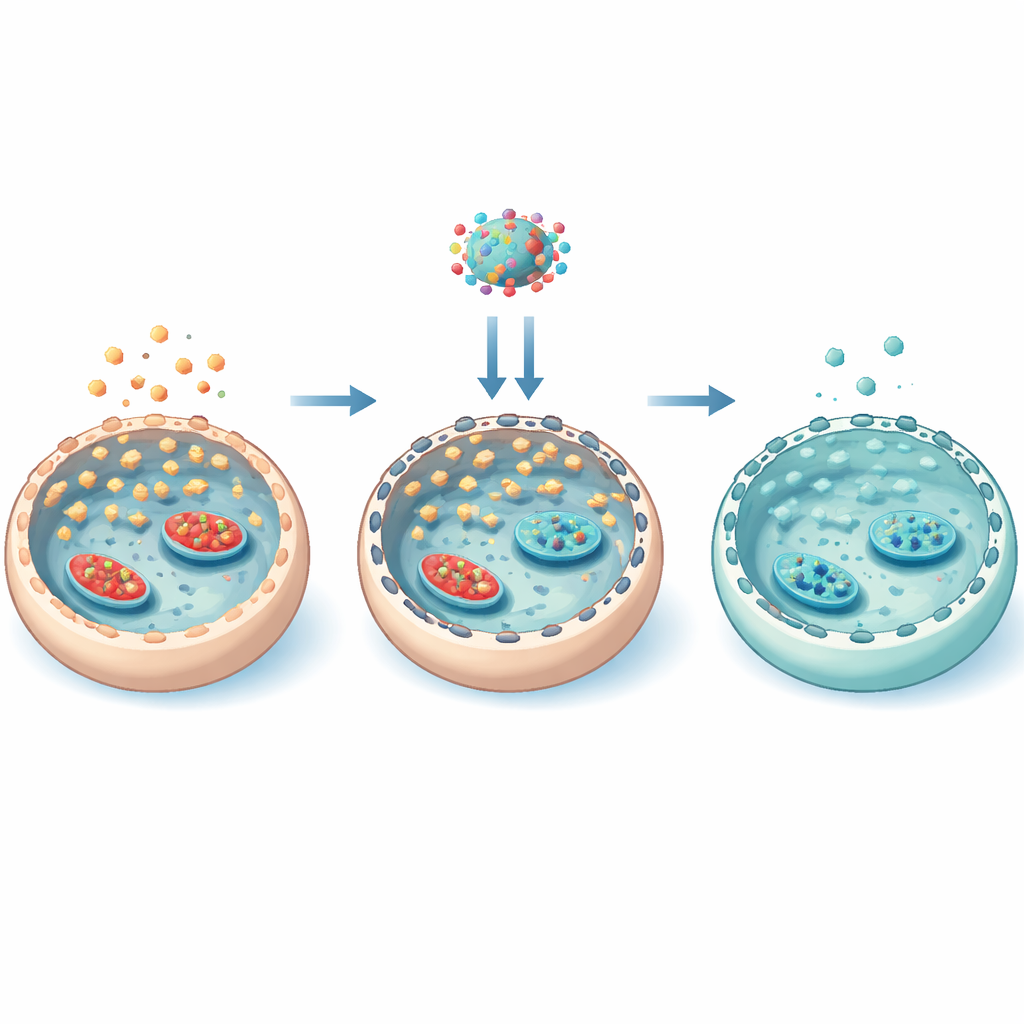
Скрытый каркас, контролирующий поступление сахара
Чтобы понять, как эверолимус действовал так избирательно, команда подробно изучила внутренний каркас клетки — актиновое волокно. При высоком уровне сахара активность mTOR усиливала фосфорилирование белка кофилина, что фиксировало актин в более стабильные филаменты. Этот стабилизированный скелет способствовал перемещению «дверей» GLUT3 к поверхности клетки, увеличивая поступление сахара. Эверолимус разрывал эту цепочку: он снижал активность mTOR, уменьшал фосфорилирование кофилина, ослаблял актиновую сеть и уводил GLUT3 с мембраны. Эксперименты, в которых актин либо стабилизировали, либо разрушали, подтвердили, что именно такое физическое переустройство каркаса было необходимо для контроля локализации GLUT3. Важно, что эверолимус не глобально перенастраивал все ферменты, обрабатывающие глюкозу; он в основном регулировал, сколько сахара может попасть внутрь через позиционирование транспортеров.
Что значат эти результаты для будущих методов лечения глаз
Для неспециалиста основной вывод заключается в том, что исследование показывает: предварительная подготовка стволовых клеток может помочь им пережить суровую, сахаронасыщенную среду диабетического глаза. Используя эверолимус перед трансплантацией, исследователи смогли частично «закрыть» некоторые сахарные «двери» на клетках, успокоить их перегруженные митохондрии и предотвратить преждевременную гибель. В модельных экспериментах такие усиленные клетки лучше защищали и восстанавливали ткани сетчатки и улучшали её функцию. Хотя перед клиническим применением требуется ещё много работы, результаты указывают на практическую стратегию: подстроить поступление сахара и реакции на стресс у клеток до их введения, чтобы они были готовы ремонтировать диабетическую сетчатку, а не оказались подавлены ею.
Цитирование: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
Ключевые слова: диабетическая ретинопатия, мезенхимальные стволовые клетки, эверолимус, окислительный стресс, транспортеры глюкозы