Clear Sky Science · ar
إيفروليموس يُثبّط نقل ناقل الجلوكوز 3 إلى الغشاء لتحسين الفعالية العلاجية لزرع الخلايا الجذعية الميزنكيمية المشتقة من دم الحبل السري في اعتلال الشبكية السكّري
لماذا حماية الرؤية في مرض السكري مهمة
غالبًا ما يقلق الأشخاص المصابون بالسكري لفترة طويلة بشأن فقدان بصرهم. اعتلال الشبكية السكّري هو مضاعفة شائعة للعيون حيث تتلف الأوعية الدموية الضعيفة والخلايا العصبية في الشبكية ببطء نتيجة ارتفاع سكر الدم. يمكن للحقن الدوائية الحالية إبطاء المرض لكنها لا تعيد بالكامل نسيج العين الدقيق. تستقصي هذه الدراسة نهجًا تجديديًا: استخدام خلايا جذعية من دم الحبل السري، وتوضح كيف يمكن لدواء مضاد للسرطان يُدعى إيفروليموس أن يساعد هذه الخلايا على البقاء بشكل أفضل في بيئة مشبعة بالسكر مثل عين مريض السكري.
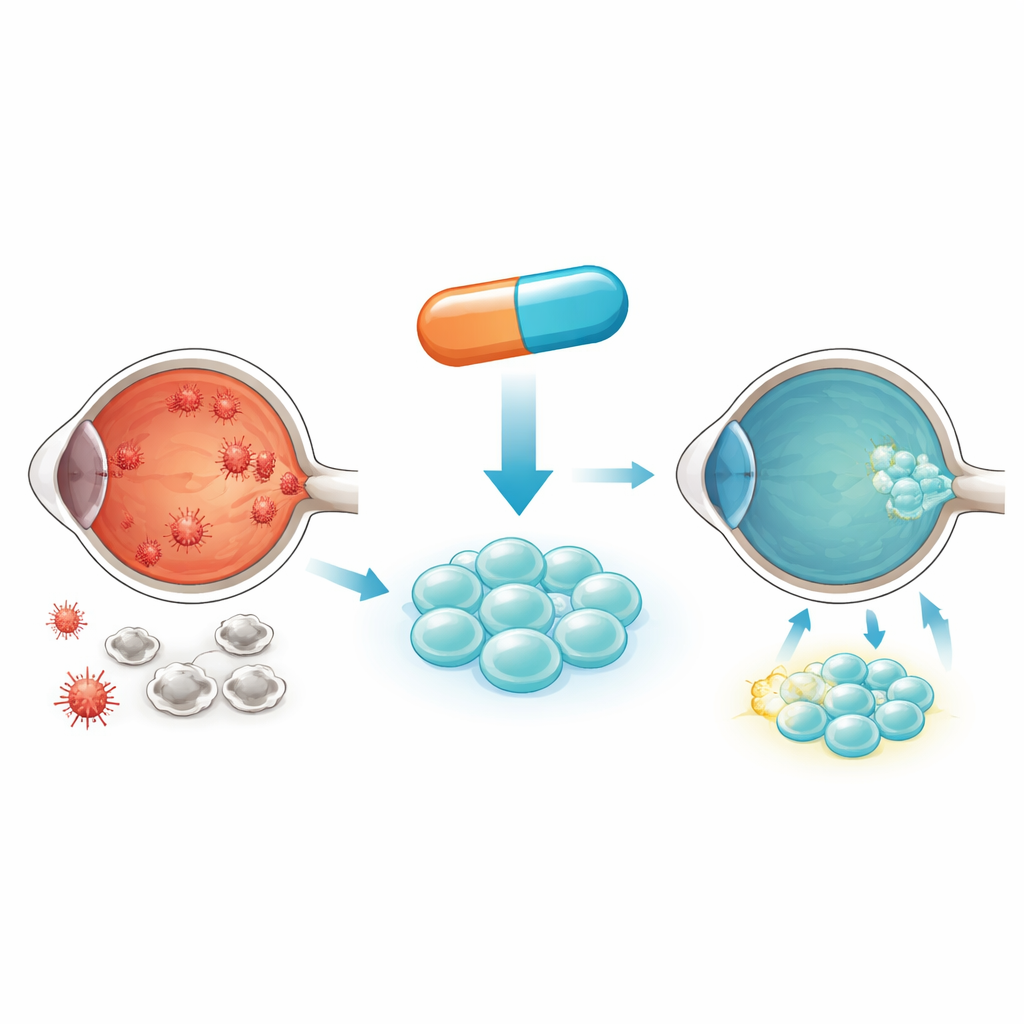
كيف يضُرّ السكري العين والخلايا الجذعية القادمة
في حالات السكري، يغمر السكر الزائد الخلايا باستمرار. داخليًا، يتم حرق هذا السكر في مصانع طاقة صغيرة تُسمى الميتوكوندريا، والتي يمكن أن تطلق أنواعًا تفاعلية من الأكسجين ضارة عند التحميل الزائد. مع الوقت، يدفع هذا الإجهاد التأكسدي الخلايا نحو الشيخوخة والوفاة المبكرة. يركّز المؤلفون على الخلايا الجذعية الميزنكيمية المشتقة من دم الحبل السري، التي يمكنها دعم وإصلاح نسيج الشبكية المتضرر. للأسف، عندما توضع هذه الخلايا في ظروف عالية السكر تشبه دم مرضى السكري، تمتص نسبة كبيرة من الجلوكوز، وتُولد إجهادًا ميتوكوندريًا مفرطًا، وتبدأ بالموت. وهذا يعني بقاء عدد أقل من الخلايا السليمة القادرة على إنقاذ الشبكية.
البوابة السكرية التي تُحدث أكبر ضرر
تستخدم الخلايا ممرات متخصصة في أغشيتها، تُعرف بناقلات الجلوكوز، للسماح بدخول السكر. فحص الفريق نوعين رئيسيين موجودين على هذه الخلايا الجذعية: GLUT1 وGLUT3. عندما عرض الباحثون الخلايا لسكر عالي لعدة ساعات، زاد كلا الناقلين، وارتفعت عملية امتصاص الجلوكوز. لكن من خلال إسكات كل بوابة على حدة بأدوات جينية، اكتشفوا أن GLUT3 لعب الدور الرئيسي في تحفيز الإجهاد الميتوكوندري. أدى حجب GLUT3 إلى خفض حاد في تراكم الأنواع المؤكسدة الضارة، واستقرار وظيفة الميتوكوندريا، وخفض إجمالي امتصاص السكر. عندما زُرعت هذه الخلايا المسكوتة عن GLUT3 في جرذان مصابة باعتلال الشبكية السكّري، تحسّنت الإشارات الكهربائية للشبكية وسمك طبقة الخلايا الضوئية أكثر من الخلايا الجذعية غير المعدلة.
دواء مضاد للسرطان مُعاد توظيفه لحماية الخلايا الجذعية
بعد ذلك تساءل العلماء عما إذا كان مركب صغير يمكنه محاكاة فوائد تحكم GLUT3. لجأوا إلى إيفروليموس، الذي يثبط محورًا رئيسيًا للنمو والتمثيل الغذائي داخل الخلايا يُدعى mTOR. في ظروف ارتفاع السكر، نشطت إشارات mTOR بقوة في الخلايا الجذعية. أضعف إيفروليموس هذا الإشارة، وقلّل دخول الجلوكوز، وخفّض الإجهاد التأكسدي الميتوكوندري بشكل أكثر فاعلية من الدواء الأقدم رابامايسين. عند جرعات نانومولارية منخفضة، حافظ إيفروليموس على فرق الجهد عبر غشاء الميتوكوندريا، ونظّم دفاعات الخلية المضادة للأكسدة، وخفّض مؤشرات الموت المبرمج. في جرذان مصابة باعتلال الشبكية السكّري، أدت حقن تحت الملتحمة لخلايا مُعالجة مسبقًا بالإيفروليموس إلى تعافٍ أقوى في الاستجابات الكهربائية للشبكية وحفاظ أفضل على بنية الشبكية مقارنة بالخلايا غير المعالجة.
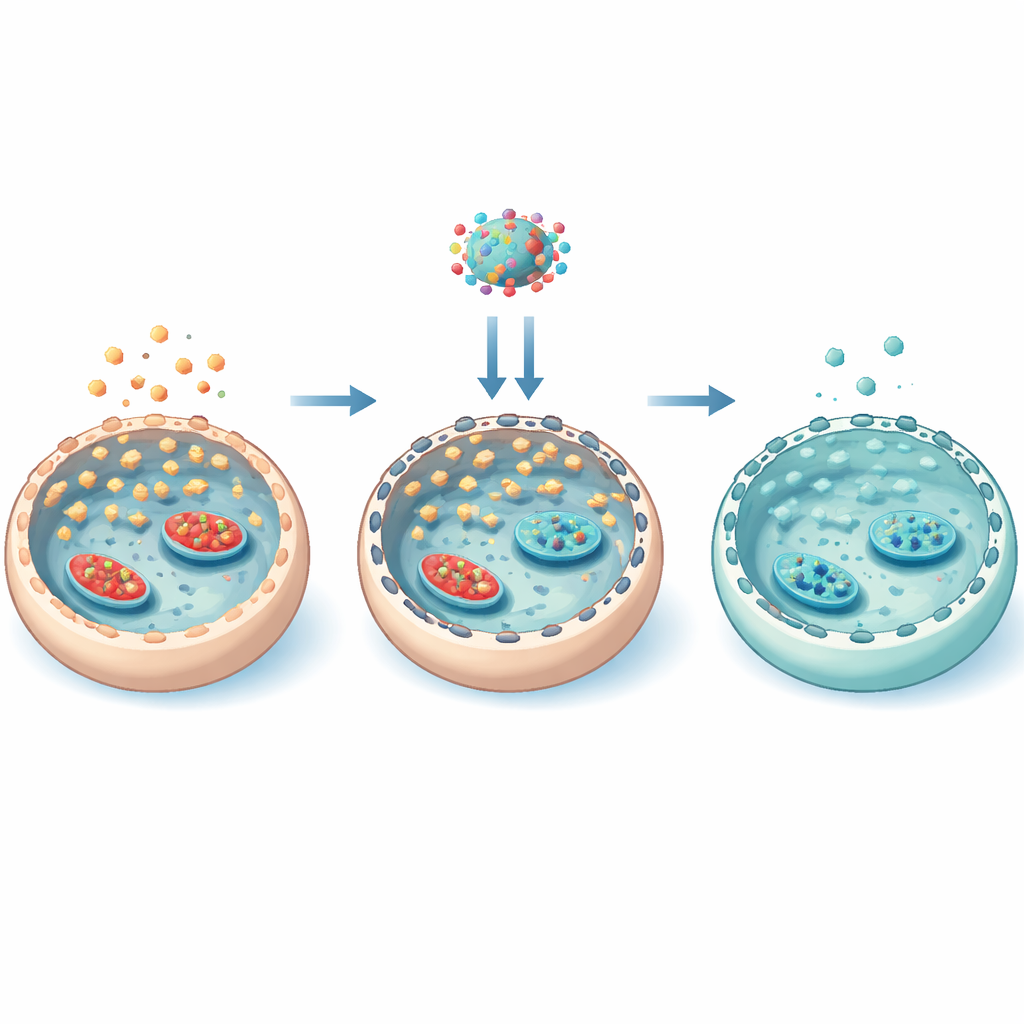
سقالة مخفية تتحكم في دخول السكر
لفهم كيف عمل الإيفروليموس بخصوصية، ركز الفريق على الهيكل الداخلي الخلوي من خيوط الأكتين. تحت ظروف السكر العالي، زادت نشاطات mTOR فسفرة بروتين يُسمى كوفيلين، مما يقفل الأكتين في خيوط أكثر استقرارًا. ساعدت هذه السقالة الثابتة على نقل بوّابات GLUT3 إلى سطح الخلية، مما زاد من دخول السكر. عكس إيفروليموس هذه السلسلة: خفّض نشاط mTOR، وقلّل فسفرة كوفيلين، وراخى شبكة الأكتين، وسحب GLUT3 بعيدًا عن الغشاء. أكدت تجارب ثبتت أو عطّلت الأكتين أن هذا إعادة الترتيب الفيزيائية للسقالة كانت أساسية للتحكم في موقع GLUT3. ومن المهم أن إيفروليموس لم يُعدّ برمجة كل إنزيمات معالجة الجلوكوز بشكل واسع؛ بل تحكّم أساسًا في مقدار السكر الذي يمكن أن يدخل عن طريق وضع ناقلات الجلوكوز.
ماذا تعني هذه النتائج لعلاجات العين المستقبلية
بالنسبة لقارئ غير متخصص، الخلاصة أن الدراسة تُظهر كيف أن إعداد الخلايا الجذعية مسبقًا يمكن أن يساعدها على البقاء في بيئة العين القاسية والمشبعة بالسكر لدى مرضى السكري. باستخدام الإيفروليموس قبل الزرع، تمكن الباحثون من إغلاق بعض "أبواب" السكر على الخلايا، وتهدئة ميتوكوندرياتها المثقلة، ومنع الموت الخلوي المبكر. في النماذج الحيوانية، قامت هذه الخلايا المُدقّية بعمل أفضل في حماية وإعادة بناء نسيج الشبكية وتحسين وظيفتها. وبينما هناك حاجة لمزيد من العمل قبل أن يُجرّب هذا النهج على المرضى، تشير النتائج إلى استراتيجية عملية: ضبط دخول السكر واستجابات الإجهاد للخلايا قبل تسليمها، لتكون جاهزة لإصلاح الشبكية المصابة بالسكري بدلاً من أن تُغلبها ظروفها.
الاستشهاد: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
الكلمات المفتاحية: اعتلال الشبكية السكّري, الخلايا الجذعية الميزنكيمية, إيفروليموس, الإجهاد التأكسدي, ناقلات الجلوكوز