Clear Sky Science · pl
Everolimus hamuje transportera glukozy 3 do błony, aby poprawić skuteczność terapeutyczną przeszczepu mezenchymalnych komórek macierzystych pochodzących z krwi pępowinowej w retinopatii cukrzycowej
Dlaczego ochrona wzroku przy cukrzycy ma znaczenie
Osoby z długo trwającą cukrzycą często obawiają się utraty wzroku. Retinopatia cukrzycowa to częste powikłanie oka, w którym delikatne naczynia krwionośne i komórki nerwowe siatkówki są stopniowo uszkadzane przez wysoki poziom cukru. Obecne zastrzyki leków mogą spowolnić chorobę, lecz nie przywracają w pełni delikatnej tkanki oka. W tym badaniu autorzy badają podejście regeneracyjne: użycie komórek macierzystych z krwi pępowinowej i pokazują, jak lek przeciwnowotworowy o nazwie everolimus może poprawić przeżywalność tych komórek w środowisku nasyconym cukrem, takim jak oko cukrzycowe.
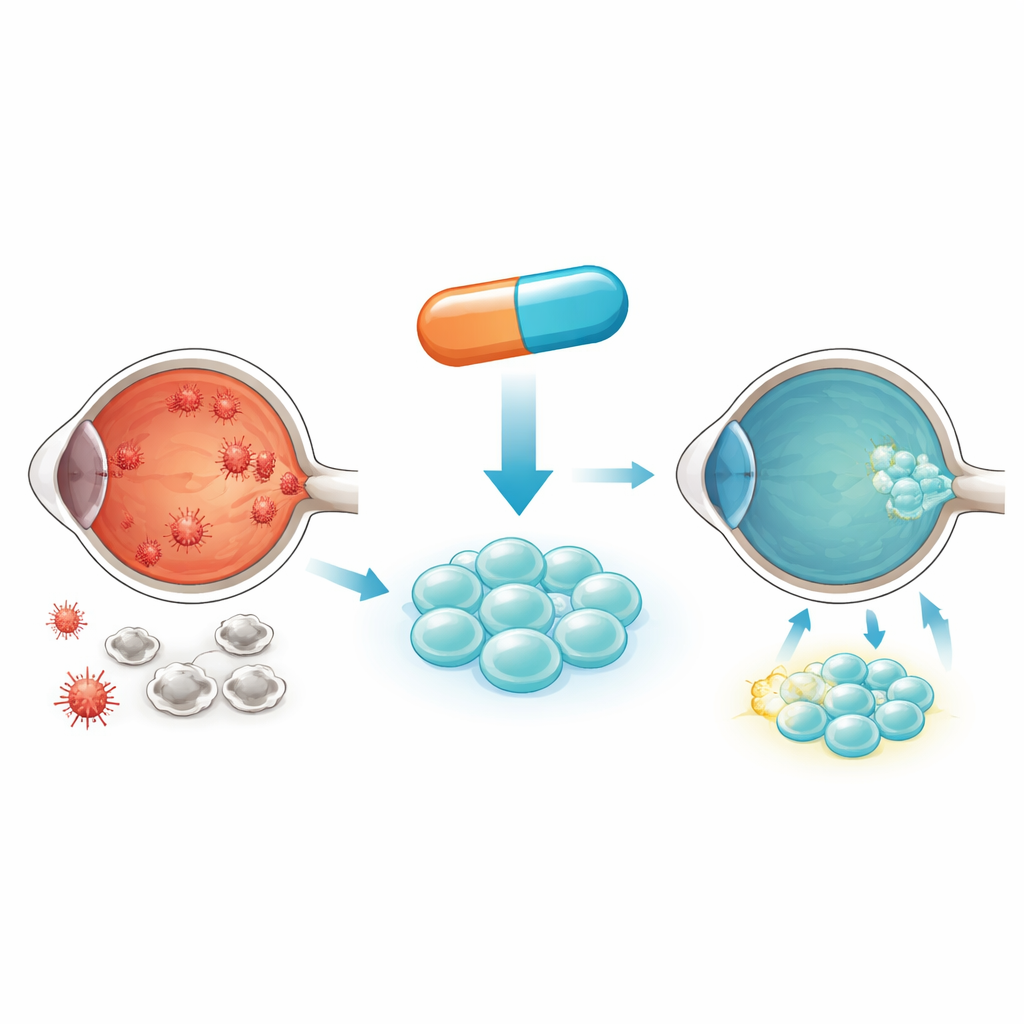
Jak cukrzyca szkodzi oku i napływającym komórkom macierzystym
W cukrzycy nadmiar cukru stale obmywa komórki. Wewnątrz jest on spalany w maleńkich elektrowniach zwanych mitochondriami, które przy przeciążeniu mogą wytwarzać szkodliwe reaktywne formy tlenu. Z czasem ten stres oksydacyjny skłania komórki do przedwczesnego starzenia się i obumierania. Autorzy skupili się na mezenchymalnych komórkach macierzystych pochodzących z krwi pępowinowej, które mogą wspierać i naprawiać uszkodzoną tkankę siatkówki. Niestety, gdy te komórki są umieszczane w warunkach o wysokim stężeniu cukru, podobnych do krwi cukrzycowej, pochłaniają zbyt dużo glukozy, generują nadmierny stres mitochondrialny i zaczynają obumierać. Oznacza to, że pozostaje mniej zdrowych komórek zdolnych do ratowania siatkówki.
Drzwi dla cukru, które wyrządzają najwięcej szkody
Komórki używają wyspecjalizowanych „drzwi” w błonach, zwanych transporterami glukozy, aby wpuszczać cukier. Zespół przeanalizował dwa główne typy występujące na tych komórkach: GLUT1 i GLUT3. Gdy badacze wystawili komórki na wysoki poziom cukru przez wiele godzin, oba transportery się zwiększyły, a wychwyt glukozy wzrósł. Jednak poprzez selektywne wyciszanie każdego z transporterów przy użyciu narzędzi genetycznych odkryli, że to GLUT3 odgrywał kluczową rolę w napędzaniu stresu mitochondrialnego. Zablokowanie GLUT3 ostro zmniejszyło gromadzenie się szkodliwych form tlenu, ustabilizowało funkcję mitochondriów i obniżyło ogólny wychwyt cukru. Gdy te komórki z wyciszonym GLUT3 przeszczepiono do szczurów z retinopatią cukrzycową, sygnały elektryczne siatkówki i grubość warstwy fotoreceptorów poprawiły się bardziej niż po przeszczepie niezmodyfikowanych komórek.
Lek przeciwnowotworowy wykorzystany ponownie, by osłonić komórki macierzyste
Naukowcy zapytali następnie, czy mała cząsteczka mogłaby naśladować korzyści wynikające z kontroli GLUT3. Zwrócili się ku everolimusowi, który blokuje kluczowy węzeł wzrostu i metabolizmu w komórkach, zwany mTOR. W warunkach wysokiego stężenia cukru szlak mTOR był silnie aktywowany w komórkach macierzystych. Everolimus osłabił ten sygnał, zmniejszył wejście glukozy i ograniczył stres oksydacyjny mitochondriów skuteczniej niż starszy lek rapamycyna. Przy niskich stężeniach nanomolowych everolimus zachowywał potencjał błony mitochondrialnej, normalizował antyoksydacyjne mechanizmy komórkowe i zmniejszał markery programowanej śmierci komórkowej. U szczurów z retinopatią cukrzycową podspojówkowe wstrzyknięcia komórek uprzednio traktowanych everolimusem prowadziły do silniejszego odzysku odpowiedzi elektrycznych siatkówki i lepszej ochrony struktury siatkówki niż po przeszczepie komórek nieleczonych.
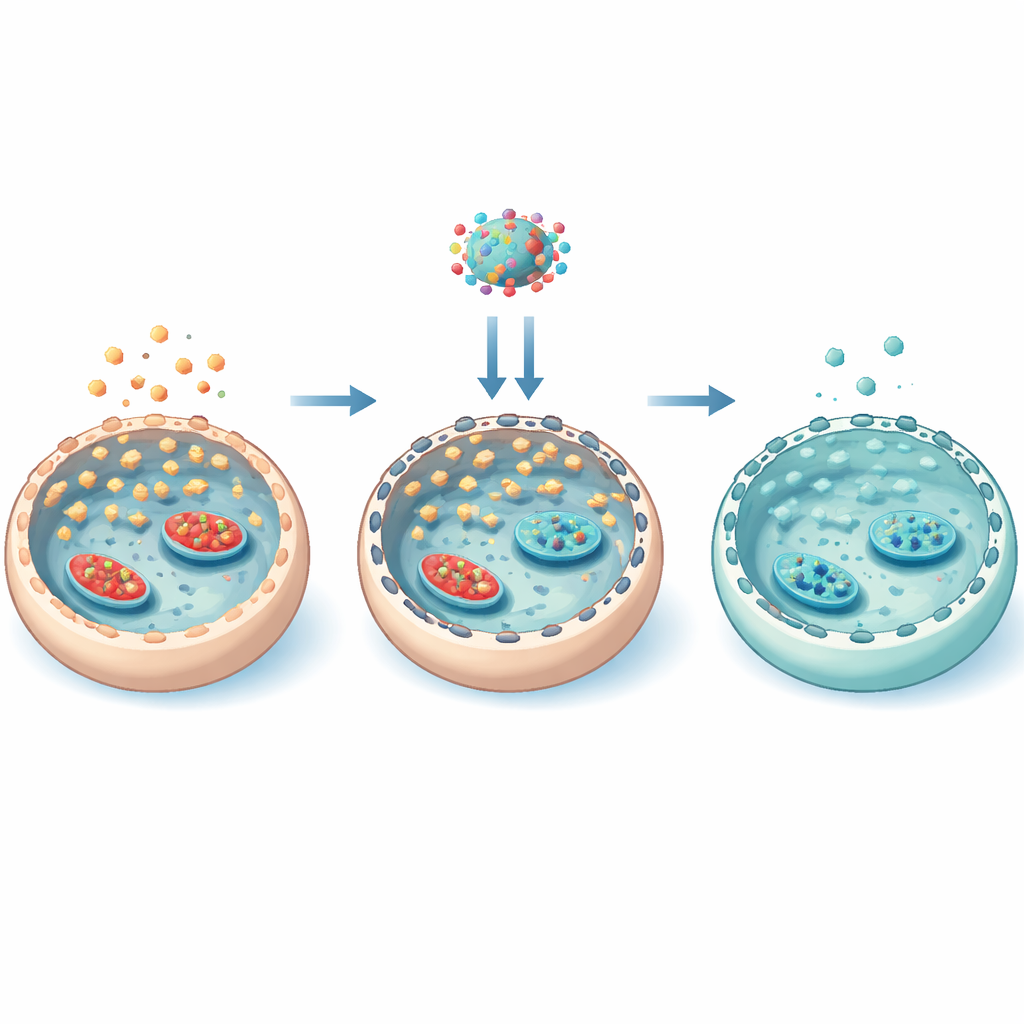
Ukryty szkielet, który kontroluje napływ cukru
Aby zrozumieć, jak everolimus działał tak specyficznie, zespół przyjrzał się wewnętrznemu szkielettowi komórki z filamentów aktynowych. W warunkach wysokiego stężenia cukru aktywność mTOR powodowała zwiększoną fosforylację białka o nazwie cofilina, które „zamraża” aktynę w bardziej stabilnych włóknach. Ten ustabilizowany szkielet ułatwiał przemieszczanie „drzwi” GLUT3 na powierzchnię komórki, zwiększając napływ cukru. Everolimus odwrócił ten ciąg zdarzeń: zmniejszył aktywność mTOR, obniżył fosforylację cofiliny, poluzował sieć aktynową i wycofał GLUT3 z błony. Eksperymenty, które stabilizowały lub zakłócały aktynę, potwierdziły, że ta fizyczna reorganizacja szkieletu była kluczowa dla kontroli lokalizacji GLUT3. Co istotne, everolimus nie przebudowywał szeroko wszystkich enzymów przetwarzających glukozę; zamiast tego głównie regulował, ile cukru może dostać się do wnętrza poprzez pozycjonowanie transporterów.
Co te odkrycia znaczą dla przyszłych terapii oka
Dla czytelnika nietechnicznego sedno jest takie: badanie pokazuje, jak przygotowanie komórek macierzystych przed przeszczepem może pomóc im przetrwać surowe, zasłodzone środowisko oka cukrzycowego. Poprzez zastosowanie everolimusu przed przeszczepem badacze zdołali „zamknąć” część drzwi dla cukru na komórkach, uspokoić ich przeciążone mitochondria i zapobiec wczesnej śmierci komórek. W modelach zwierzęcych te twardsze komórki lepiej chroniły i odbudowywały tkankę siatkówki oraz poprawiały jej funkcję. Choć przed próbami u pacjentów potrzeba jeszcze badań, praca ta wskazuje praktyczną strategię: dostroić napływ cukru i reakcje na stres w komórkach przed ich podaniem, aby były gotowe naprawiać cukrzycową siatkówkę, zamiast być przez nią przytłoczone.
Cytowanie: Jo, H.Y., Jung, J.S., Jo, H.H. et al. Everolimus suppresses glucose transporter 3 membrane trafficking to improve therapeutic efficacy of umbilical cord blood-derived mesenchymal stem cell transplantation in diabetic retinopathy. Cell Death Dis 17, 426 (2026). https://doi.org/10.1038/s41419-026-08673-6
Słowa kluczowe: retinopatia cukrzycowa, mezenchymalne komórki macierzyste, everolimus, stres oksydacyjny, transportery glukozy