Clear Sky Science · zh
苹果酸酶2通过与TRIM25竞争相互作用稳定ATAD3A,从而抑制PINK1-Parkin介导的线粒体自噬
为什么这些微小的能量工厂很重要
我们体内的每个细胞都依赖线粒体——这些制造能量的小型发电站。细胞不断修复和回收这些结构,当这一清理过程出错时,会促进包括癌症和神经退行性疾病在内的病理发生。本研究探讨了一种长期以参与能量产生而闻名的代谢酶苹果酸酶2(ME2),如何在肝癌细胞中出人意料地充当线粒体清理的‘交通指挥’,改变受损线粒体被清除的速度以及肿瘤细胞的生长能力。
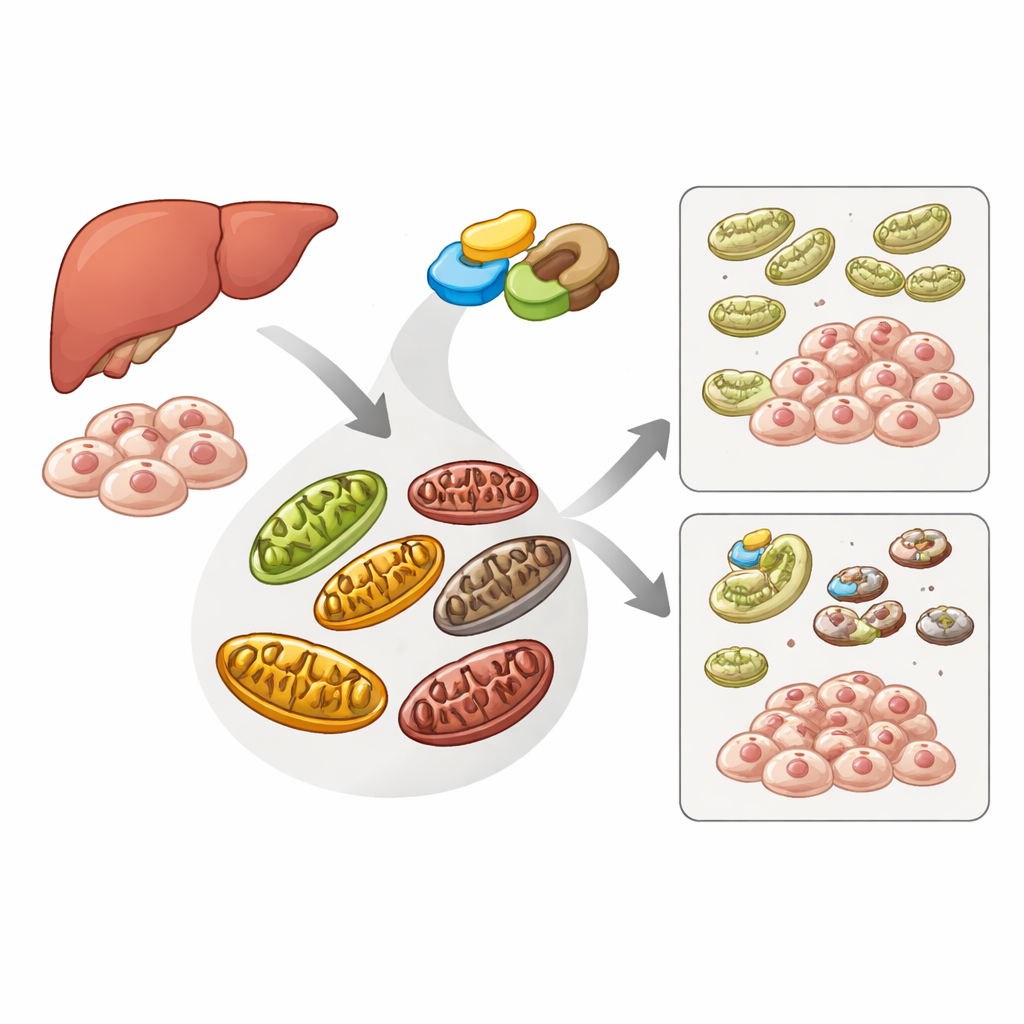
细胞对受损发电站的清理队伍
细胞使用一种专门的回收途径——线粒体自噬(mitophagy)来识别并除去受损线粒体,以免它们伤害细胞。一个名为PINK1的传感蛋白和一个名为Parkin的辅助蛋白是该通路的核心:当线粒体不健康时,PINK1在其表面积累,吸引Parkin,共同给故障的细胞器打上标记以便降解。另一个蛋白ATAD3A通常帮助将PINK1运入线粒体以使其被分解,从而防止不必要的清理。作者想弄清楚,作为细胞主要能量生成循环支持者的ME2,是否也会影响这一质量控制系统。
当ME2丧失时,线粒体清理进入过度状态
研究者在带有线粒体自噬报告系统的人类细胞系中下调ME2并观察结果。他们发现Parkin招募到线粒体的现象显著增加,线粒体自噬标志物升高,表明更多线粒体被标记并清除。在肝癌(HepG2)细胞中,ME2缺失导致PINK1在线粒体上积累,同时关键线粒体蛋白减少,这与活跃的降解一致。显微镜观察显示线粒体与自噬体标志的重叠增多,确认受损‘发电站’被细胞回收机械吞噬的频率远高于正常水平。
过度清理削弱细胞的能量系统
尽管理想程度的线粒体自噬有保护作用,但过度则有害。在ME2耗竭的肝癌细胞中,线粒体变得支离破碎且稀少,ATP产量下降,线粒体DNA拷贝数减少。细胞产生更多活性氧分子,膜电位降低,都是线粒体受压或功能衰竭的标志。氧耗测量显示其呼吸能力明显受损。在功能上,这些细胞增殖变慢,形成的克隆减少,三维球体体积更小。用药物阻断线粒体自噬或沉默PINK1本身,能部分挽救细胞生长,将增殖减缓直接关联到过度活跃的线粒体清理。
决定线粒体命运的蛋白质拉锯战
为了解ME2如何控制该过程,研究团队筛查了与其物理相互作用的蛋白,发现了调节PINK1的线粒体门控蛋白ATAD3A。他们证明ME2与ATAD3A结合,并保护其免受TRIM25破坏——TRIM25是一种通过给目标蛋白加上“我要被扔掉”的小标签,从而将其送往细胞蛋白降解机械的蛋白。当ME2缺失时,TRIM25对ATAD3A的标记增多,导致ATAD3A被降解,降低了清除线粒体表面PINK1的能力。结果是PINK1滞留、线粒体自噬激增,线粒体被过度清除。重要的是,即便缺乏催化活性的ME2突变体仍能抑制线粒体自噬,表明其支架作用——与ATAD3A结合并与TRIM25竞争——在这里比其酶学活性更为关键。
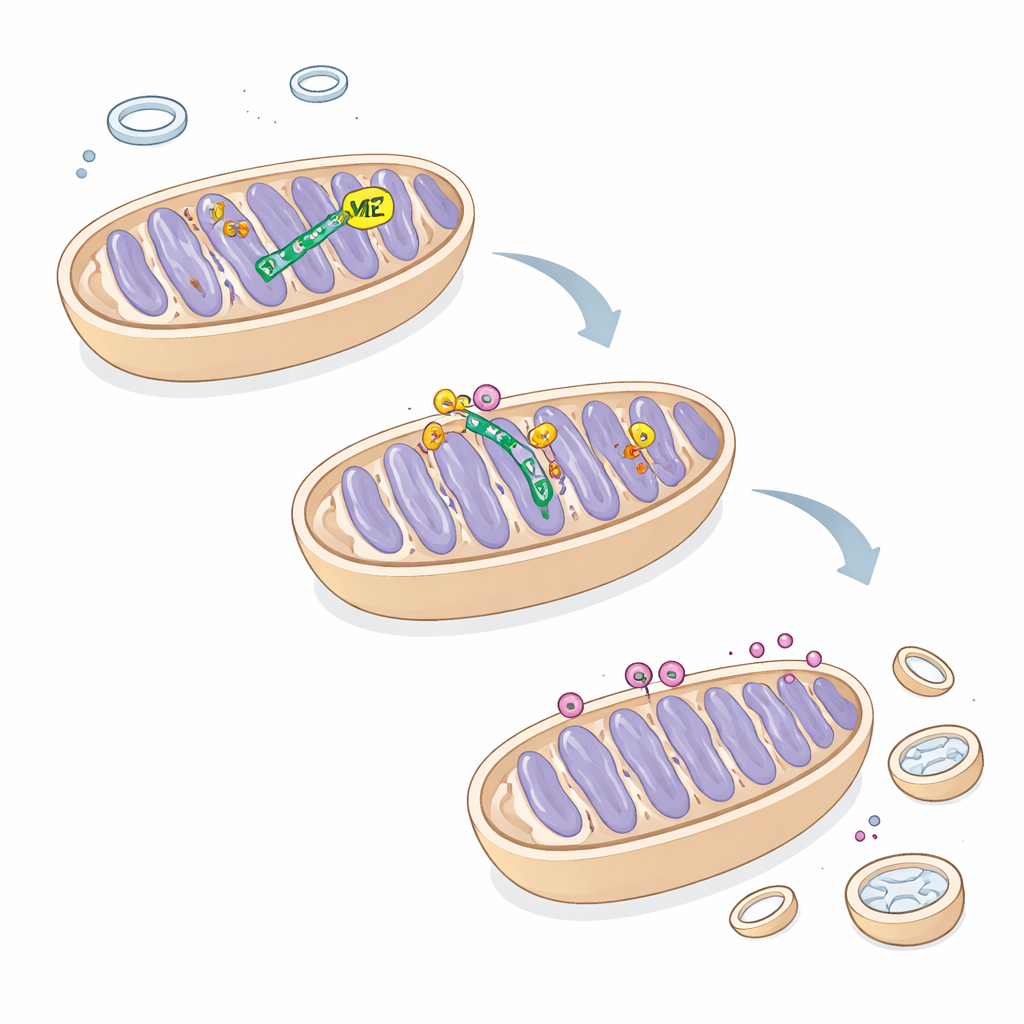
在肝癌中重新平衡生长与清理
通过在TRIM25过表达的细胞中恢复ME2,作者能够抑制线粒体自噬,改善线粒体形态与功能,并部分恢复细胞增殖。这些发现揭示了一个先前未被注意的回路:ME2保护ATAD3A,使PINK1得以适当周转,从而将线粒体清理保持在受控范围。对普通读者来说,结论是:一种曾被简单视为燃料燃烧助推器的酶,也以结构性调节者的身份平衡线粒体何时被修复或被销毁。在肝癌细胞中,失去ME2会将清理系统推向过度运转,剥夺细胞的能量生产装置并减慢其生长——这是一种未来可能被利用的脆弱性。
引用: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
关键词: 线粒体自噬, 线粒体, 苹果酸酶2, 肝癌, 细胞代谢