Clear Sky Science · ar
إنزيم الماليك 2 يثبط التميتوفاغي المعتمد على PINK1-Parkin عن طريق استقرار ATAD3A عبر تداخل تنافسي مع TRIM25
لماذا تهم المحطات الصغيرة للطاقة في السرطان
تعتمد كل خلية في أجسامنا على الميتوكوندريا، المحطات الصغيرة للطاقة التي تولّد الطاقة. تقوم الخلايا باستمرار بإصلاح وإعادة تدوير هذه البنى، وعندما يختل هذا المسار يمكن أن يساهم في أمراض مثل السرطان والتنكس العصبي. تستكشف هذه الدراسة كيف يعمل إنزيم أيضي يسمى إنزيم الماليك 2 (ME2)، المعروف منذ زمن بدوره في إنتاج الطاقة، بشكل غير متوقع كضابط مرور لعملية تنظيف الميتوكوندريا في خلايا سرطان الكبد — مغيرًا من سرعة إزالة الميتوكوندريا التالفة وقدرة الخلايا الورمية على النمو.
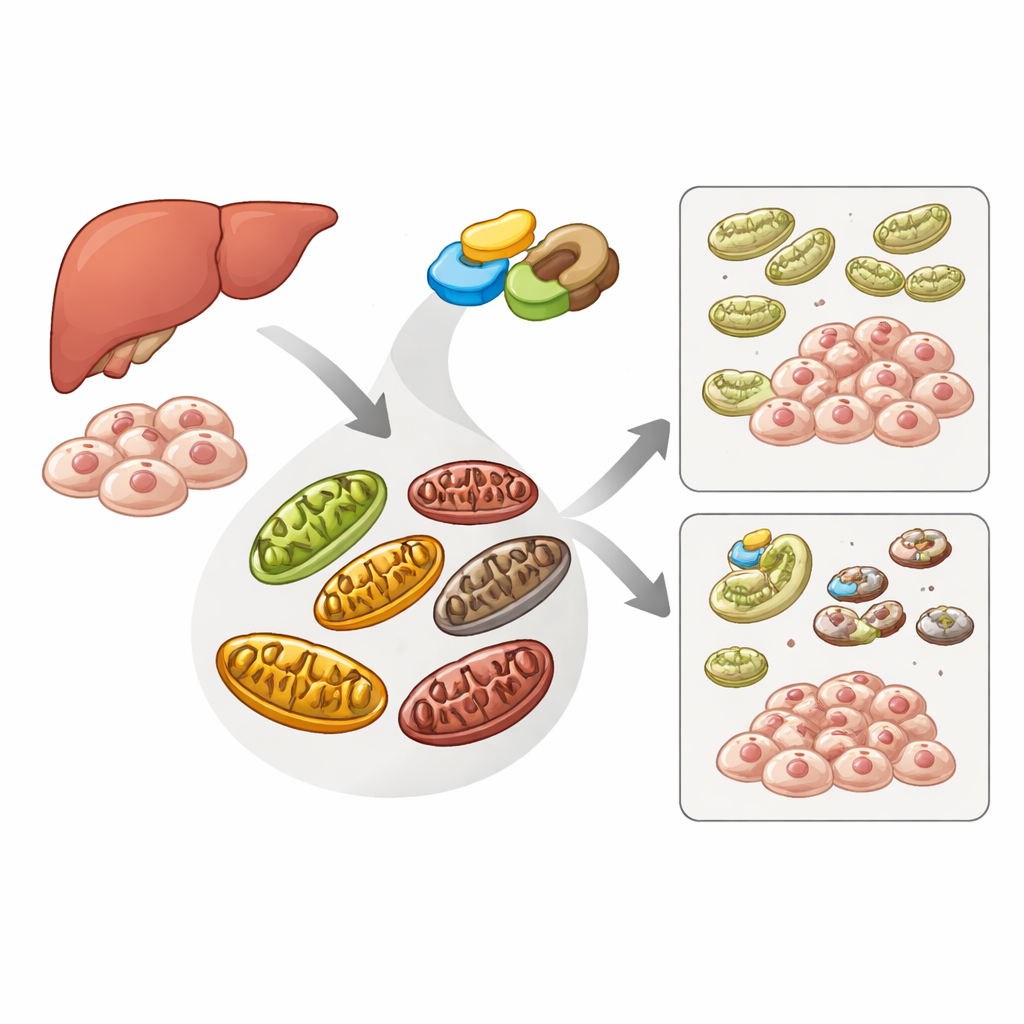
طواقم التنظيف الخلوية للمحطات الطاقية التالفة
تستخدم الخلايا مسارًا متخصصًا لإعادة التدوير يُسمى التميتوفاغي للتعرّف على الميتوكوندريا التالفة وإزالتها قبل أن تُلحق الضرر بالخلية. بروتين استشعاري يسمى PINK1 وبروتين مساعد يسمى Parkin يقفان في قلب هذا المسار: عندما تكون الميتوكوندريا غير صحية، يتراكم PINK1 على سطحها، ويجذب Parkin، ومعًا يعلّمان العضية المعيبة للتخلص منها. بروتين آخر، ATAD3A، يساعد عادةً في نقل PINK1 داخل الميتوكوندريا حتى يتم تكسيره، مانعًا عملية التنظيف غير الضرورية. سعى المؤلفون لاكتشاف ما إذا كان ME2، المعروف أساسًا بدعمه للدورة الرئيسية لتوليد الطاقة في الخلية، يؤثر أيضًا على هذا النظام للسيطرة على الجودة.
عند فقدان ME2، يسرع تنظيف الميتوكوندريا بشكل مفرط
باستخدام سلالات خلوية بشرية معدلة للإبلاغ عن نشاط التميتوفاغي، قلّل الباحثون مستويات ME2 ورصدوا ما يحدث. لاحظوا ارتفاعًا لافتًا في جذب Parkin إلى الميتوكوندريا وزيادة في مؤشرات التميتوفاغي، مما يدل على وضع علامات وإزالة عدد أكبر من الميتوكوندريا. في خلايا سرطان الكبد (HepG2)، أدّى فقدان ME2 إلى تراكم PINK1 على الميتوكوندريا في حين اختفت بروتينات ميتوكوندرية رئيسية، وهو ما يتسق مع التحلل النشط. أظهرت الميكروسكوبية زيادة التداخل بين الميتوكوندريا وعلامات الجسيمات الذاتية، مؤكدة أن المحطات الطاقية التالفة كانت تُبتلع بواسطة آليات إعادة التدوير في الخلية بوتيرة أعلى بكثير من الطبيعي.
كثرة التنظيف تضعف نظام الطاقة الخلوي
بينما يكون بعض التميتوفاغي وقائيًا، فإن الإفراط فيه يمكن أن يكون ضارًا. في خلايا سرطان الكبد المنزوعة ME2، أصبحت الميتوكوندريا مجزأة ونادرة، انخفض إنتاج ATP، وتناقص عدد نسخ الحمض النووي الميتوكوندري. أنتجت الخلايا المزيد من الجزيئات التفاعلية للأكسجين وكان لديها إمكانات غشائية أدنى، وكلاهما علامات على ميتوكوندريا متوترة أو متدهورة. كشفت قياسات استهلاك الأكسجين أن قدرتها التنفسية تدهورت بشكل ملحوظ. وظيفيًا، انقسمت هذه الخلايا بوتيرة أبطأ، شكلت مستعمرات أقل، وأنتجت كريات ثلاثية الأبعاد أصغر. أدى حجب التميتوفاغي بالأدوية، أو إسكات مستشعر PINK1 نفسه، إلى إنقاذ جزئي لنمو الخلايا، مما يربط تباطؤ التكاثر مباشرةً بفرط نشاط تنظيف الميتوكوندريا.
شد حبل بروتيني يقرر مصير الميتوكوندريا
لفهم كيف يتحكم ME2 في هذه العملية، بحث الفريق عن بروتينات ترتبط به فعليًا وحدد ATAD3A، حارس البوابة الميتوكوندرية الذي يساعد في تنظيم PINK1. أظهروا أن ME2 يرتبط بـATAD3A ويحميه من التحلل بواسطة TRIM25، وهو بروتين يعلّم البروتينات الأخرى بإشارات صغيرة «اقتلني» ليتم تكسيرها بواسطة آلية التهديم البروتيني في الخلية. عندما غاب ME2، وضع TRIM25 علامات أكثر على ATAD3A، مما أدى إلى تحلّله وانخفاض القدرة على إزالة PINK1 من سطح الميتوكوندريا. نتيجة لذلك، ظل PINK1 متراكمًا، تصاعد التميتوفاغي، وأزيلت الميتوكوندريا بشكل مفرط. والأهم أن نسخًا طفيلية من ME2 خالية من النشاط التحفيزي لا تزال تقمع التميتوفاغي، مشيرةً إلى أن دورها الهيكلي — الاحتفاظ بـATAD3A والتنافس مع TRIM25 — هو ما يهم هنا، وليس وظيفتها الكيميائية.
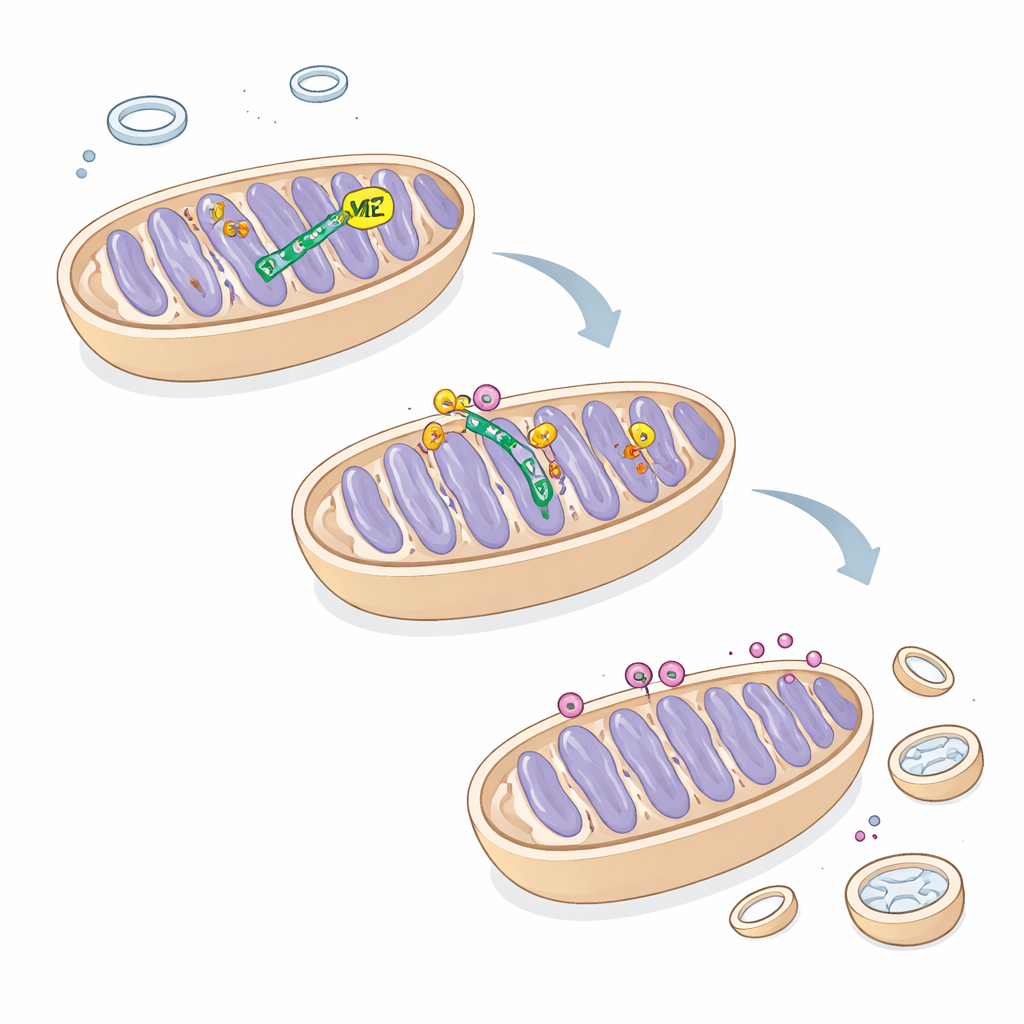
إعادة توازن النمو والتنظيف في سرطان الكبد
من خلال استعادة ME2 في خلايا محمّلة بـTRIM25، تمكن المؤلفون من التخفيف من التميتوفاغي، وتحسين شكل الميتوكوندريا ووظيفتها، واستعادة التكاثر الخلوي جزئيًا. تكشف هذه النتائج عن دائرة مخفية سابقًا يقي فيها ME2 ATAD3A، مما يسمح بتدوير مناسب لـPINK1 ويحافظ على ضبط تنظيف الميتوكوندريا. للقراء غير المتخصصين، الرسالة أن إنزيمًا كان يُعتقد سابقًا أنه يساعد ببساطة في حرق الوقود يعمل أيضًا كمنظّم هيكلي يوازن بين متى تُصلح الميتوكوندريا ومتى تُدمر. في خلايا سرطان الكبد، يؤدي اضطراب هذا التوازن بفقدان ME2 إلى دفع نظام التنظيف إلى فرط النشاط، مجتثًا خلايا الآلات المنتجة للطاقة ومبطئًا نموها — وهي نقطة ضعف قد يُستغل يومًا ما لعلاجات جديدة.
الاستشهاد: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
الكلمات المفتاحية: التميتوفاغي, الميتوكوندريا, إنزيم الماليك 2, سرطان الكبد, تمثيل الخلايا الغذائي