Clear Sky Science · it
L’enzima malico 2 sopprime la mitofagia mediata da PINK1-Parkin stabilizzando ATAD3A tramite un’interazione competitiva con TRIM25
Perché i piccoli “generatori” sono importanti nel cancro
Ogni cellula del nostro organismo dipende dai mitocondri, i piccoli impianti energetici che producono energia. Le cellule riparano e riciclano continuamente queste strutture e, quando questo processo di pulizia va storto, può contribuire a malattie come il cancro e le neurodegenerazioni. Questo studio esplora come un enzima metabolico chiamato enzima malico 2 (ME2), noto da tempo per il suo ruolo nella produzione di energia, agisca inaspettatamente come un regolatore del traffico per la pulizia mitocondriale nelle cellule del cancro del fegato—modificando la velocità con cui i mitocondri danneggiati vengono rimossi e la capacità delle cellule tumorali di proliferare.
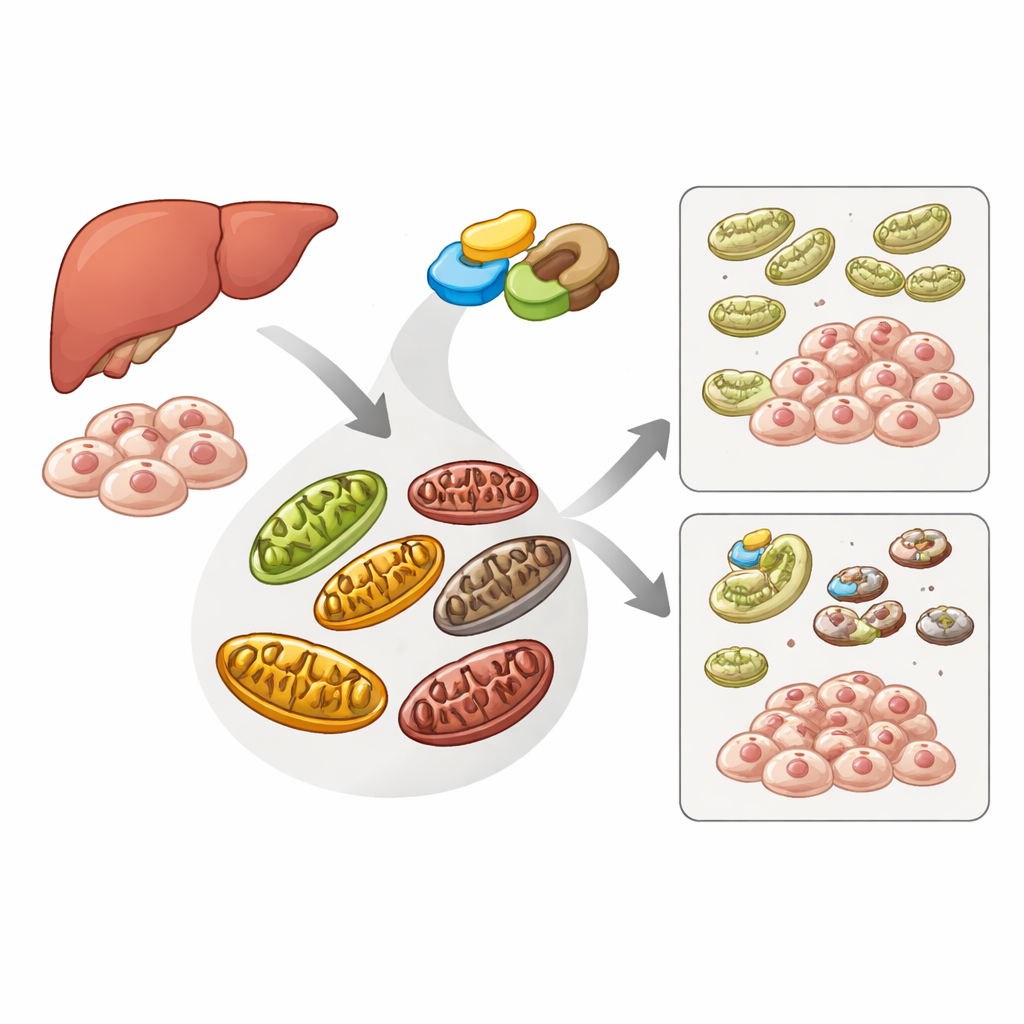
La squadra di pulizia della cellula per gli impianti energetici danneggiati
Le cellule usano una via di riciclo specializzata, la mitofagia, per identificare e rimuovere i mitocondri danneggiati prima che danneggino la cellula. Una proteina sensore chiamata PINK1 e una proteina ausiliaria chiamata Parkin sono al centro di questa via: quando i mitocondri sono malsani, PINK1 si accumula sulla loro superficie, recluta Parkin e insieme etichettano l’organello difettoso per la distruzione. Un’altra proteina, ATAD3A, normalmente aiuta a trasportare PINK1 nei mitocondri affinché venga degradato, evitando una pulizia non necessaria. Gli autori hanno voluto scoprire se ME2, noto soprattutto per il supporto al principale ciclo di produzione energetica della cellula, influenzi anche questo sistema di controllo qualità.
Quando ME2 viene perso, la pulizia mitocondriale accelera
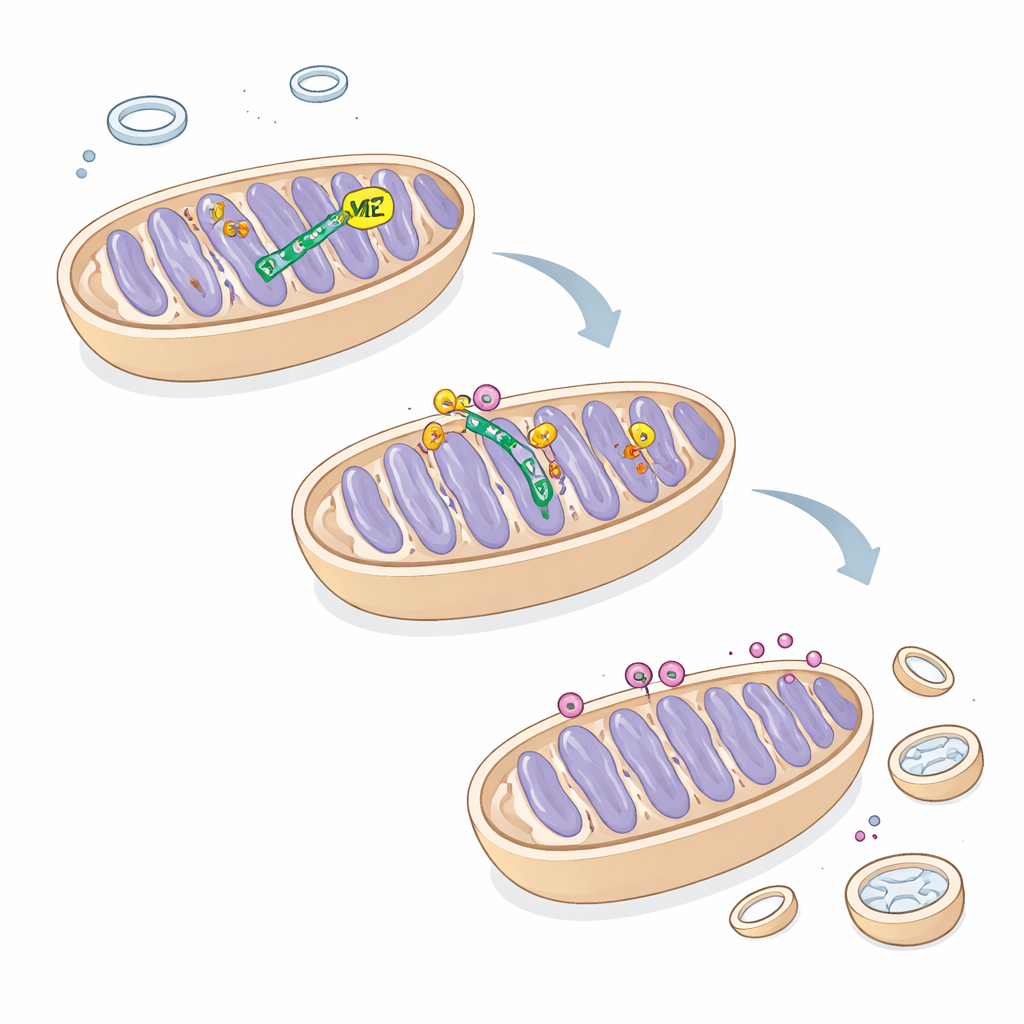
Usando linee cellulari umane ingegnerizzate per riportare l’attività di mitofagia, i ricercatori hanno ridotto i livelli di ME2 e osservato cosa accadeva. Hanno riscontrato un netto aumento del reclutamento di Parkin sui mitocondri e un incremento dei marcatori di mitofagia, indicando che più mitocondri venivano etichettati e rimossi. Nelle cellule di cancro del fegato (HepG2), la perdita di ME2 ha causato l’accumulo di PINK1 sui mitocondri mentre proteine mitocondriali chiave scomparivano, coerente con una degradazione attiva. La microscopia ha mostrato una maggiore sovrapposizione tra mitocondri e marker dell’autofagosoma, confermando che i “generatori” danneggiati venivano inglobati dalla macchina di riciclo della cellula molto più frequentemente del normale.
Troppa pulizia indebolisce il sistema energetico della cellula
Se da un lato una certa mitofagia è protettiva, un’eccessiva attività può essere dannosa. Nelle cellule di cancro del fegato prive di ME2, i mitocondri risultavano frammentati e scarsi, la produzione di ATP diminuiva e il numero di copie del DNA mitocondriale calava. Le cellule producevano più radicali reattivi e presentavano un potenziale di membrana ridotto, entrambi segnali di mitocondri sotto stress o in malfunzionamento. Le misurazioni del consumo di ossigeno hanno rivelato che la loro capacità respiratoria era significativamente compromessa. Dal punto di vista funzionale, queste cellule si dividevano più lentamente, formavano meno colonie e generavano sfere tridimensionali più piccole. Bloccare la mitofagia con farmaci, o silenziare lo stesso sensore PINK1, ha parzialmente recuperato la crescita cellulare, collegando il rallentamento della proliferazione direttamente a un’eccessiva attività di pulizia mitocondriale.
Una lotta proteica che decide il destino dei mitocondri
Per capire come ME2 controlli questo processo, il gruppo ha cercato proteine che si associano fisicamente a ME2 e ha identificato ATAD3A, il custode mitocondriale che aiuta a regolare PINK1. Hanno dimostrato che ME2 si lega ad ATAD3A e la protegge dalla distruzione operata da TRIM25, una proteina che etichetta altre proteine con piccoli segnali “buttami” per la loro eliminazione dal sistema di degradazione cellulare. Quando ME2 veniva meno, TRIM25 aggiungeva più tag ad ATAD3A, portando alla sua degradazione e riducendo la capacità di eliminare PINK1 dalla superficie mitocondriale. Di conseguenza, PINK1 persisteva, la mitofagia aumentava e i mitocondri venivano rimossi in eccesso. Importante, anche versioni mutanti di ME2 prive dell’attività catalitica riuscivano comunque a limitare la mitofagia, indicando che il ruolo strutturale—il tenere legata ATAD3A e competere con TRIM25—è ciò che conta qui, non la sua funzione enzimatica.
Ribilanciare crescita e pulizia nel cancro del fegato
Ripristinando ME2 in cellule sovraccariche di TRIM25, gli autori sono riusciti ad attenuare la mitofagia, migliorare la forma e la funzione mitocondriale e ripristinare parzialmente la proliferazione cellulare. Questi risultati rivelano un circuito prima nascosto in cui ME2 protegge ATAD3A, permettendo un adeguato ricambio di PINK1 e mantenendo sotto controllo la pulizia mitocondriale. Per il lettore non specialista, il messaggio è che un enzima un tempo considerato semplicemente coinvolto nella combustione del carburante agisce anche come regolatore strutturale che bilancia quando i mitocondri vengono riparati rispetto a quando vengono distrutti. Nelle cellule di cancro del fegato, il disordine di questo equilibrio per perdita di ME2 spinge il sistema di pulizia in sovraattività, spogliando le cellule dei macchinari produttori di energia e rallentandone la crescita—una vulnerabilità che in futuro potrebbe essere sfruttata per nuove terapie.
Citazione: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
Parole chiave: mitofagia, mitocondri, enzima malico 2, cancro del fegato, metabolismo cellulare