Clear Sky Science · es
La enzima málica 2 suprime la mitofagia mediada por PINK1-Parkin estabilizando ATAD3A mediante una interacción competitiva con TRIM25
Por qué importan las pequeñas centrales en el cáncer
Cada célula de nuestro cuerpo depende de las mitocondrias, las diminutas centrales energéticas que producen energía. Las células reparan y reciclan constantemente estas estructuras, y cuando este proceso de limpieza falla puede contribuir a enfermedades como el cáncer y la neurodegeneración. Este estudio explora cómo una enzima metabólica llamada enzima málica 2 (ME2), conocida desde hace tiempo por su papel en la producción de energía, actúa inesperadamente como un regulador del reciclaje mitocondrial en células de cáncer hepático: modifica la velocidad a la que se eliminan las mitocondrias dañadas y, por tanto, la capacidad de crecimiento de las células tumorales.
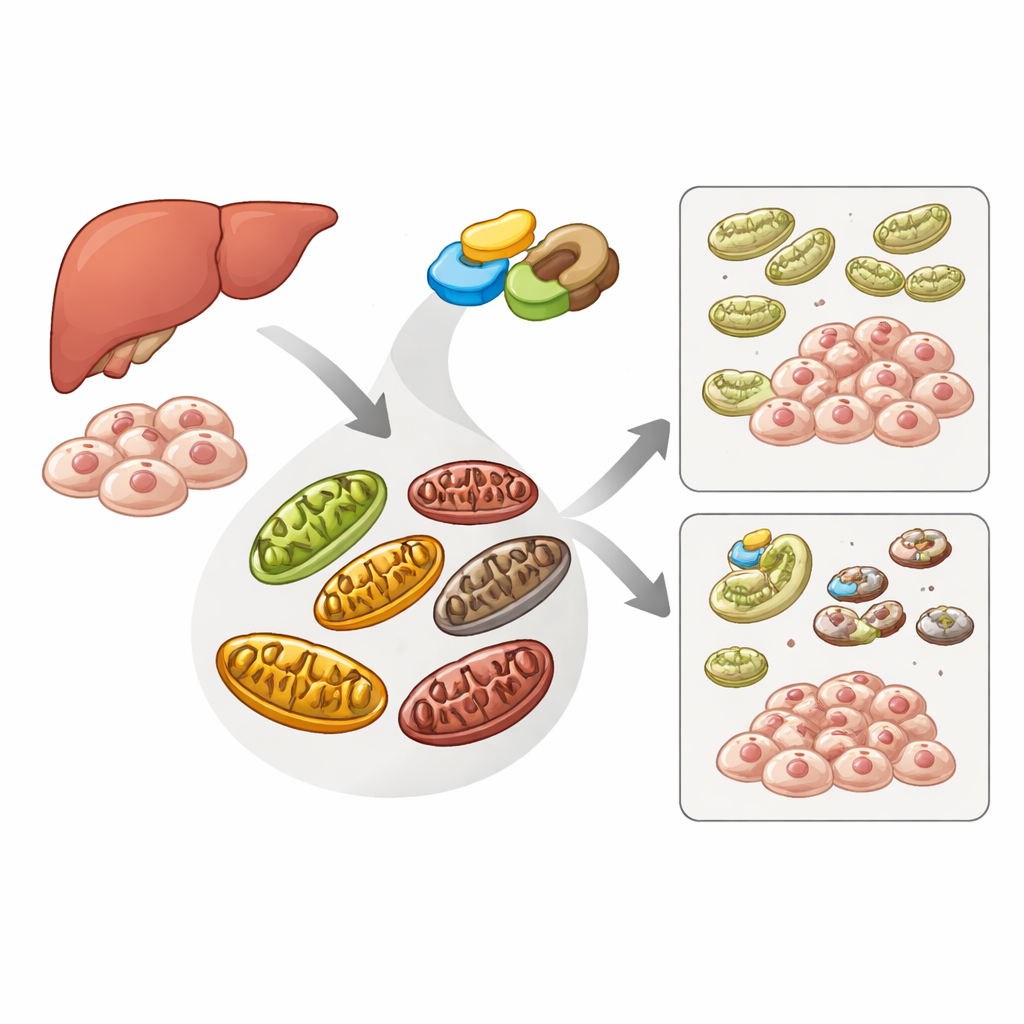
El equipo de limpieza de la célula para centrales dañadas
Las células emplean una vía de reciclaje especializada, la mitofagia, para identificar y eliminar mitocondrias dañadas antes de que perjudiquen a la célula. Una proteína sensor llamada PINK1 y una proteína ayudante llamada Parkin son el núcleo de esta vía: cuando las mitocondrias están enfermas, PINK1 se acumula en su superficie, atrae a Parkin y juntos etiquetan el orgánulo defectuoso para su degradación. Otra proteína, ATAD3A, normalmente ayuda a transportar PINK1 hacia el interior mitocondrial para que pueda ser degradado, evitando una limpieza innecesaria. Los autores se propusieron descubrir si ME2, conocida por sustentar el principal ciclo de generación de energía celular, también influye en este sistema de control de calidad.
Cuando se pierde ME2, la limpieza mitocondrial se desboca
Usando líneas celulares humanas diseñadas para informar sobre la actividad de la mitofagia, los investigadores redujeron los niveles de ME2 y observaron lo que ocurría. Detectaron un notable aumento en la reclutación de Parkin a las mitocondrias y un salto en marcadores de mitofagia, lo que indica que más mitocondrias estaban siendo etiquetadas y eliminadas. En células de cáncer hepático (HepG2), la pérdida de ME2 provocó la acumulación de PINK1 en las mitocondrias mientras que proteínas mitocondriales clave desaparecían, consistente con degradación activa. La microscopía mostró mayor solapamiento entre mitocondrias y marcadores de autofagosomas, confirmando que las centrales dañadas eran engullidas por la maquinaria de reciclaje celular con mucha más frecuencia de lo normal.
Demasiada limpieza debilita el sistema energético de la célula
Aunque cierta mitofagia es protectora, un exceso puede ser perjudicial. En células de cáncer hepático privadas de ME2, las mitocondrias se fragmentaron y quedaron escasas, la producción de ATP descendió y el número de copias del ADN mitocondrial disminuyó. Las células generaron más moléculas reactivas de oxígeno y exhibieron un potencial de membrana reducido, ambos signos de mitocondrias estresadas o en fallo. Las mediciones de consumo de oxígeno revelaron que su capacidad respiratoria estaba significativamente comprometida. Funcionalmente, estas células se dividían más despacio, formaban menos colonias y producían esferas tridimensionales más pequeñas. Bloquear la mitofagia con fármacos, o silenciar el propio sensor PINK1, rescató parcialmente el crecimiento celular, vinculando la ralentización de la proliferación directamente con la mitofagia hiperactiva.
Una lucha proteica que decide el destino de las mitocondrias
Para entender cómo ME2 controla este proceso, el equipo buscó proteínas que se asocien físicamente con ella e identificó ATAD3A, el portero mitocondrial que ayuda a regular PINK1. Mostraron que ME2 se une a ATAD3A y lo protege de la destrucción por TRIM25, una proteína que etiqueta a otras proteínas con pequeñas señales de “destrúyeme” para que la maquinaria degradadora celular las elimine. Cuando ME2 estaba ausente, TRIM25 añadía más etiquetas a ATAD3A, lo que conducía a su degradación y a una menor capacidad para eliminar PINK1 de la superficie mitocondrial. Como resultado, PINK1 persistía, la mitofagia se disparaba y las mitocondrias eran eliminadas en exceso. Es importante que incluso versiones mutantes de ME2 carentes de actividad catalítica siguieran reprimiendo la mitofagia, lo que indica que aquí lo relevante es su papel estructural—mantener a ATAD3A y competir con TRIM25—y no su actividad enzimática.
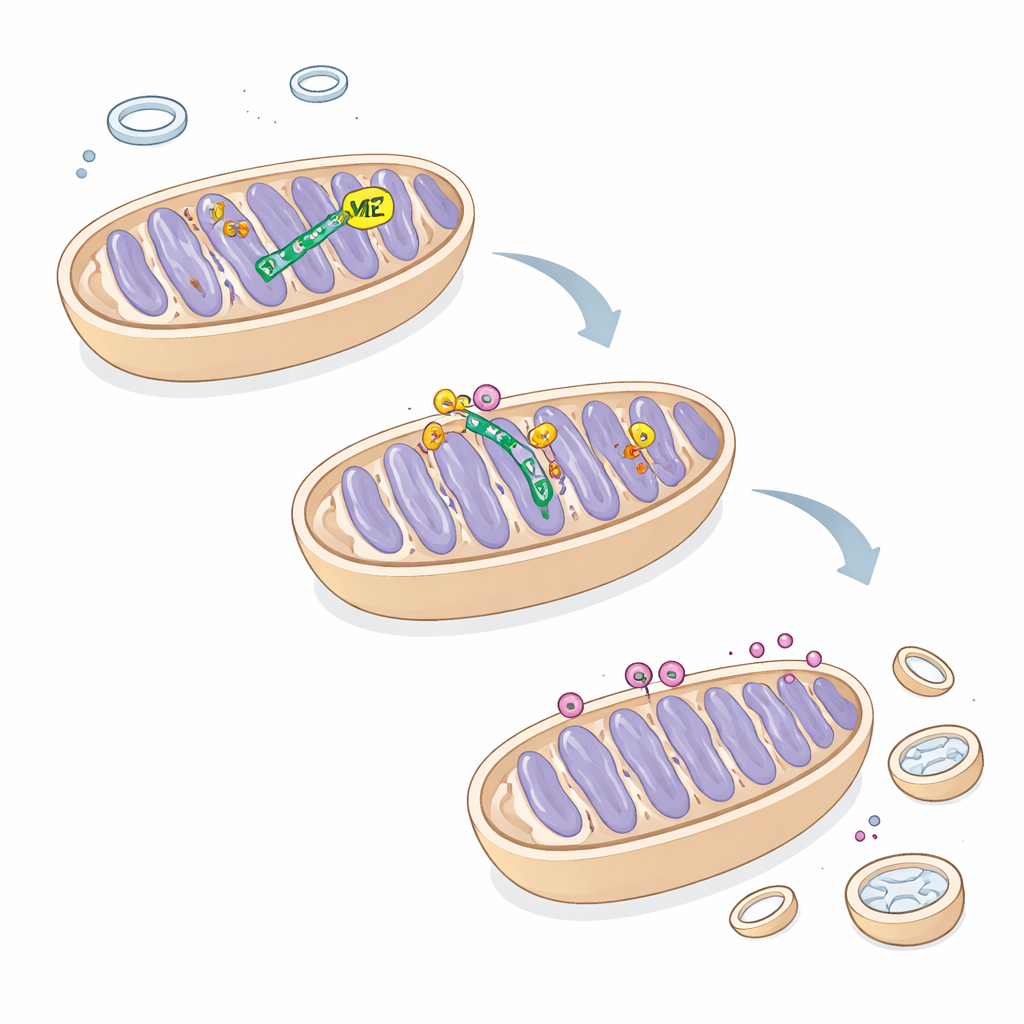
Reequilibrar crecimiento y limpieza en el cáncer de hígado
Restaurando ME2 en células saturadas de TRIM25, los autores pudieron atenuar la mitofagia, mejorar la morfología y función mitocondrial y rescatar parcialmente la proliferación celular. Estos hallazgos revelan un circuito hasta ahora oculto en el que ME2 protege a ATAD3A, permitiendo el recambio apropiado de PINK1 y manteniendo la mitofagia bajo control. Para el lector no especializado, el mensaje es que una enzima antes considerada solo como participante en la combustión de combustible también actúa como regulador estructural que equilibra cuándo las mitocondrias se reparan frente a cuándo se destruyen. En células de cáncer hepático, alterar este equilibrio perdiendo ME2 empuja al sistema de limpieza a la sobreactividad, despojando a las células de la maquinaria productora de energía y frenando su crecimiento—una vulnerabilidad que algún día podría explotarse para nuevas terapias.
Cita: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
Palabras clave: mitofagia, mitocondrias, enzima málica 2, cáncer de hígado, metabolismo celular