Clear Sky Science · ja
マリック酵素2はTRIM25との競合的相互作用を通じてATAD3Aを安定化し、PINK1-Parkin依存性ミトファジーを抑制する
がんにとって小さな発電所が重要な理由
私たちの体のあらゆる細胞は、エネルギーを生み出す小さな発電所であるミトコンドリアに依存しています。細胞はこれらの構造を常に修復・再利用しており、この清掃プロセスが乱れるとがんや神経変性などの疾患に寄与することがあります。本研究は、エネルギー産生に関与する酵素として長く知られるマリック酵素2(ME2)が、肝がん細胞におけるミトコンドリアの清掃(品質管理)を思いがけず制御し、損傷ミトコンドリアの除去速度や腫瘍細胞の増殖に影響を与える仕組みを探ります。
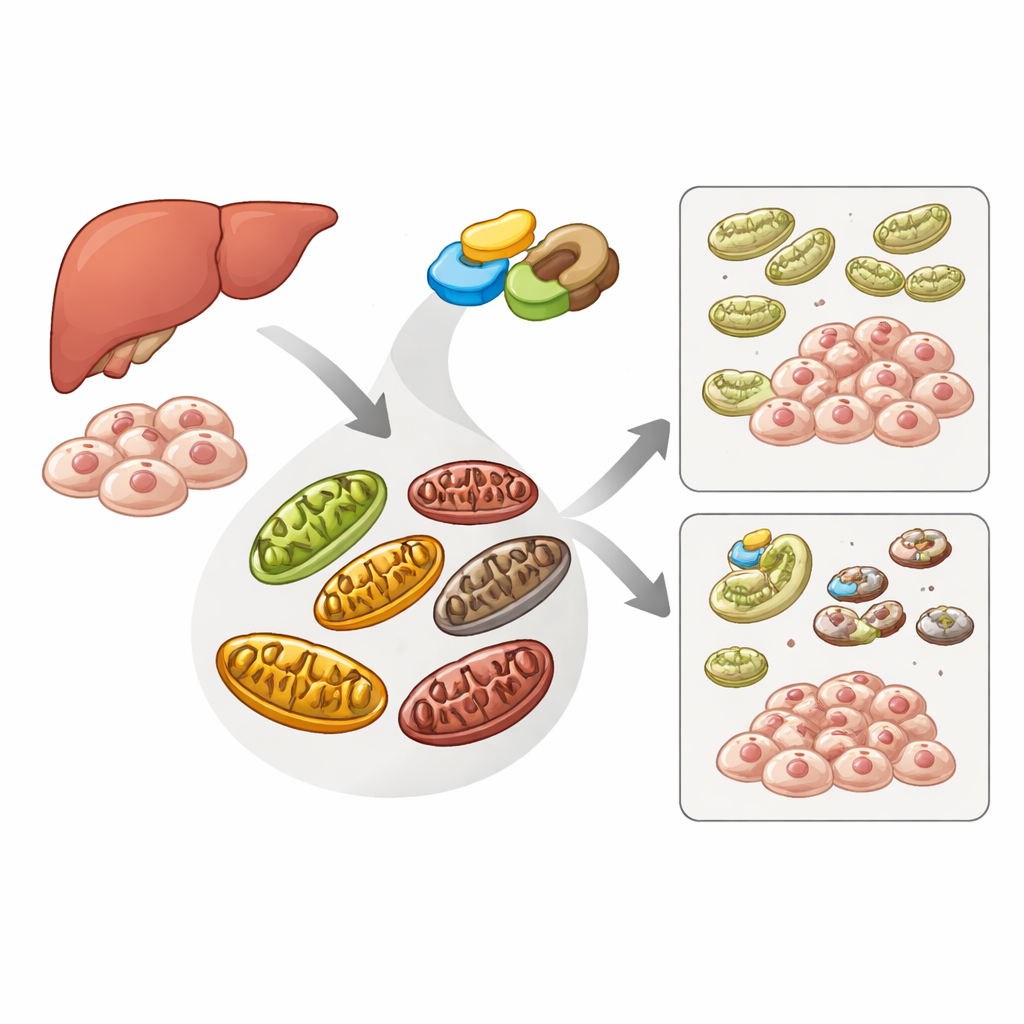
損傷した発電所を片づける細胞の清掃班
細胞はミトファジーという特殊なリサイクル経路を使って、損傷したミトコンドリアを特定して除去し、細胞に害を及ぼす前に処理します。この経路の中心にはセンサータンパク質PINK1と補助タンパク質Parkinがあり、ミトコンドリアが不調になるとPINK1がその表面に蓄積してParkinを呼び寄せ、共同して欠陥あるオルガネラに除去の目印を付けます。別のタンパク質ATAD3Aは通常、PINK1をミトコンドリア内へ運び分解させる役割を担い、不要な清掃が起きないようにします。著者らは、主に細胞の主要なエネルギー産生サイクルを支えることで知られるME2が、この品質管理システムに影響を与えるかどうかを調べました。
ME2が失われるとミトコンドリア清掃が過剰に進む
ミトファジー活性を報告するよう設計されたヒト細胞株を用いて、研究者らはME2のレベルを低下させ、その結果を観察しました。するとParkinのミトコンドリアへの動員が著しく増加し、ミトファジーのマーカーも上昇して、より多くのミトコンドリアがタグ付けされ除去されていることが示されました。肝がん(HepG2)細胞では、ME2の欠失によりPINK1がミトコンドリアに蓄積し、主要なミトコンドリアタンパク質が消失することが見られ、活発な分解が起きていることと一致しました。顕微鏡観察ではミトコンドリアとオートファゴソームのマーカーの重なりが増え、損傷した発電所が通常よりも頻繁に細胞のリサイクル機構によって取り込まれていることが確認されました。
過剰な清掃は細胞のエネルギーシステムを弱める
適度なミトファジーは保護的ですが、過剰だと有害になり得ます。ME2を欠く肝がん細胞ではミトコンドリアが断片化しまばらになり、ATP産生が低下し、ミトコンドリアDNAのコピー数も減少しました。細胞はより多くの活性酸素を産生し、膜電位が低下するなど、ミトコンドリアがストレスあるいは機能不全に陥っている兆候を示しました。酸素消費量の測定では呼吸能力が著しく損なわれていました。機能的にはこれらの細胞は分裂速度が遅く、コロニー形成能が低下し、三次元培養での球状体も小さくなりました。薬剤でミトファジーを阻害するか、PINK1そのものをサイレンシングすると細胞増殖が部分的に回復し、増殖低下が過剰なミトコンドリア清掃に直接結びつくことが示されました。
ミトコンドリアの運命を決めるタンパク質の綱引き
ME2がこの過程をどのように制御するかを理解するため、研究チームはME2と物理的に結合するタンパク質を探し、PINK1の調節を助けるミトコンドリアの門番であるATAD3Aを同定しました。彼らはME2がATAD3Aに結合し、他のタンパク質に“廃棄せよ”シグナルを付けて細胞の分解機構へ送るTRIM25による分解からATAD3Aを保護することを示しました。ME2が存在しないとTRIM25がATAD3Aにより多くの標識を付け、その結果ATAD3Aが分解され、PINK1をミトコンドリア表面から除去する能力が低下します。その結果、PINK1が残存しミトファジーが急増し、ミトコンドリアが過剰に除去されます。重要なのは、触媒活性を失った変異型のME2であってもミトファジーを抑制したことから、ここで重要なのはME2の酵素活性ではなく、ATAD3Aに結合してTRIM25と競合する足場(スキャフォルド)としての役割であるという点です。
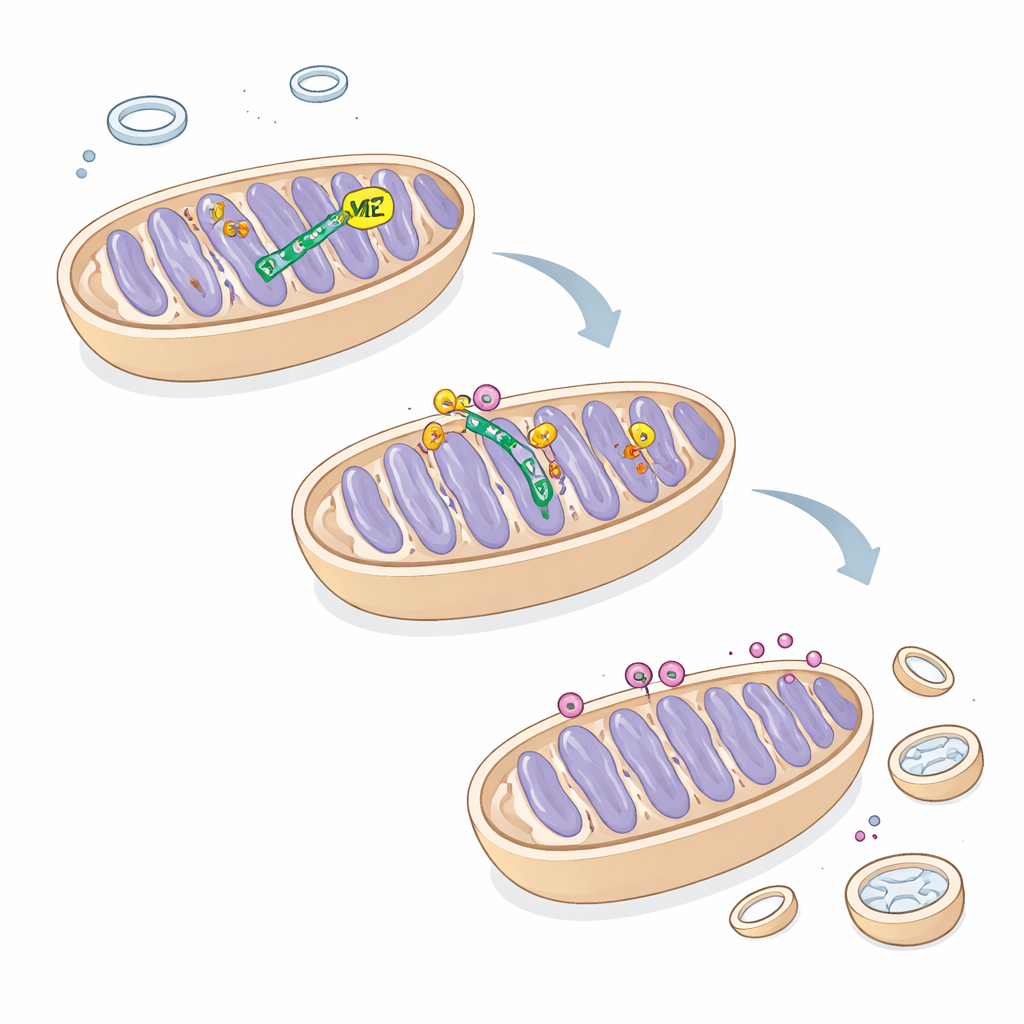
肝がんにおける増殖と清掃のバランスを取り戻す
TRIM25が過剰な細胞にME2を再導入すると、著者らはミトファジーを抑え、ミトコンドリアの形状と機能を改善し、細胞増殖を部分的に回復させることができました。これらの発見は、ME2がATAD3Aを保護してPINK1の適切なターンオーバーを可能にし、ミトコンドリアの清掃を制御するという新たな回路を明らかにします。一般向けに言えば、かつて単に燃料を燃やす助けをする酵素と考えられていたものが、ミトコンドリアを修復するか破壊するかのバランスを取る構造的な調節因子として機能することを示しています。肝がん細胞ではME2を失うことでこのバランスが崩れ、清掃システムが過剰に働いてエネルギー産生機構を奪い細胞増殖を遅らせる—これは将来的に新たな治療戦略に利用できる脆弱性となる可能性があります。
引用: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
キーワード: ミトファジー, ミトコンドリア, マリック酵素2, 肝臓がん, 細胞代謝