Clear Sky Science · sv
Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25
Varför de små kraftverken är viktiga för cancer
Varje cell i vår kropp är beroende av mitokondrierna, de små kraftstationerna som producerar energi. Celler reparerar och återvinner ständigt dessa strukturer, och när detta städningsarbete går fel kan det bidra till sjukdomar som cancer och neurodegeneration. Denna studie undersöker hur ett metabolismenzym kallat malic enzyme 2 (ME2), länge känt för sin roll i energiproduktion, oväntat fungerar som en slags trafikpolis för mitokondriell städning i levercancerceller — det ändrar hur snabbt skadade mitokondrier avlägsnas och hur väl tumörceller kan växa.
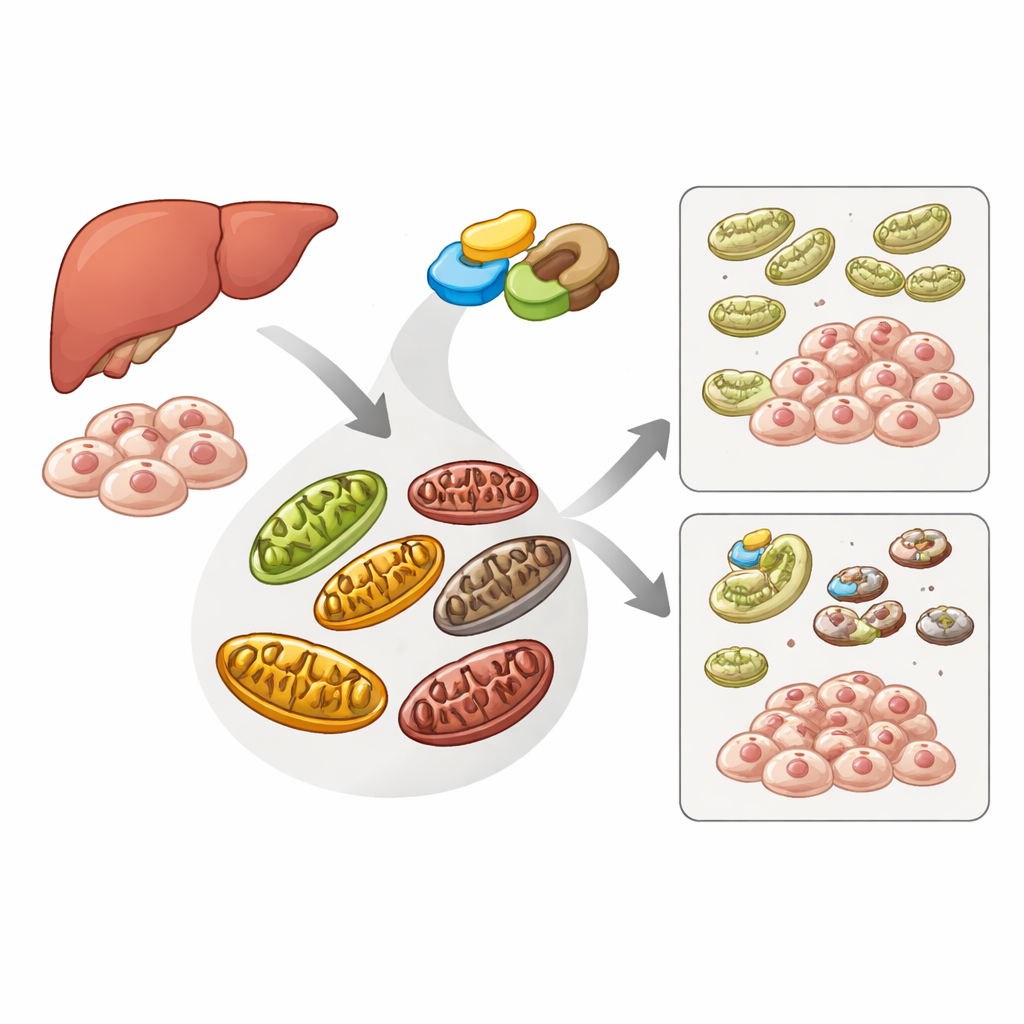
Cellens städpatrull för skadade kraftstationer
Celler använder en specialiserad återvinningsväg, mitofagi, för att identifiera och avlägsna skadade mitokondrier innan de skadar cellen. Ett sensorprotein kallat PINK1 och ett hjälpprotein kallat Parkin står i centrum för denna väg: när mitokondrier är ohälsosamma ansamlas PINK1 på deras yta, rekryterar Parkin, och tillsammans markerar de det felande organellen för nedbrytning. Ett annat protein, ATAD3A, hjälper normalt till att föra in PINK1 i mitokondrierna så att det kan brytas ner, vilket förhindrar onödig städning. Författarna ville ta reda på om ME2, mest känt för att stödja cellens huvudsakliga energigenererande cykel, också påverkar detta kvalitetskontrollsystem.
När ME2 försvinner går mitokondriell städning på högvarv
Med hjälp av humana cellinjer konstruerade för att rapportera mitofagiaktivitet minskade forskarna ME2-nivåerna och observerade vad som hände. De såg en påtaglig ökning i rekryteringen av Parkin till mitokondrierna och ett hopp i markörer för mitofagi, vilket indikerar att fler mitokondrier markerades och avlägsnades. I levercancerceller (HepG2) orsakade förlust av ME2 att PINK1 ackumulerades på mitokondrierna samtidigt som viktiga mitokondriella proteiner försvann, i linje med aktiv nedbrytning. Mikroskopi visade mer överlappning mellan mitokondrier och autofagosom-markörer, vilket bekräftar att skadade kraftstationer slukades av cellens återvinningsmaskineri mycket oftare än normalt.
För mycket städning försvagar cellens energisystem
Medan viss mitofagi är skyddande kan för mycket vara skadligt. I ME2-depleterade levercancerceller blev mitokondrierna fragmenterade och glesa, ATP-produktionen sjönk och antalet kopior av mitokondrie-DNA föll. Cellerna producerade fler reaktiva syremolekyler och hade lägre membranpotential, båda tecken på stressade eller sviktande mitokondrier. Mätningar av syreförbrukning visade att deras respiratoriska kapacitet var kraftigt nedsatt. Funktionellt delade sig dessa celler långsammare, bildade färre kolonier och genererade mindre tredimensionella sfärer. Att blockera mitofagi med läkemedel eller tysta sensorn PINK1 delvis räddade celltillväxten, vilket kopplar ihop den avmattade proliferation direkt till överaktiv mitokondriell städning.
En protein-dragningskraft som avgör mitokondriernas öde
För att förstå hur ME2 kontrollerar denna process sökte teamet efter proteiner som fysiskt binder till det och identifierade ATAD3A, den mitokondriella grindvakt som hjälper till att reglera PINK1. De visade att ME2 binder ATAD3A och skyddar det från nedbrytning av TRIM25, ett protein som märker andra proteiner med små "släng mig"-signaler för nedbrytning av cellens proteinnedbrytningsmaskineri. När ME2 saknades fäste TRIM25 fler märken på ATAD3A, vilket ledde till dess nedbrytning och minskad förmåga att rensa bort PINK1 från mitokondriens yta. Som ett resultat dröjde PINK1 kvar, mitofagin sköt i höjden och mitokondrier avlägsnades i överkant. Viktigt är att även mutantvarianter av ME2 som saknade katalytisk aktivitet fortfarande begränsade mitofagin, vilket indikerar att dess scaffold-rollen — att hålla i ATAD3A och konkurrera med TRIM25 — är det som spelar roll här, inte dess katalys.
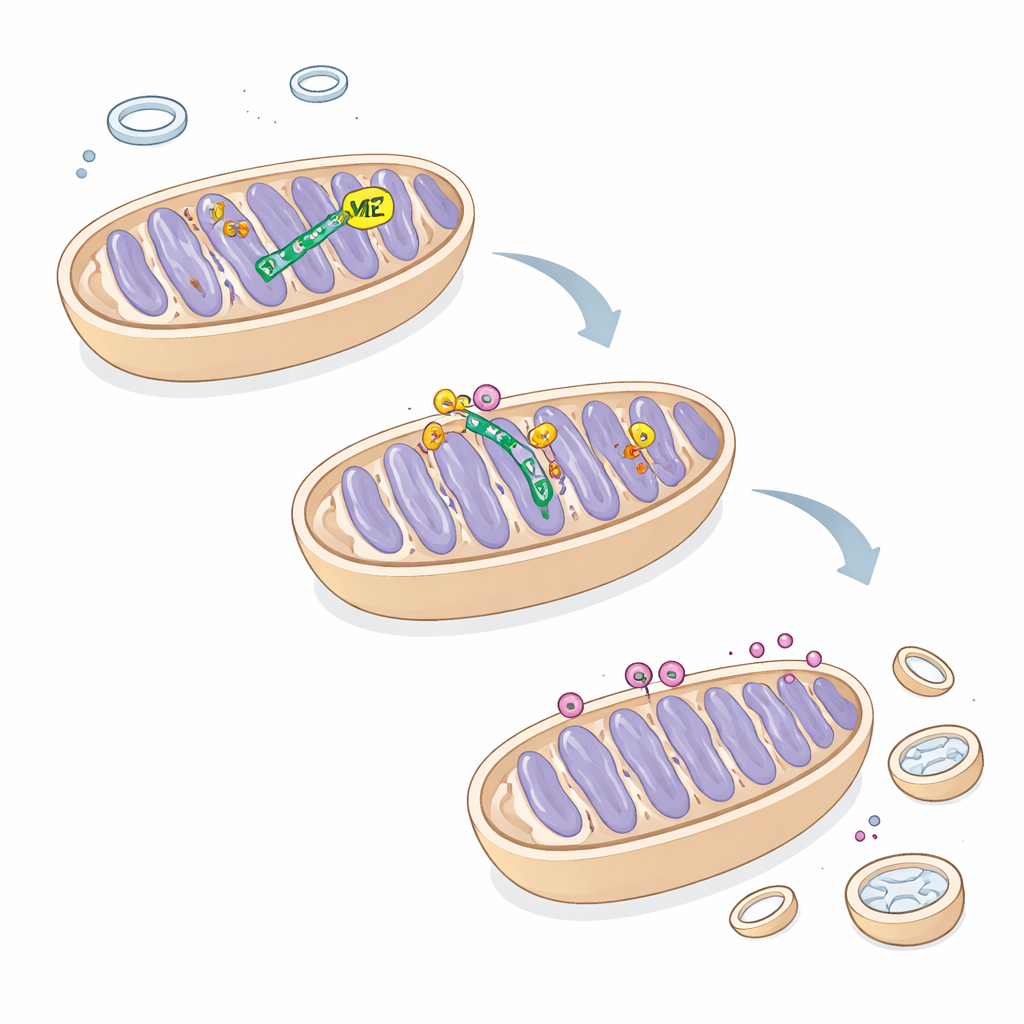
Återbalansering av tillväxt och städning i levercancer
Genom att återställa ME2 i celler överbelastade med TRIM25 kunde författarna dämpa mitofagin, förbättra mitokondriernas form och funktion och delvis återställa cellproliferation. Dessa fynd avslöjar en tidigare dold krets där ME2 skyddar ATAD3A, möjliggör korrekt PINK1-omsättning och håller mitokondriell städning i schack. För en allmän läsare är budskapet att ett enzym som tidigare antogs enbart hjälpa till att förbränna bränsle också fungerar som en strukturell reglerare som balanserar när mitokondrier repareras kontra förstörs. I levercancerceller skjuter förlust av ME2 denna balans mot överdriven städning, vilket berövar cellerna deras energiproducerande maskineri och bromsar deras tillväxt — en sårbarhet som en dag skulle kunna utnyttjas för nya terapier.
Citering: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
Nyckelord: mitofagi, mitokondrier, malic enzyme 2, levercancer, cellmetabolism