Clear Sky Science · ru
Малатдегидрогеназа 2 подавляет митофагию, опосредованную PINK1-Parkin, стабилизируя ATAD3A через конкурентное взаимодействие с TRIM25
Почему крошечные энергостанции важны при раке
Каждая клетка в нашем организме зависит от митохондрий — крошечных энергетических станций, вырабатывающих энергию. Клетки постоянно ремонтируют и утилизируют эти структуры, и когда процесс очистки нарушается, это может способствовать развитию таких заболеваний, как рак и нейродегенерация. В этом исследовании рассматривается, как метаболический фермент малатдегидрогеназа 2 (ME2), давно известный своей ролью в энергетическом обмене, неожиданно выступает в роли регулировщика митохондриальной очистки в клетках рака печени — меняя скорость удаления повреждённых митохондрий и способность опухолевых клеток к росту.
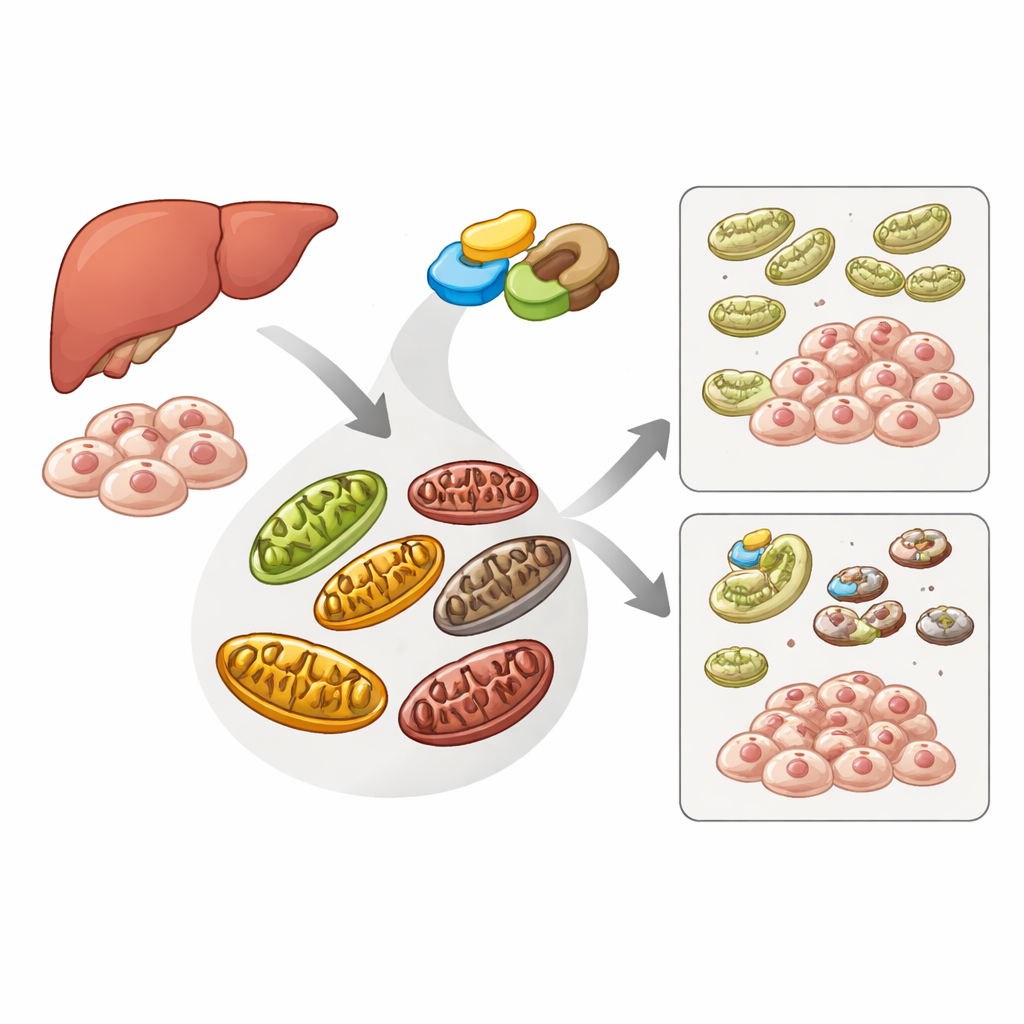
Команда очистки клетки для повреждённых энергостанций
Клетки используют специализированный путь утилизации — митофагию — чтобы обнаруживать и удалять повреждённые митохондрии до того, как они нанесут вред клетке. Датчик PINK1 и вспомогательный белок Parkin находятся в центре этого пути: когда митохондрии нездоровы, PINK1 накапливается на их поверхности, привлекает Parkin, и вместе они маркируют повреждённый органелл для уничтожения. Другой белок, ATAD3A, обычно помогает транспортировать PINK1 в митохондрии для его разрушающего расщепления, предотвращая излишнюю очистку. Авторы поставили цель выяснить, влияет ли ME2, известный прежде всего как участник основного энергетического цикла клетки, на эту систему контроля качества.
При потере ME2 митохондриальная очистка ускоряется
Используя человеческие клеточные линии с отчётными системами активности митофагии, исследователи снизили уровень ME2 и наблюдали за последствиями. Они обнаружили заметное увеличение привлечения Parkin к митохондриям и рост маркеров митофагии, что указывает на то, что больше митохондрий маркировалось и удалялось. В клетках рака печени (HepG2) потеря ME2 вызвала накопление PINK1 на митохондриях при одновременном исчезновении ключевых митохондриальных белков, что согласуется с активным их разрушением. Микроскопия показала большую степень наложения между митохондриями и маркерами аутофагосом, подтверждая, что повреждённые энергостанции гораздо чаще захватываются системой утилизации клетки.
Чрезмерная очистка ослабляет энергетическую систему клетки
Хотя некоторая митофагия защищает клетку, её избыток может быть вреден. В клетках рака печени с дефицитом ME2 митохондрии фрагментировались и редели, выработка АТФ снизилась, а копий митохондриальной ДНК стало меньше. Клетки производили больше реактивных кислородных частиц и имели пониженный мембранный потенциал — признаки стресса или отказа митохондрий. Измерения потребления кислорода показали значительное снижение их респираторной ёмкости. Функционально такие клетки делились медленнее, образовывали меньше колоний и давали более мелкие трёхмерные шарики. Блокирование митофагии препаратами или инактивация самого датчика PINK1 частично восстанавливали рост клеток, связывая замедление пролиферации напрямую с чрезмерной митофагией.
Белковая схватка, решающая судьбу митохондрий
Чтобы понять, как ME2 контролирует этот процесс, команда искала белки, физически взаимодействующие с ним, и выявила ATAD3A — митохондриальную «шлюзовую» молекулу, помогающую регулировать PINK1. Они показали, что ME2 связывается с ATAD3A и защищает его от уничтожения со стороны TRIM25, белка, который метит другие белки маленькими «метками на уничтожение» для утилизации клеточной системой разрушения белков. При отсутствии ME2 TRIM25 чаще присоединял такие метки к ATAD3A, что приводило к его деградации и снижению способности удалять PINK1 с поверхности митохондрий. В результате PINK1 задерживался, митофагия усиливалась, и митохондрии удалялись в избытке. Важно, что даже мутантные формы ME2 без каталитической активности по-прежнему сдерживали митофагию, что указывает на то, что здесь важно его каркасное (скелетное) свойство — удержание ATAD3A и конкуренция с TRIM25 — а не ферментативная функция.
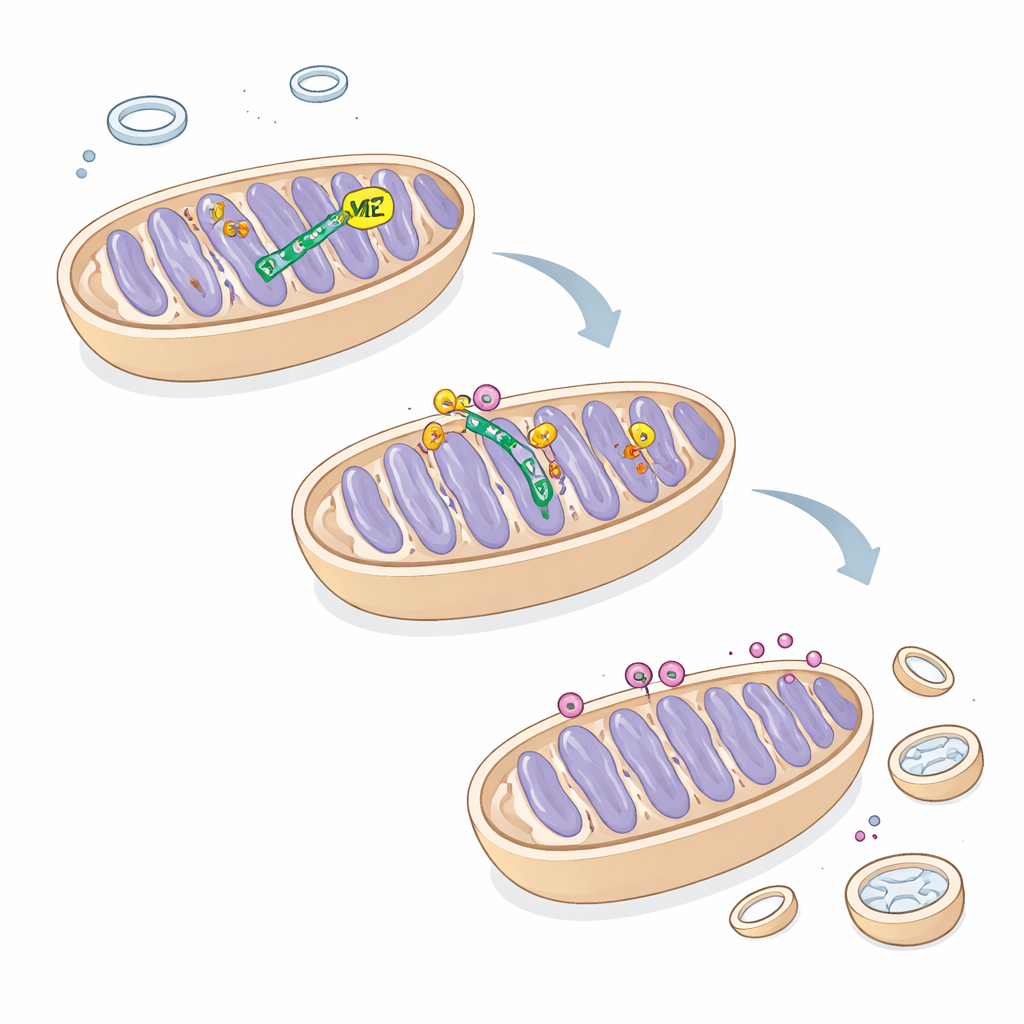
Восстановление баланса между ростом и очисткой при раке печени
Восстановив экспрессию ME2 в клетках с избытком TRIM25, авторы смогли снизить митофагию, улучшить форму и функцию митохондрий и частично вернуть пролиферацию клеток. Эти результаты выявляют ранее скрытую цепочку, в которой ME2 защищает ATAD3A, обеспечивая корректную утилизацию PINK1 и удерживая митохондриальную очистку под контролем. Для неспециалиста вывод таков: фермент, считавшийся прежде просто участником сжигания топлива, также действует как структурный регулятор, балансирующий между ремонтом и уничтожением митохондрий. В клетках рака печени нарушение этого баланса при потере ME2 переводит систему очистки в режим «аварийного удаления», лишая клетки энергетического аппарата и замедляя их рост — уязвимость, которую потенциально можно будет использовать в терапевтических целях.
Цитирование: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
Ключевые слова: митофагия, митохондрии, малатдегидрогеназа 2, рак печени, клеточный метаболизм