Clear Sky Science · fr
L’enzyme malique 2 supprime la mitophagie médiée par PINK1-Parkin en stabilisant ATAD3A via une interaction compétitive avec TRIM25
Pourquoi les minuscules centrales électriques importent en cancérologie
Toutes les cellules de notre corps dépendent des mitochondries, ces petites centrales qui produisent l’énergie. Les cellules réparent et recyclent en permanence ces structures, et lorsque ce processus d’entretien dysfonctionne, il peut contribuer à des maladies comme le cancer et les maladies neurodégénératives. Cette étude examine comment une enzyme métabolique appelée enzyme malique 2 (ME2), connue de longue date pour son rôle dans la production d’énergie, agit de manière inattendue comme un régulateur du nettoyage mitochondrial dans les cellules du cancer du foie — modulant la vitesse d’élimination des mitochondries endommagées et la capacité des cellules tumorales à se développer.
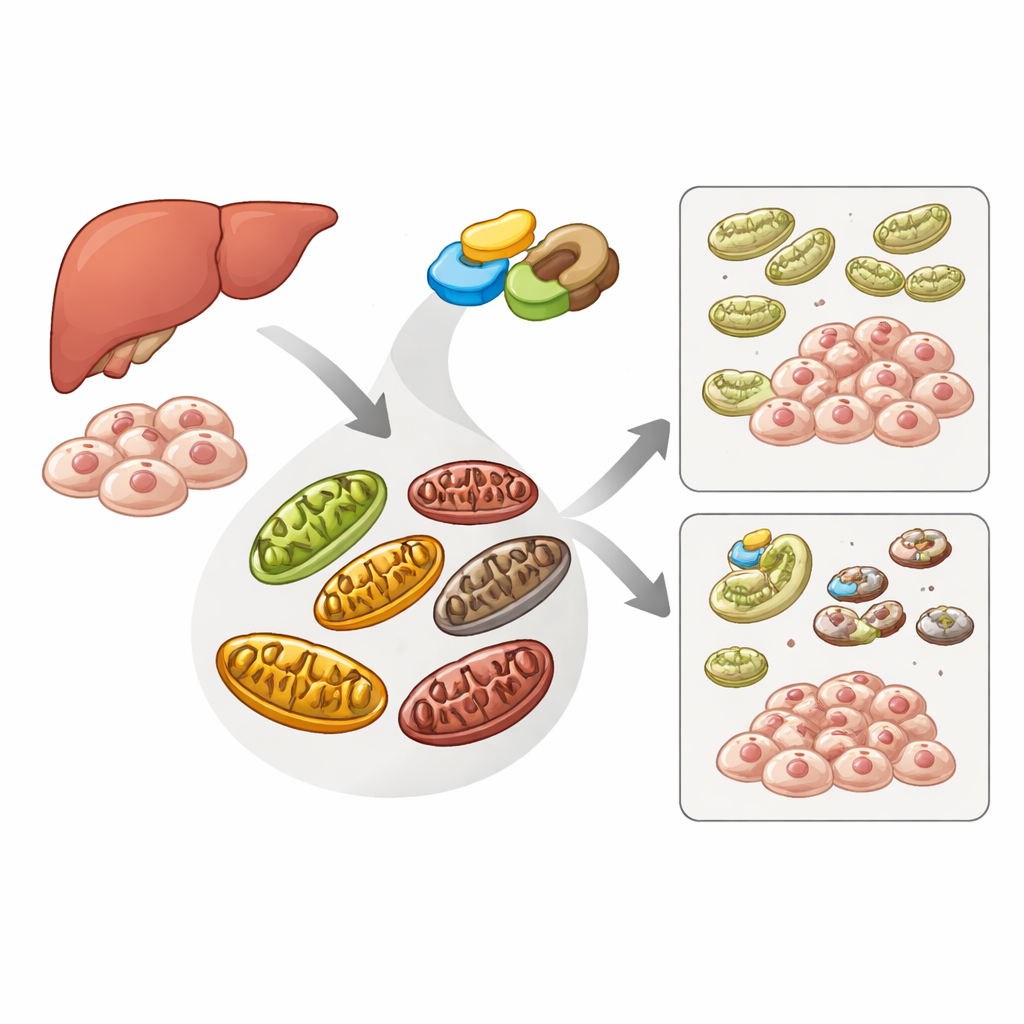
L’équipe de nettoyage d’une cellule pour les centrales endommagées
Les cellules utilisent une voie de recyclage spécialisée, la mitophagie, pour identifier et éliminer les mitochondries endommagées avant qu’elles n’endommagent la cellule. Une protéine détectrice appelée PINK1 et une protéine auxiliaire appelée Parkin sont au cœur de cette voie : lorsque les mitochondries sont en mauvais état, PINK1 s’accumule à leur surface, attire Parkin, et ensemble elles marquent l’organite défectueux pour destruction. Une autre protéine, ATAD3A, facilite normalement le transport de PINK1 vers l’intérieur des mitochondries afin qu’il soit dégradé, évitant un nettoyage inutile. Les auteurs ont cherché à déterminer si ME2, surtout connue pour soutenir le principal cycle de production d’énergie de la cellule, influence aussi ce système de contrôle qualité.
Lorsque ME2 disparaît, le nettoyage mitochondrial s’emballe
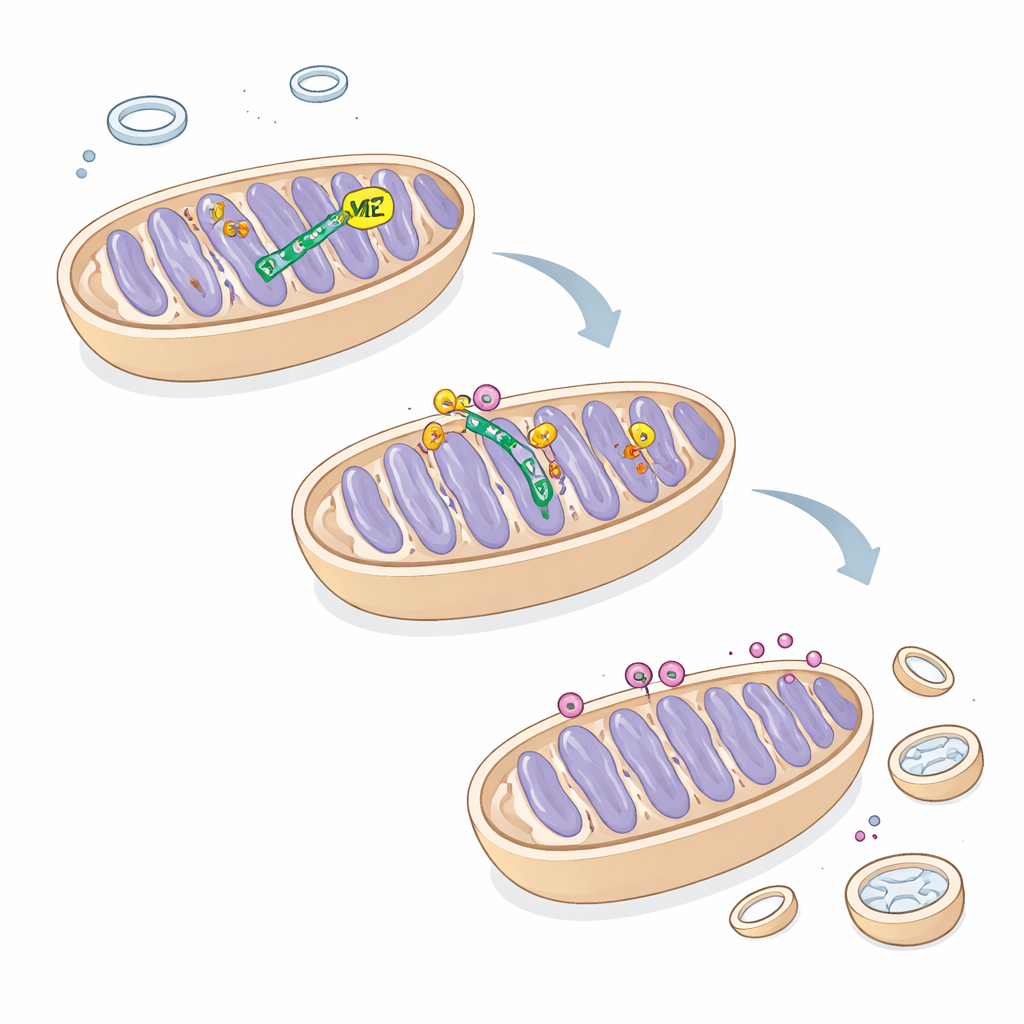
En utilisant des lignées cellulaires humaines conçues pour reporter l’activité de la mitophagie, les chercheurs ont réduit les niveaux de ME2 et observé les conséquences. Ils ont constaté une augmentation marquée du recrutement de Parkin vers les mitochondries et une hausse des marqueurs de mitophagie, indiquant que davantage de mitochondries étaient marquées et éliminées. Dans des cellules de cancer du foie (HepG2), la perte de ME2 provoquait l’accumulation de PINK1 sur les mitochondries tandis que des protéines mitochondriales clés disparaissaient, conforme à une dégradation active. La microscopie a montré un recouvrement plus important entre mitochondries et marqueurs d’autophagosomes, confirmant que les centrales endommagées étaient englouties par la machinerie de recyclage de la cellule beaucoup plus fréquemment que la normale.
Trop de nettoyage affaiblit le système énergétique de la cellule
Si une certaine mitophagie est protectrice, un excès peut être délétère. Dans les cellules de cancer du foie appauvries en ME2, les mitochondries devenaient fragmentées et clairsemées, la production d’ATP chutait et le nombre de copies d’ADN mitochondrial diminuait. Les cellules produisaient davantage de molécules réactives et présentaient un potentiel de membrane réduit, deux signes de mitochondries stressées ou défaillantes. Les mesures de consommation d’oxygène ont révélé une capacité respiratoire significativement altérée. Sur le plan fonctionnel, ces cellules se divisaient plus lentement, formaient moins de colonies et produisaient des sphères tridimensionnelles plus petites. Bloquer la mitophagie avec des médicaments, ou silencer le détecteur PINK1 lui-même, a partiellement restauré la croissance cellulaire, reliant directement le ralentissement de la prolifération à une activité de nettoyage mitochondriale excessive.
Une lutte de protéines qui décide du sort des mitochondries
Pour comprendre comment ME2 contrôle ce processus, l’équipe a recherché des protéines qui s’associent physiquement à ME2 et a identifié ATAD3A, la porte mitochondriale qui aide à réguler PINK1. Ils ont montré que ME2 se lie à ATAD3A et le protège de la destruction par TRIM25, une protéine qui ajoute aux cibles de petits signaux « jette-moi » pour leur élimination par la machinerie de dégradation des protéines de la cellule. En l’absence de ME2, TRIM25 ajoutait davantage d’étiquettes à ATAD3A, entraînant sa dégradation et une moindre capacité à éliminer PINK1 de la surface mitochondriale. En conséquence, PINK1 persistait, la mitophagie augmentait et les mitochondries étaient éliminées de manière excessive. Fait important, même des versions mutantes de ME2 dépourvues d’activité catalytique restreignaient la mitophagie, indiquant que c’est son rôle d’échafaudage — maintenir ATAD3A et entrer en compétition avec TRIM25 — qui importe ici, et non son activité enzymatique.
Rééquilibrer croissance et nettoyage dans le cancer du foie
En restaurant ME2 dans des cellules surchargées en TRIM25, les auteurs ont pu atténuer la mitophagie, améliorer la forme et la fonction mitochondriales, et partiellement rétablir la prolifération cellulaire. Ces résultats révèlent un circuit jusqu’alors caché dans lequel ME2 protège ATAD3A, permettant un turnover adéquat de PINK1 et maintenant le nettoyage mitochondrial sous contrôle. Pour un lecteur non spécialiste, le message est qu’une enzyme autrefois considérée comme simple aide énergétique joue aussi un rôle structural qui équilibre la réparation et la destruction des mitochondries. Dans les cellules du cancer du foie, la perturbation de cet équilibre par la perte de ME2 pousse le système de nettoyage en surrégime, dépouillant les cellules de leur machinerie de production d’énergie et ralentissant leur croissance — une vulnérabilité qui pourrait un jour être exploitée pour de nouvelles thérapies.
Citation: Liu, Q., Su, L., Wei, X. et al. Malic enzyme 2 suppresses PINK1-Parkin-mediated mitophagy by stabilizing ATAD3A via competitive interaction with TRIM25. Cell Death Dis 17, 353 (2026). https://doi.org/10.1038/s41419-026-08623-2
Mots-clés: mitophagie, mitochondries, enzyme malique 2, cancer du foie, métabolisme cellulaire