Clear Sky Science · zh
识别与食管腺癌患者生存相关的异构体转换事件,提示新的预后和治疗靶点
这项研究为何重要
食管腺癌是一种食管的癌症,发病率逐渐上升,但生存率仍然很低。现有筛查方法常常漏检高风险人群,化疗和手术等标准治疗仅对少部分患者有效。这项研究提出了一个新问题:与其只关注肿瘤中哪些基因被打开或关闭,不如更仔细地看这些基因使用的是哪些版本?通过聚焦这些“发生切换”的基因版本,研究者发现了新的不良生存预警信号,并指向可能减少对正常细胞损害的治疗策略。
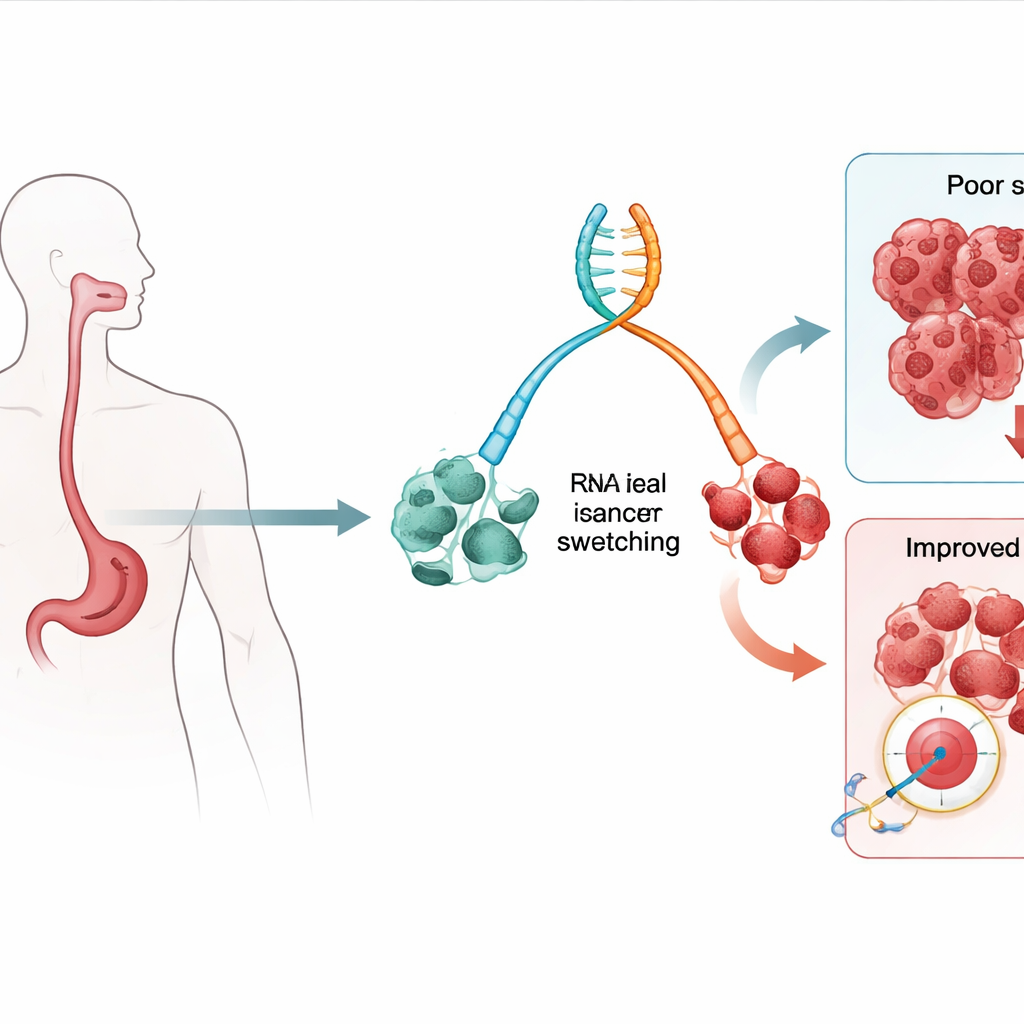
基因信息的变化作为早期警示
我们的基因可以从同一段 DNA 产生多个略有不同的信息,称为异构体。研究团队分析了来自巴雷特食管(已知的癌前状态)和已发展为食管腺癌患者的组织样本中的 RNA——携带这些信息的分子。他们寻找异构体“切换”,即在组织从低风险的巴雷特向高风险病变和癌变进展时,某一基因的一个版本变得更常见而另一个变得更少见。通过将这些切换与患者结局关联的统计模型,研究者鉴定出数十个其存在或缺失与全因死亡率及癌症相关死亡率升高相关的异构体。
两种预示危险的基因版本
在发现的众多异构体中,有两种尤为突出:分别属于 TTLL12 和 HM13 基因的特定版本。这些特定版本在高级别的癌前病变和癌组织中比在低级别巴雷特组织中更常见,依赖这些异构体的肿瘤患者通常预后较差。重要的是,TTLL12 和 HM13 基因的总体表达水平并不能完全说明这一点;真正发出警示的是向这些特定异构体的转换。研究者不仅在患者样本中确认了这些模式,还在反流驱动的食管癌大鼠模型和独立的人类癌症数据集中得到了验证,表明这些发现具有稳健性和生物学意义。
将有害异构体反过来针对癌症
为了测试这些异构体是标志还是疾病的驱动因子,科学家在两种体外培养的食管癌细胞系中,使用小型 RNA 工具选择性沉默了 TTLL12 和 HM13 的高风险版本。抑制任一异构体都显著减缓了癌细胞的生长并降低了其迁移能力——这是扩散的关键一步——而对正常食管细胞的影响很小。更引人注目的是,当这些异构体被沉默时,常规化疗药物(紫杉醇和卡铂)的疗效增强,与异构体敲低联用呈协同效应,远比单独使用任一方法杀死更多癌细胞。
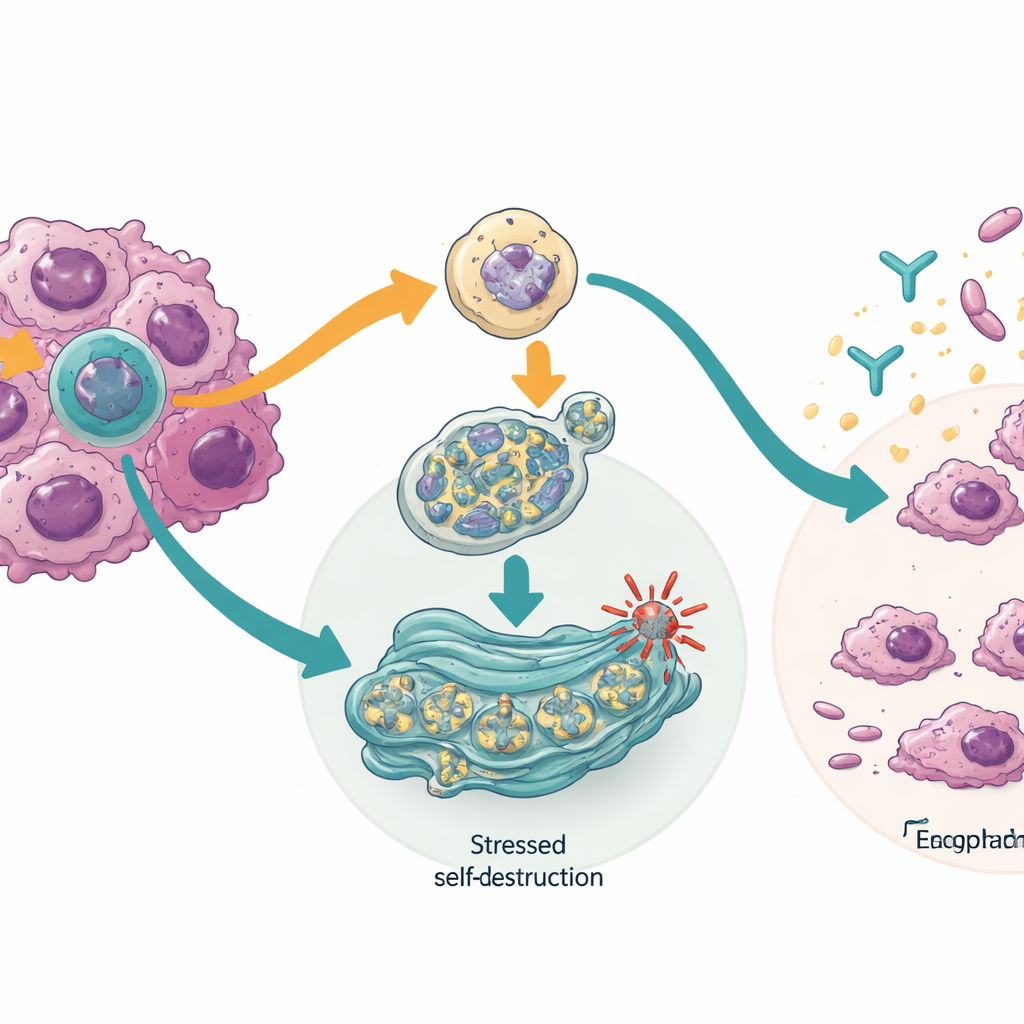
癌细胞如何被推向自我毁灭
深入机制研究发现,阻断 TTLL12 异构体会激活细胞内一种称为伴侣介导自噬的质控系统,该系统有助于分解受损或有害的蛋白质。在癌细胞中,其激活降低了有助于肿瘤在 DNA 损伤下生存的蛋白质水平,包括 CHK1 和突变形式的著名守护基因 TP53。另一方面,阻断 HM13 异构体会给细胞的蛋白折叠工厂——内质网施加压力,触发一条应激反应通路,该通路可暂停蛋白质合成、激活对有缺陷细胞器的回收,最终促使细胞进入程序性死亡。在某些癌细胞中,这一变化还使它们对针对 PD-L1 的免疫药物更为敏感,提示异构体切换可能有助于肿瘤逃避免疫监视。
这对患者可能意味着什么
综合来看,这些发现表明关注肿瘤使用哪些异构体,可能有助于医生更好地预测谁属于高危人群以及谁可能更好地响应特定治疗。这里强调的 TTLL12 和 HM13 的特定版本不仅是危险信号;它们似乎帮助癌细胞生存、迁移并抗药,但在实验室条件下可以在不显著伤害正常食管细胞的前提下被选择性靶向。尽管这项工作仍处于早期实验阶段,需要更大规模的患者研究,但它为未来监测异构体模式的检测以及旨在选择性关闭食管癌中最有害基因版本的新药或基于 RNA 的治疗打开了大门。
引用: Zhang, Y., Ntsiful, D.A., Israel, R. et al. Identification of isoform switching events linked with esophageal adenocarcinoma patient survival informs novel prognostic and therapeutic targets. Cell Death Dis 17, 305 (2026). https://doi.org/10.1038/s41419-026-08542-2
关键词: 食管癌, 巴雷特食管, RNA 异构体, 靶向治疗, 自噬