Clear Sky Science · ru
Выявление событий переключения изоформ, связанных с выживаемостью пациентов с аденокарциномой пищевода, определяет новые прогностические и терапевтические мишени
Почему это исследование важно
Аденокарцинома пищевода — тип рака пищевода, который становится более распространённым, но при этом сохраняет очень низкую выживаемость. Текущие скрининговые тесты часто не выявляют людей с повышенным риском, а стандартные методы лечения, такие как химиотерапия и хирургия, помогают лишь части пациентов. В этом исследовании задан новый вопрос: вместо того чтобы смотреть только на то, какие гены включены или выключены в опухолях, что если внимательнее исследовать, какие версии этих генов используются? Сосредоточившись на этих «переключившихся» вариантах, исследователи обнаружили новые признаки плохого прогноза и указали на потенциальные стратегии терапии, которые могли бы щадить здоровые клетки.
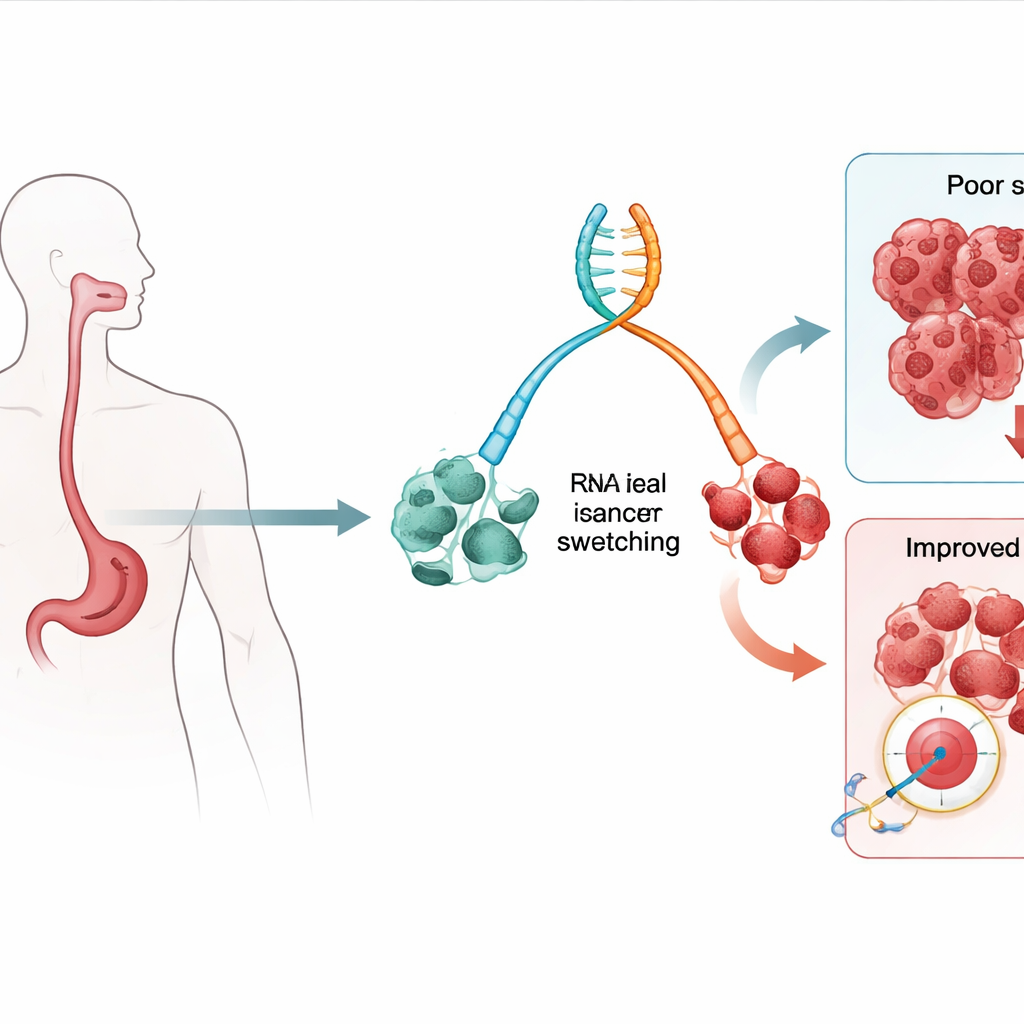
Сдвиги в генетических сообщениях как ранние предупреждающие признаки
Наши гены могут производить несколько слегка различных сообщений, известных как изоформы, из одного и того же участка ДНК. Команда проанализировала РНК — молекулу, несущую эти сообщения — в образцах ткани от людей с пищеводом Барретта (известным предраковым состоянием) и от пациентов с уже развившейся аденокарциномой пищевода. Они искали «переключения» изоформ, когда одна версия гена становится более распространённой, а другая — менее распространённой по мере прогрессирования ткани от низкого риска Барретта к высокорисковым поражениям и раку. С помощью статистических моделей, связывающих эти переключения с исходами у пациентов, были выделены десятки изоформ, чье присутствие или отсутствие было связано с повышенным риском смерти — как по всем причинам, так и от рака в частности.
Две версии генов, предвещающие проблемы
Среди многих обнаруженных изоформ две оказались особенно заметными: определённые варианты генов TTLL12 и HM13. Эти конкретные изоформы чаще встречались в предраковых поражениях высокой степени и в опухолях, чем в тканях с низкой степенью поражения Барретта; пациенты, опухоли которых в значительной степени опирались на эти изоформы, как правило, имели более плохой прогноз. Важно, что общие уровни экспрессии генов TTLL12 и HM13 не рассказывали всей истории; именно сдвиг в пользу этих конкретных изоформ стал сигнальным маркером. Исследователи подтвердили эти закономерности не только в образцах пациентов, но и в модели рака пищевода у крыс, а также в независимом наборе данных по человеческим опухолям, что указывает на устойчивость и биологическую значимость результатов.
Обращение вредных изоформ против самой опухоли
Чтобы проверить, являются ли эти изоформы лишь маркерами или фактическими драйверами болезни, учёные использовали маленькие РНК-инструменты для селективного заглушения рискованных вариантов TTLL12 и HM13 в двух клеточных линиях рака пищевода, выращенных в лаборатории. Блокирование любой из этих изоформ резко снижало рост раковых клеток и замедляло их способность к миграции — ключевой шаг к распространению — при этом оказывая лишь незначительное влияние на нормальные клетки пищевода. Ещё более примечательно, что при заглушении изоформ стандартные препараты химиотерапии (паклитаксел и карбоплатин) становились более эффективными: в сочетании с подавлением изоформ они действовали синергетически, убивая намного больше раковых клеток, чем каждая стратегия по отдельности.
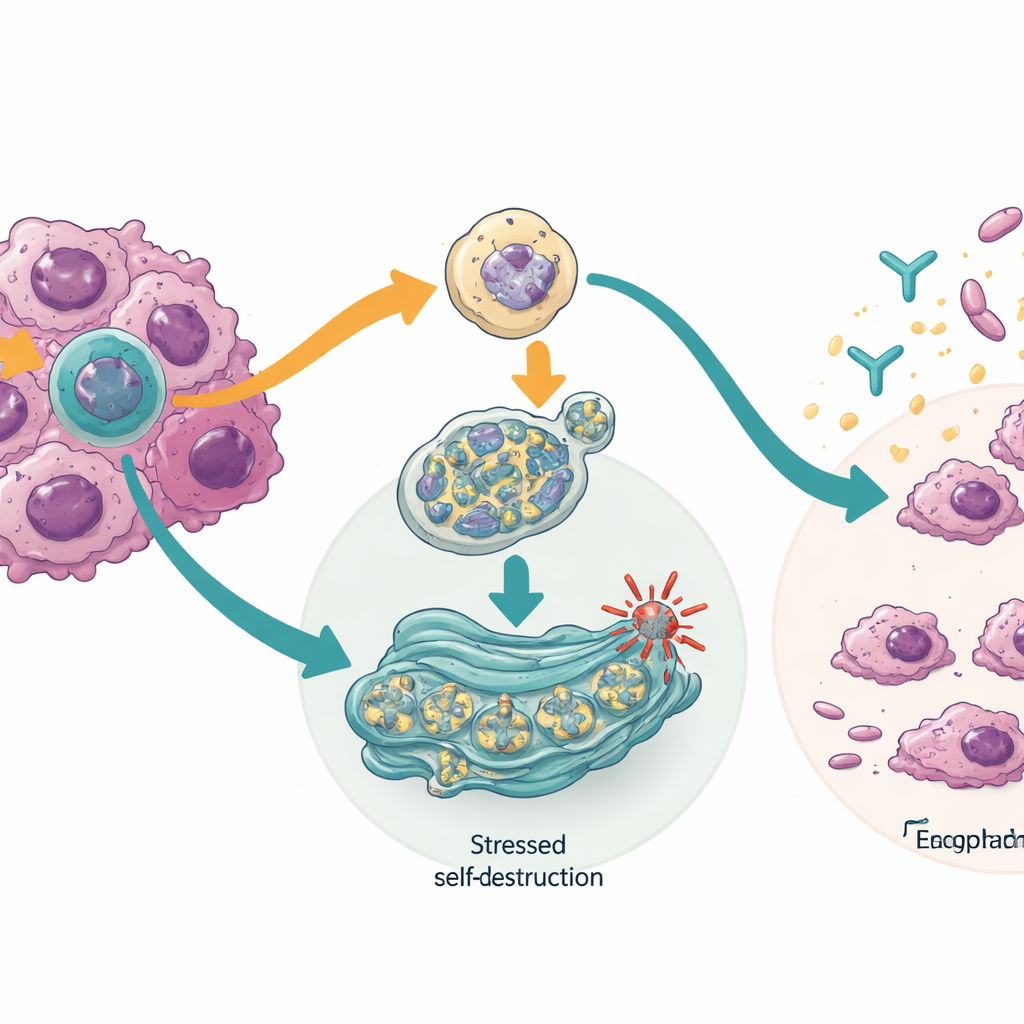
Как раковые клетки заставляют себя самоуничтожаться
Изучая механизмы действия, команда обнаружила, что блокирование изоформы TTLL12 включает систему контроля качества внутри клетки, называемую шаперон-опосредованной аутопагией. Эта система помогает разрушать повреждённые или опасные белки. В раковых клетках её активация снижала уровни белков, которые помогают опухолям переживать повреждение ДНК, включая CHK1 и мутантные формы хорошо известного гена-стража TP53. Блокирование изоформы HM13, напротив, вызывало стресс в белково-сворачивающем аппарате клетки — эндоплазматическом ретикулуме, активируя сигнальные пути, которые могут остановить синтез белка, запустить переработку повреждённых клеточных компонентов и в конечном итоге привести клетку к программируемой гибели. В некоторых раковых клетках эти изменения также делали их более уязвимыми к иммунной терапии, нацеленой на PD-L1, что говорит о том, что переключение изоформ может помогать опухолям скрываться от иммунной системы.
Что это может означать для пациентов
Вместе эти результаты говорят о том, что внимание к тому, какие изоформы использует опухоль, может улучшить способность врачей предсказывать, кто находится в наивысшей группе риска и кто лучше ответит на определённые виды лечения. Конкретные версии TTLL12 и HM13, выделенные в этом исследовании, делают больше, чем просто сигнализируют об опасности: они, по-видимому, помогают раковым клеткам выживать, двигаться и сопротивляться терапии, но при этом могут быть нацелены без значительного вреда для нормальных клеток пищевода в лабораторных условиях. Хотя эта работа всё ещё находится на ранней экспериментальной стадии и требуются более крупные клинические исследования, она открывает путь к будущим тестам, отслеживающим паттерны изоформ, а также к разработке новых лекарств или РНК-ориентированных терапий, предназначенных для избирательного подавления самых вредных версий генов при раке пищевода.
Цитирование: Zhang, Y., Ntsiful, D.A., Israel, R. et al. Identification of isoform switching events linked with esophageal adenocarcinoma patient survival informs novel prognostic and therapeutic targets. Cell Death Dis 17, 305 (2026). https://doi.org/10.1038/s41419-026-08542-2
Ключевые слова: рак пищевода, пищевод Барретта, РНК-изоформы, таргетная терапия, аутфагия