Clear Sky Science · de
Identifizierung von Isoform‑Wechselereignissen, die mit dem Überleben von Patienten mit ösophagealem Adenokarzinom verbunden sind, weist auf neue prognostische und therapeutische Ziele hin
Warum diese Forschung wichtig ist
Das ösophageale Adenokarzinom ist eine Krebsform der Speiseröhre, die immer häufiger auftritt, aber nach wie vor eine sehr niedrige Überlebensrate hat. Aktuelle Screening‑Tests übersehen oft Menschen mit Risiko, und Standardbehandlungen wie Chemotherapie und Operation helfen nur einem Teil der Patientinnen und Patienten. Diese Studie stellt eine neue Frage: Anstatt nur zu betrachten, welche Gene in Tumoren an- oder ausgeschaltet sind, wird genauer hingeschaut, welche Versionen dieser Gene verwendet werden. Indem die Forscher auf diese „umgeschalteten“ Versionen achten, entdecken sie neue Warnsignale für schlechte Überlebensaussichten und weisen auf mögliche Behandlungsstrategien hin, die gesunde Zellen weitgehend schonen könnten.
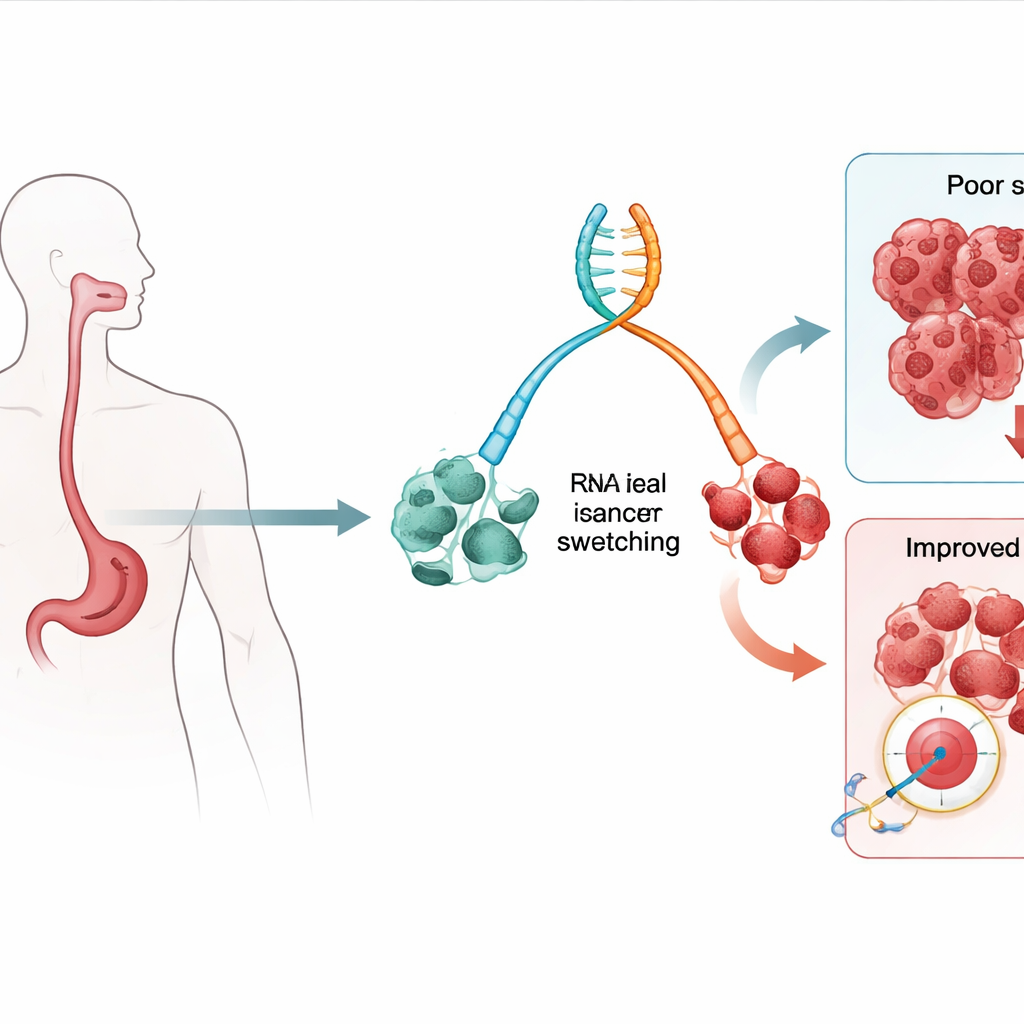
Verschiebungen in Genbotschaften als Frühwarnzeichen
Unsere Gene können mehrere leicht unterschiedliche Botschaften hervorbringen, sogenannte Isoforme, aus demselben DNA‑Abschnitt. Das Team untersuchte RNA, das Molekül, das diese Botschaften trägt, aus Gewebeproben von Personen mit Barrett‑Ösophagus (einer bekannten Präkanzerose) und von Patienten mit bereits entwickeltem ösophagealem Adenokarzinom. Sie suchten nach Isoform‑„Switches“, bei denen eine Genvariante mit der Progression von niedrig‑risikigem Barrett‑Gewebe zu hohem Risiko und Krebs häufiger wird, während eine andere seltener wird. Mithilfe statistischer Modelle, die diese Wechsel mit dem Patientenoutcome verknüpfen, identifizierten sie Dutzende von Isoformen, deren Vorhandensein oder Fehlen mit erhöhten Sterberisiken sowohl insgesamt als auch krebsspezifisch verbunden war.
Zwei Genvarianten mit problematischer Bedeutung
Unter den vielen entdeckten Isoformen hoben sich zwei besonders hervor: bestimmte Varianten der Gene TTLL12 und HM13. Diese spezifischen Isoforme kamen in hochgradigen präkanzerösen Läsionen und in Tumoren häufiger vor als in niedriggradigem Barrett‑Gewebe, und Patienten, deren Tumoren stark auf diese Isoforme setzten, hatten tendenziell ein schlechteres Überleben. Wichtig ist, dass die Gesamtmenge der TTLL12‑ und HM13‑Genexpression die Lage nicht vollständig erklärte; ausschlaggebend war der Wechsel hin zu genau diesen Isoformen. Die Forscher bestätigten diese Muster nicht nur in Patientenproben, sondern auch in einem Rattenmodell für refluxgetriebenen Speiseröhrenkrebs und in einem unabhängigen menschlichen Krebsdatensatz, was darauf hindeutet, dass die Ergebnisse robust und biologisch relevant sind.
Schädliche Isoforme gegen den Krebs einsetzen
Um zu prüfen, ob diese Isoforme nur Marker oder tatsächliche Treiber der Krankheit sind, verwendeten die Wissenschaftler kleine RNA‑Werkzeuge, um die riskanten Varianten von TTLL12 und HM13 selektiv in zwei in Kultur gehaltenen Speiseröhrenkrebs‑Zelllinien zu deaktivieren. Das Blockieren jeder der Isoforme reduzierte das Krebszellwachstum deutlich und verlangsamte ihre Wanderungsfähigkeit — ein wichtiger Schritt der Metastasierung — während normale Speiseröhrenzellen nur geringfügig betroffen waren. Noch bemerkenswerter war, dass durch das Abschalten der Isoforme Standard‑Chemotherapeutika (Paclitaxel und Carboplatin) wirksamer wurden und synergistisch mit der Herunterregulierung zusammenwirkten, sodass deutlich mehr Krebszellen abgetötet wurden als durch eine der Maßnahmen allein.
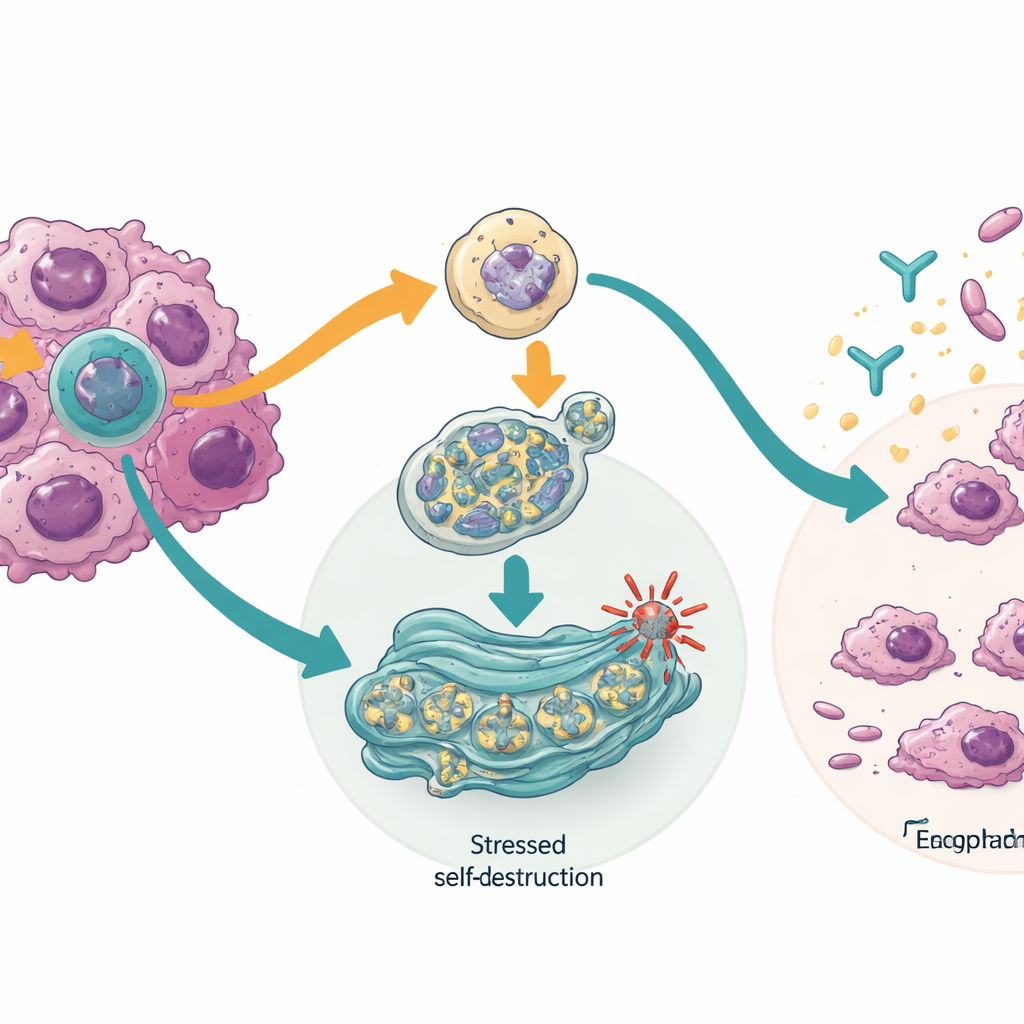
Wie die Krebszellen zur Selbstzerstörung getrieben werden
Bei der Untersuchung der zugrundeliegenden Mechanismen fanden die Forschenden heraus, dass das Blockieren der TTLL12‑Isoform ein intrazelluläres Qualitätskontrollsystem namens chaperonvermittelte Autophagie aktivierte. Dieses System hilft dabei, beschädigte oder gefährliche Proteine abzubauen. In den Krebszellen senkte seine Aktivierung die Spiegel von Proteinen, die Tumoren beim Überleben nach DNA‑Schäden unterstützen, darunter CHK1 und mutierte Formen des bekannten Wächtergens TP53. Das Blockieren der HM13‑Isoform hingegen belastete das zelluläre Protein‑Faltungszentrum, das endoplasmatische Retikulum, und löste einen Antwortweg aus, der die Proteinproduktion stoppen, den Recyclingprozess fehlerhafter Zellbestandteile aktivieren und schließlich den programmierten Zelltod auslösen kann. In einigen Krebszellen machte diese Veränderung sie zudem anfälliger für ein immunbasiertes Medikament, das PD‑L1 anvisiert, was darauf hindeutet, dass Isoformwechsel Tumoren helfen können, sich dem Immunsystem zu entziehen.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt deuten diese Befunde darauf hin, dass die Beachtung der Isoformen, die ein Tumor nutzt, die Vorhersage verbessern könnte, wer das höchste Risiko trägt und wer am besten auf bestimmte Therapien anspricht. Die hier hervorgehobenen Varianten von TTLL12 und HM13 signalisieren nicht nur Gefahr; sie scheinen Krebszellen beim Überleben, bei der Bewegung und bei der Therapieresistenz zu helfen, lassen sich im Labor jedoch gezielt angreifen, ohne normale Speiseröhrenzellen stark zu schädigen. Obwohl sich diese Arbeit noch in einem frühen experimentellen Stadium befindet und größere Patientenstudien nötig sind, öffnet sie den Weg für künftige Tests, die Isoform‑Muster verfolgen, sowie für neue Wirkstoffe oder RNA‑basierte Therapien, die darauf abzielen, die schädlichsten Genvarianten beim ösophagealen Krebs selektiv auszuschalten.
Zitation: Zhang, Y., Ntsiful, D.A., Israel, R. et al. Identification of isoform switching events linked with esophageal adenocarcinoma patient survival informs novel prognostic and therapeutic targets. Cell Death Dis 17, 305 (2026). https://doi.org/10.1038/s41419-026-08542-2
Schlüsselwörter: Speiseröhrenkrebs, Barrett‑Ösophagus, RNA‑Isoforme, gezielte Therapie, Autophagie