Clear Sky Science · he
זיהוי אירועי החלפת איזופורמים הקשורים להישרדות חולים עם אדנוקרצינומה של הוושט מעניק תובנות לגבי מטרות פרוגנוסטיות וטיפוליות חדשות
מדוע מחקר זה חשוב
אדנוקרצינומה של הוושט היא סוג של סרטן צינור המזון שהופך ליותר שכיח אך עדיין מאופיין בשיעורי הישרדות נמוכים מאוד. בדיקות סקר נוכחיות פעמים רבות מפספסות אנשים בסיכון, וטיפולים סטנדרטיים כמו כימותרפיה וניתוחים מועילים רק לחלק מהחולים. המחקר שואל שאלה חדשה: במקום להסתכל רק על אילו גנים דולקים או כבויים בגידול, מה אם נבחן ביתר פירוט אילו גרסאות של אותם גנים בשימוש? בהתמקדות בגרסאות ה"מוחלפות" הללו, החוקרים מגלים סימנים חדשים המעידים על הישרדות ירודה ומצביעים על אסטרטגיות טיפול פוטנציאליות שעשויות לשמר תאים בריאים.
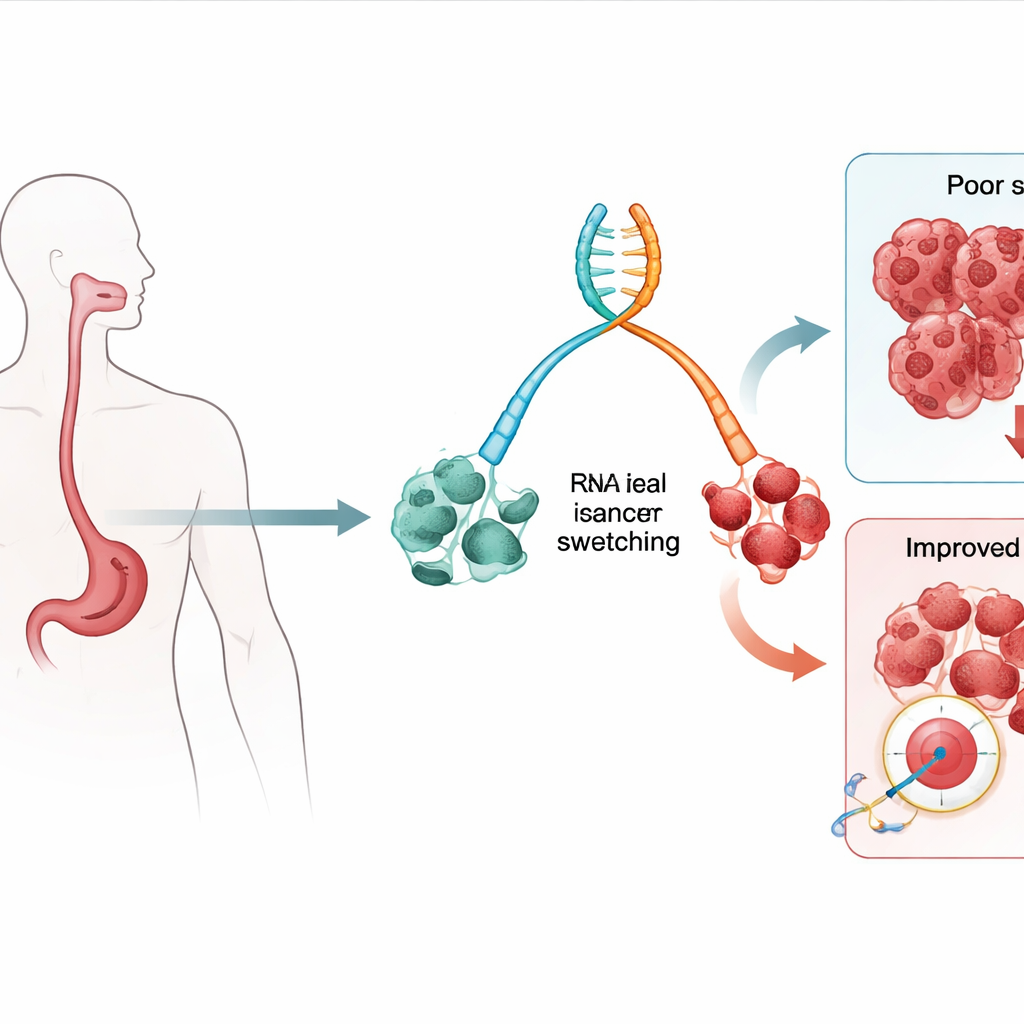
שינויים במסרי הגן כסימני אזהרה מוקדמים
הגנים שלנו יכולים לייצר מספר מסרים מעט שונים, הידועים כאיזופורמים, מאותו מקטע DNA. הצוות בחן RNA, המולקולה שמועברת המסרים האלה, מדגימות רקמה שנלקחו מאנשים עם וושט של בארט (מצב טרום- סרטני ידוע) ומאלה שכבר פיתחו אדנוקרצינומה של הוושט. הם חיפשו "החלפות" איזופורמים, שבהן גרסה אחת של גן נעשית שכיחה יותר ואחרת פחות ככל שהרקמה מתקדמת מוושט של בארט בסיכון נמוך למחלה בסיכון גבוה ולסרטן. באמצעות מודלים סטטיסטיים שמקשרים החלפות אלו לתוצאי מטופלים, זיהו החוקרים עשרות איזופורמים שנוכחותם או העדרם היו קשורים לסיכויים גבוהים יותר למוות מכל הסיבות ובמיוחד ממחלת הסרטן.
שתי גרסאות גנים שמסמנות סיכון
מבין האיזופורמים הרבים שנחשפו, בלטו שתי גרסאות: גרסאות מסוימות של הגנים המכונים TTLL12 ו-HM13. גרסאות ספציפיות אלה הופיעו בשכיחות גבוהה יותר בנגעים טרום-סרטן בדרגה גבוהה ובסרטן מאשר ברקמת בארט בדרגה נמוכה, וחולים שהגידולים שלהם הסתמכו רבות על איזופורמים אלה נטו להישרדות גרועה יותר. חשוב לציין שרמות הגן הכוללות של TTLL12 ו-HM13 לא סיפקו את כל התמונה; הזזת השימוש לגרסאות המסוימות הללו היא שהעבירה את אות האזהרה. החוקרים אימתו דפוסים אלה לא רק בדגימות מטופלים, אלא גם במודל עכבר של סרטן ושט מונע על ידי רפלוקס ובמאגר נתוני סרטן אנושי עצמאי, מה שמצביע על כך שהממצאים יציבים ובעלי משמעות ביולוגית.
להפוך איזופורמים מזיקים נגד הסרטן
כדי לבדוק האם איזופורמים אלה הם רק סמנים או מנהלי מחלה בפועל, השתמשו המדענים בכלי RNA קטנים על מנת להשתיק באופן סלקטיבי את הגרסאות המסוכנות של TTLL12 ו-HM13 בשתי שורות תאים של סרטן הוושט שגודלו במעבדה. חסימת כל אחד מהאיזופורמים הפחיתה במידה חדה את גדילת תאי הסרטן ועיכבה את יכולתם להגר — שלב מרכזי בהתפשטות — בעוד שהשפעות על תאים תקינים של הוושט היו שוליות. אף על פי כן, מרשים עוד יותר, כאשר האיזופורמים הושתקו, תרופות הכימותרפיה הסטנדרטיות (paclitaxel ו-carboplatin) הפכו ליעילות יותר, פועלות בשילוב סינרגיסטי עם השתקת האיזופורמים להרוג הרבה יותר תאי סרטן מאשר כל אחת מהשיטות בנפרד.
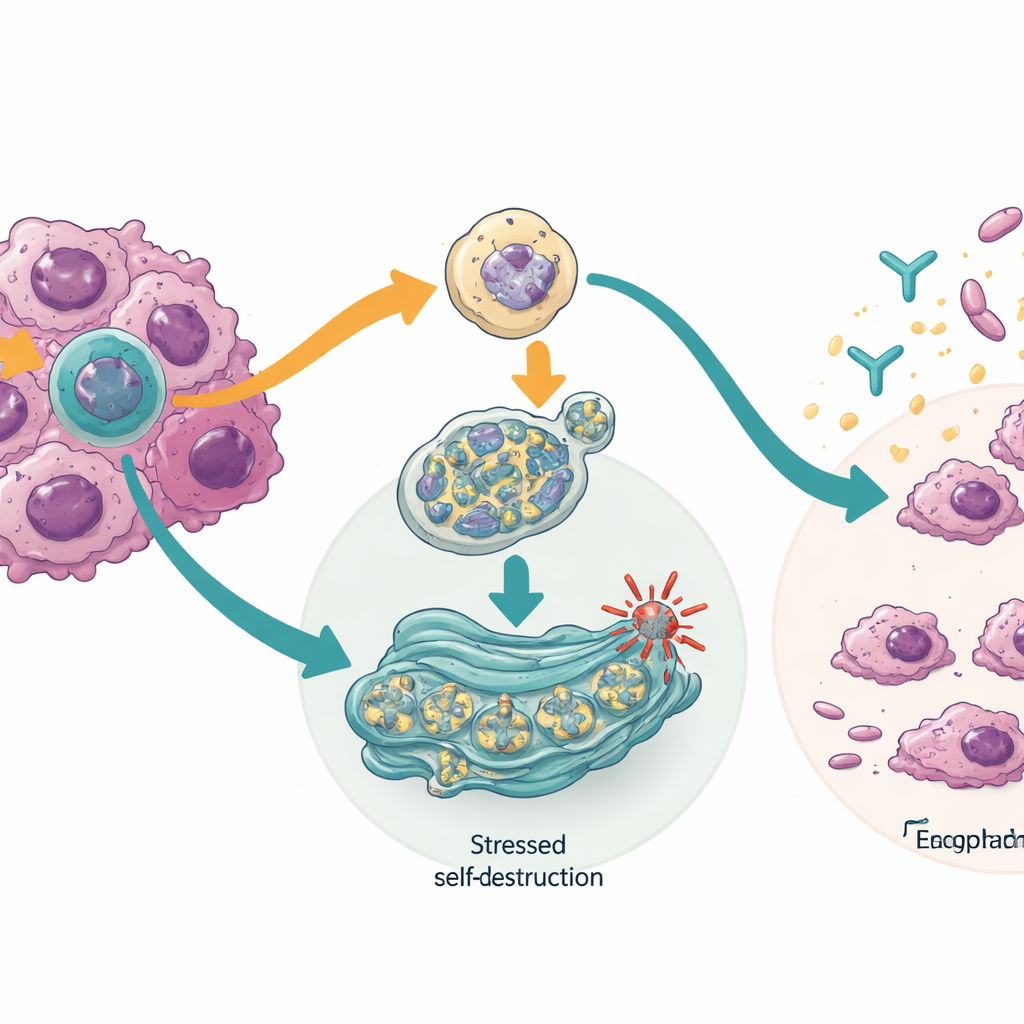
כיצד דוחפים את תאי הסרטן לעבר השמדת-עצמית
בחינה מעמיקה של המנגנון גילתה כי חסימת איזופורם ה-TTLL12 הפעלה של מערכת בקרת איכות בתוך התאים הנקראת אוטופגיה מתווכת-חפרון (chaperone-mediated autophagy). מערכת זו מסייעת לפרק חלבונים פגומים או מסוכנים. בתאי הסרטן, הפעלתה הורידה רמות של חלבונים המסייעים לגידולים לשרוד נזקי DNA, כולל CHK1 וצורות מוטנטיות של הגן השומר הידוע TP53. לעומת זאת, חסימת איזופורם ה-HM13 יצרה מתח במפעל קיפול החלבונים של התא, הרשתית האנדופלסמטית, והפעילה דרך תגובתית שיכולה לעצור ייצור חלבונים, להפעיל מיחזור של רכיבים תאים פגומים ובסופו של דבר להוביל למוות מתוכנת של התא. בחלק מתאי הסרטן, שינוי זה גם הגביר את הרגישות שלהם לתרופה מבוססת חיסון שממוקדת ב-PD-L1, מה שמעיד שאיזופורם-שינוי עשוי לעזור לגידולים להסתתר ממערכת החיסון.
מה זה עשוי להצביע עבור מטופלים
ביחד, ממצאים אלה מצביעים על כך שהתמקדות באיזופורמים שבהם משתמש הגידול עשויה לשפר את היכולת של רופאים לחזות מי בסיכון הגבוה ביותר ומי עשוי להגיב טוב יותר לטיפולים מסוימים. הגרסאות הספציפיות של TTLL12 ו-HM13 המודגשות כאן עושות יותר מתן אותות סיכון; נראה שהן מסייעות לתאי הסרטן לשרוד, לנוע ולהיות עמידים לטיפול, ובכל זאת ניתן למקד אותן מבלי לפגוע במידה רבה בתאים תקינים של הוושט במעבדה. למרות שעבודה זו נמצאת עדיין בשלבים ניסויית מוקדמים ונדרשים מחקרים גדולים יותר בחולים, היא פותחת דלת לבדיקות עתידיות שמנטרות דפוסי איזופורמים ולפיתוח תרופות או טיפולים מבוססי RNA שמתוכננים להשתיק באופן סלקטיבי את גרסאות הגנים המזיקות ביותר בסרטן הוושט.
ציטוט: Zhang, Y., Ntsiful, D.A., Israel, R. et al. Identification of isoform switching events linked with esophageal adenocarcinoma patient survival informs novel prognostic and therapeutic targets. Cell Death Dis 17, 305 (2026). https://doi.org/10.1038/s41419-026-08542-2
מילות מפתח: סרטן הוושט, וושט של בארט, איזופורמי RNA, טיפול ממוקד, אוטופגיה