Clear Sky Science · pl
Identyfikacja zdarzeń przełączania izoform związanych z przeżyciem pacjentów z gruczolakorakiem przełyku dostarcza nowych celów prognostycznych i terapeutycznych
Dlaczego to badanie ma znaczenie
Gruczolakorak przełyku to rodzaj nowotworu przełyku, którego występowanie rośnie, a jednocześnie charakteryzuje się bardzo niskim wskaźnikiem przeżyć. Obecne testy przesiewowe często nie wykrywają osób zagrożonych, a standardowe terapie, takie jak chemioterapia i zabieg chirurgiczny, pomagają tylko części pacjentów. W tym badaniu zadano nowe pytanie: zamiast patrzeć wyłącznie na to, które geny są włączone lub wyłączone w guzach, co się stanie, jeśli przyjrzymy się uważniej, które wersje tych genów są wykorzystywane? Skupiając się na tych „przełączonych” wersjach, naukowcy odkryli nowe wskaźniki złego rokowania i wskazali potencjalne strategie leczenia, które mogą oszczędzać zdrowe komórki.
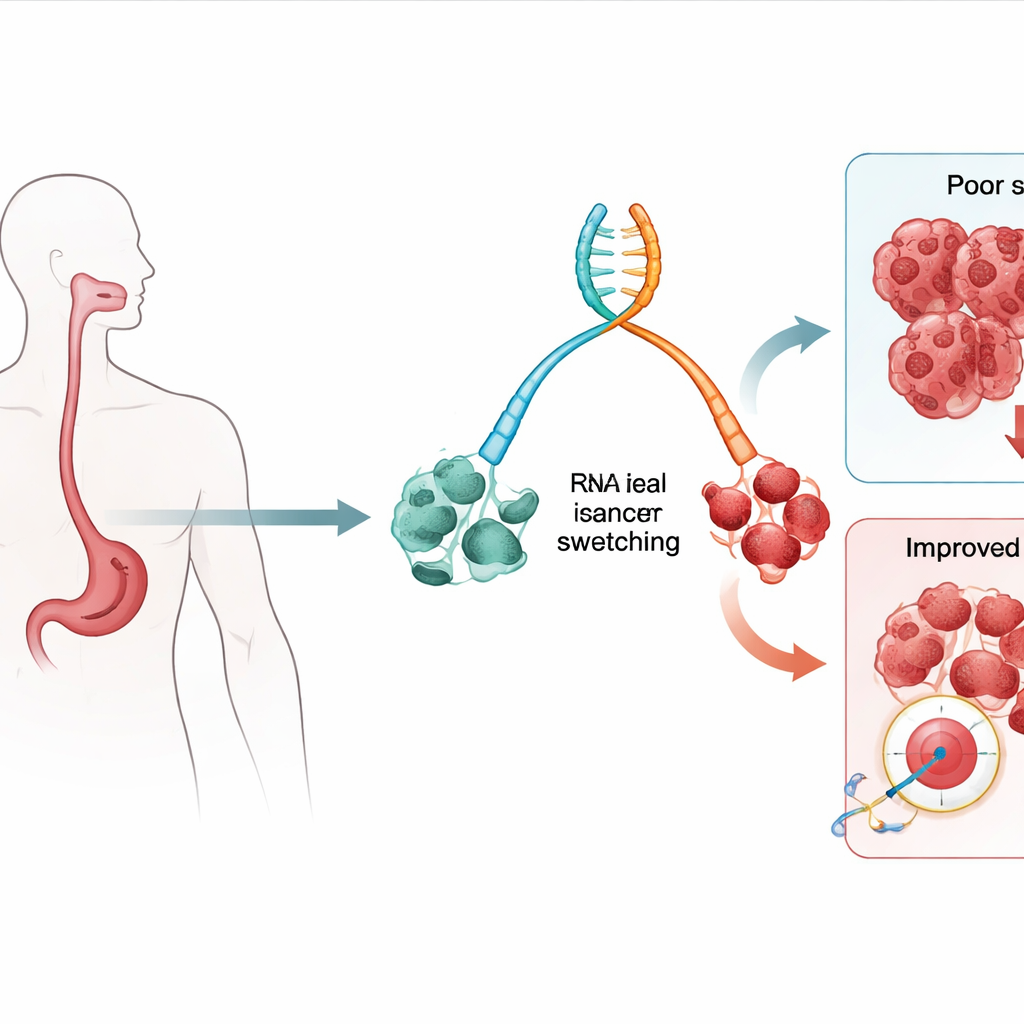
Zmiany w komunikatach genowych jako wczesne sygnały ostrzegawcze
Nasze geny mogą wytwarzać kilka nieco różnych komunikatów, znanych jako izoformy, z tego samego odcinka DNA. Zespół badał RNA, cząsteczkę przenoszącą te komunikaty, w próbkach tkankowych pobranych od osób z przełykiem Barretta (znanym stanem przedrakowym) oraz od pacjentów z rozwiniętym gruczolakorakiem przełyku. Poszukiwano „przełączeń” izoform, gdy jedna wersja genu staje się bardziej powszechna, a inna mniej powszechna w miarę przejścia tkanki od niskiego ryzyka Barretta do zaawansowanej choroby i raka. Korzystając z modeli statystycznych łączących te przełączenia z rezultatami pacjentów, zidentyfikowano dziesiątki izoform, których obecność lub brak wiązał się z wyższym ryzykiem śmierci z dowolnej przyczyny i ze śmiercią z powodu raka.
Dwie wersje genów zwiastujące kłopoty
Wśród wielu odkrytych izoform wyróżniły się dwie: konkretne wersje genów nazwanych TTLL12 i HM13. Te specyficzne izoformy występowały częściej w zmianach przednowotworowych wysokiego stopnia i w nowotworach niż w tkance Barretta niskiego stopnia, a pacjenci, których guzy silnie polegały na tych izoformach, mieli gorsze przeżycie. Co ważne, całkowite poziomy genów TTLL12 i HM13 nie oddawały całej prawdy; to właśnie przesunięcie w stronę tych konkretnych izoform niosło sygnał ostrzegawczy. Badacze potwierdzili te wzorce nie tylko w próbkach pacjentów, ale także w modelu szczurzym raka przełyku wywołanego refluksem oraz w niezależnym ludzkim zestawie danych nowotworowych, co sugeruje, że odkrycia są rzetelne i biologicznie istotne.
Wykorzystanie szkodliwych izoform przeciwko rakowi
Aby sprawdzić, czy te izoformy są jedynie markerami, czy rzeczywistymi czynnikami napędzającymi chorobę, naukowcy zastosowali małe narzędzia RNA do selektywnego wyciszenia ryzykownych wersji TTLL12 i HM13 w dwóch liniach komórek raka przełyku hodowanych w laboratorium. Zablokowanie którejkolwiek z izoform zdecydowanie zmniejszyło wzrost komórek nowotworowych i spowolniło ich zdolność do migracji — kluczowego kroku w rozsiewie — przy jednoczesnym jedynie niewielkim wpływie na normalne komórki przełyku. Co jeszcze bardziej uderzające, po wyciszeniu izoform standardowe leki chemioterapeutyczne (paklitaksel i karboplatyna) stały się bardziej skuteczne, działając razem z knockdownem w sposób synergistyczny i zabijając znacznie więcej komórek nowotworowych niż każda z tych metod osobno.
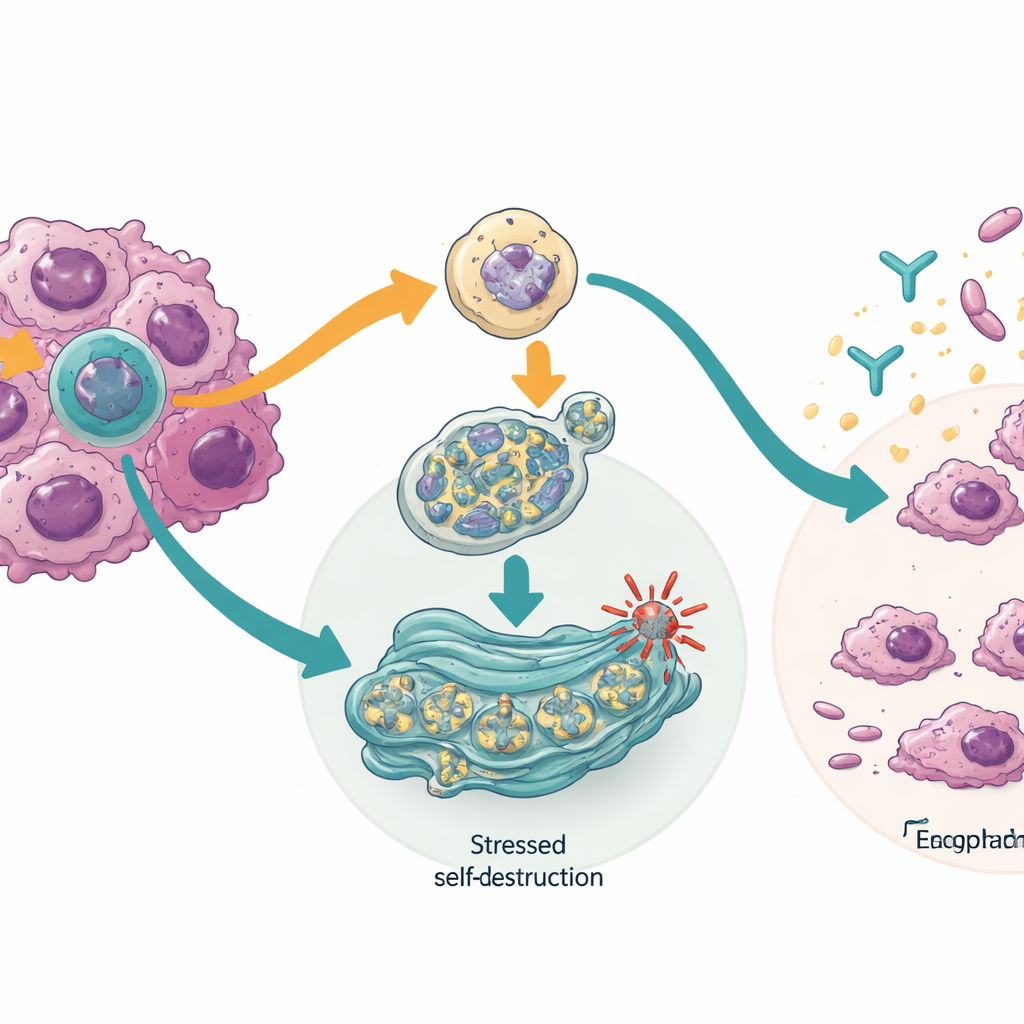
Jak komórki rakowe są popychane ku samozniszczeniu
Zgłębiając mechanizmy, zespół odkrył, że blokada izoformy TTLL12 uruchamia system kontroli jakości w komórce zwany chaperonowo-mediowaną autofagią. System ten pomaga rozkładać uszkodzone lub niebezpieczne białka. W komórkach nowotworowych jego aktywacja obniżała poziomy białek pomagających guzom przetrwać uszkodzenia DNA, w tym CHK1 oraz zmutowane formy znanego genu strażnika TP53. Z kolei blokada izoformy HM13 stresowała fabrykę fałdowania białek w komórce — retikulum endoplazmatyczne — uruchamiając szlak odpowiedzi, który może zatrzymać produkcję białek, aktywować recykling wadliwych elementów komórkowych i ostatecznie doprowadzić komórkę do zaprogramowanej śmierci. W niektórych komórkach nowotworowych ta sama zmiana uczyniła je także bardziej podatnymi na lek immunoterapeutyczny celujący w PD-L1, co sugeruje, że przełączanie izoform może pomagać guzom ukrywać się przed układem odpornościowym.
Co to może znaczyć dla pacjentów
Łącznie te wyniki sugerują, że zwracanie uwagi na to, których izoform używa guz, mogłoby poprawić zdolność lekarzy do przewidywania, kto jest najbardziej zagrożony i kto może najlepiej odpowiedzieć na określone terapie. Wyróżnione tu wersje TTLL12 i HM13 robią więcej niż wskazują na niebezpieczeństwo; wydają się pomagać komórkom nowotworowym przetrwać, poruszać się i opierać terapii, a jednocześnie mogą być celowane bez większej szkody dla normalnych komórek przełyku w warunkach laboratoryjnych. Choć prace te pozostają we wczesnej, eksperymentalnej fazie i potrzebne są większe badania na pacjentach, otwierają drogę do przyszłych testów śledzących wzorce izoform oraz do nowych leków lub terapii opartych na RNA, zaprojektowanych tak, by selektywnie wyłączać najbardziej szkodliwe wersje genów w raku przełyku.
Cytowanie: Zhang, Y., Ntsiful, D.A., Israel, R. et al. Identification of isoform switching events linked with esophageal adenocarcinoma patient survival informs novel prognostic and therapeutic targets. Cell Death Dis 17, 305 (2026). https://doi.org/10.1038/s41419-026-08542-2
Słowa kluczowe: rak przełyku, przełyk Barretta, izoformy RNA, terapia celowana, autofagia