Clear Sky Science · fr
Identification des événements de commutation d’isoformes liés à la survie des patients atteints d’adénocarcinome œsophagien informe de nouvelles cibles pronostiques et thérapeutiques
Pourquoi cette recherche est importante
L’adénocarcinome de l’œsophage est un type de cancer de la voie alimentaire dont l’incidence augmente mais dont le taux de survie reste très faible. Les tests de dépistage actuels manquent souvent les personnes à risque, et les traitements standard comme la chimiothérapie et la chirurgie ne profitent qu’à une fraction des patients. Cette étude pose une question nouvelle : au lieu de ne regarder que quels gènes sont activés ou désactivés dans les tumeurs, que se passe-t-il si l’on examine de plus près quelles versions de ces gènes sont utilisées ? En se concentrant sur ces versions « basculées », les chercheurs mettent en lumière de nouveaux signaux annonciateurs d’une mauvaise survie et désignent des stratégies thérapeutiques potentielles qui pourraient épargner les cellules saines.
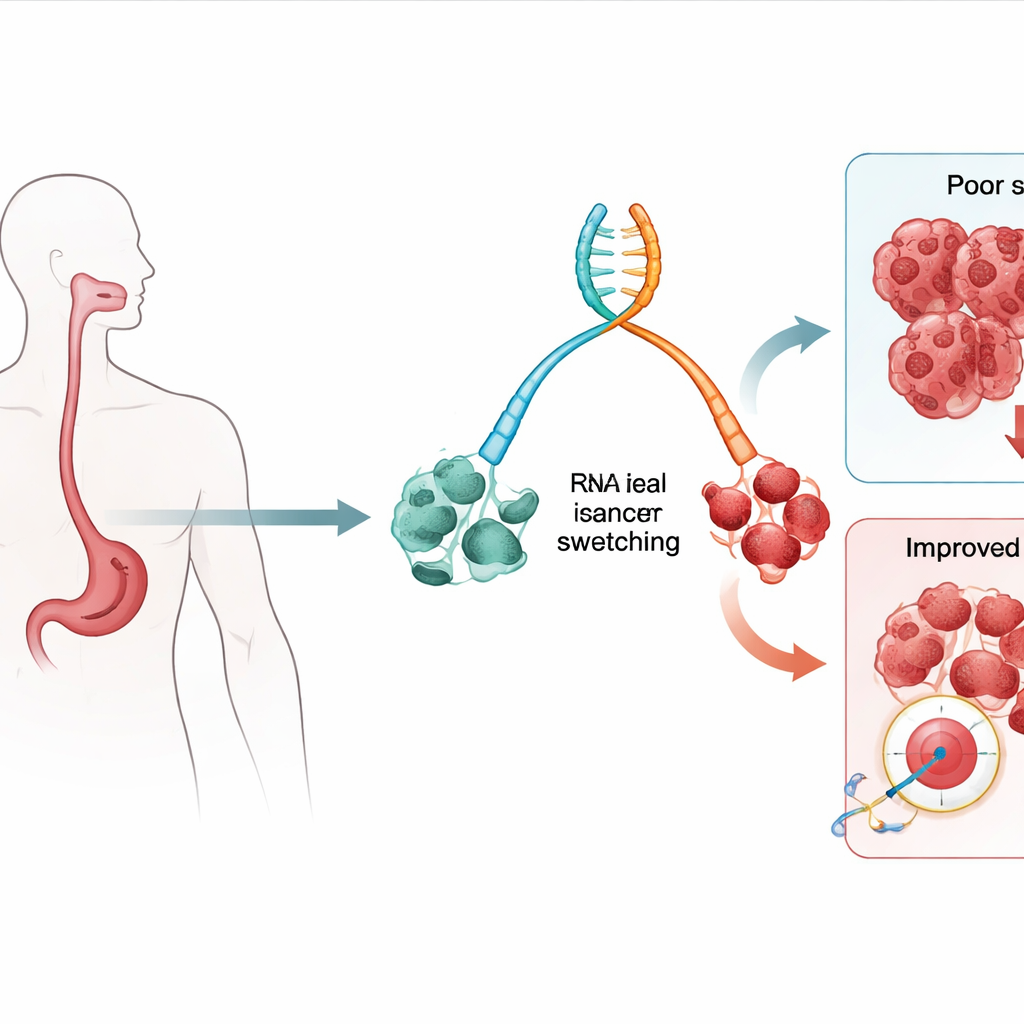
Des changements dans les messages génétiques comme signaux précoces
Nos gènes peuvent produire plusieurs messages légèrement différents, appelés isoformes, à partir d’un même segment d’ADN. L’équipe a analysé l’ARN, la molécule qui transporte ces messages, issu d’échantillons de tissus prélevés chez des personnes atteintes d’un œsophage de Barrett (une affection pré‑cancéreuse reconnue) et chez des patients ayant développé un adénocarcinome œsophagien. Ils ont recherché des « commutations » d’isoformes, où une version d’un gène devient plus fréquente tandis qu’une autre devient moins fréquente à mesure que le tissu évolue d’un Barrett à faible risque vers une maladie à haut risque et vers le cancer. À l’aide de modèles statistiques reliant ces commutations aux résultats des patients, ils ont identifié des dizaines d’isoformes dont la présence ou l’absence était associée à des risques accrus de décès toutes causes confondues et de décès liés au cancer spécifiquement.
Deux versions de gènes qui annoncent des complications
Parmi les nombreux isoformes découverts, deux ont particulièrement attiré l’attention : des versions spécifiques des gènes TTLL12 et HM13. Ces isoformes étaient plus fréquentes dans les lésions précancéreuses de haut grade et dans les cancers que dans le tissu de Barrett de bas grade, et les patients dont les tumeurs dépendaient fortement de ces isoformes présentaient en général une survie plus mauvaise. Fait important, les niveaux globaux des gènes TTLL12 et HM13 ne racontaient pas toute l’histoire ; c’est le basculement vers ces isoformes particulières qui portait le signal d’alerte. Les chercheurs ont confirmé ces schémas non seulement dans des échantillons de patients, mais aussi dans un modèle rat de cancer œsophagien induit par le reflux et dans un jeu de données humain indépendant, suggérant que les résultats sont robustes et biologiquement pertinents.
Retourner les isoformes nuisibles contre le cancer
Pour vérifier si ces isoformes sont de simples marqueurs ou de vrais moteurs de la maladie, les scientifiques ont utilisé de petits outils ARN pour silencier sélectivement les versions à risque de TTLL12 et HM13 dans deux lignées cellulaires cancéreuses œsophagiennes cultivées en laboratoire. Bloquer l’un ou l’autre isoforme a fortement réduit la croissance des cellules cancéreuses et ralenti leur capacité de migration — une étape clé de la dissémination — tout en n’ayant que des effets mineurs sur les cellules œsophagiennes normales. Plus frappant encore, lorsque les isoformes étaient inhibées, les médicaments de chimiothérapie standards (paclitaxel et carboplatine) devenaient plus efficaces, agissant de façon synergique avec l’inhibition pour tuer bien plus de cellules cancéreuses que chaque approche prise isolément.
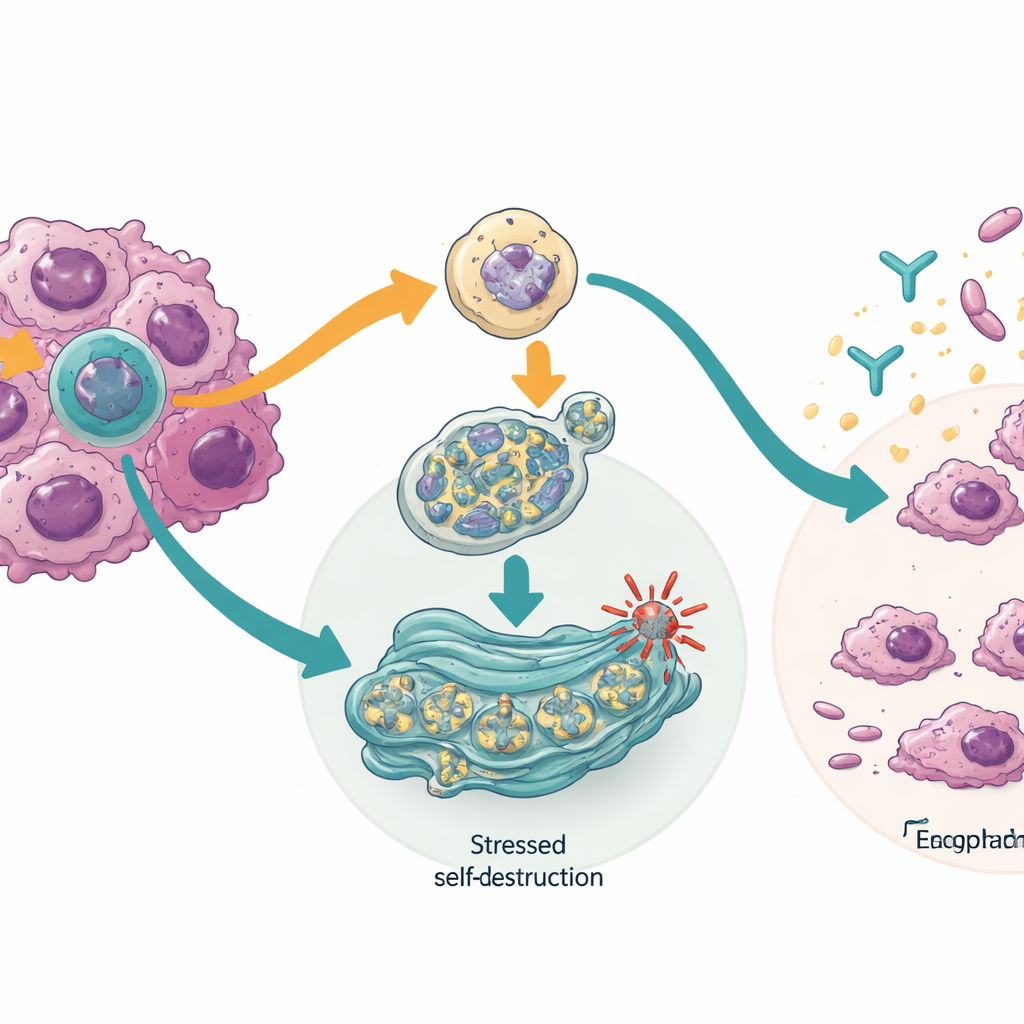
Comment les cellules cancéreuses sont poussées à l’autodestruction
En creusant le mécanisme, l’équipe a découvert que le blocage de l’isoforme TTLL12 activait un système de contrôle qualité intracellulaire appelé autophagie médiée par chaperonne. Ce système aide à dégrader les protéines endommagées ou dangereuses. Dans les cellules cancéreuses, son activation abaissait les niveaux de protéines qui aident les tumeurs à survivre aux dommages de l’ADN, notamment CHK1 et des formes mutées du célèbre gène gardien TP53. Le blocage de l’isoforme HM13, en revanche, mettait à rude épreuve l’usine de repliement des protéines de la cellule, le réticulum endoplasmique, déclenchant une voie de réponse capable d’arrêter la production protéique, d’activer le recyclage des éléments cellulaires défectueux et, en fin de compte, de pousser la cellule vers la mort programmée. Dans certaines cellules cancéreuses, ce même changement les rendait aussi plus vulnérables à un médicament immunitaire ciblant PD‑L1, ce qui suggère que la commutation d’isoformes pourrait aider les tumeurs à se cacher du système immunitaire.
Ce que cela pourrait signifier pour les patients
Ensemble, ces résultats suggèrent que prêter attention aux isoformes utilisés par une tumeur pourrait améliorer la prédiction par les médecins de qui est le plus à risque et qui pourrait le mieux répondre à certains traitements. Les versions spécifiques de TTLL12 et HM13 mises en avant ici font plus que signaler un danger ; elles semblent aider les cellules cancéreuses à survivre, à migrer et à résister aux thérapies, tout en pouvant être ciblées sans grand tort pour les cellules œsophagiennes normales en laboratoire. Bien que ces travaux en soient encore à un stade expérimental précoce et que des études plus larges chez les patients soient nécessaires, ils ouvrent la voie à de futurs tests qui suivraient les profils d’isoformes et à de nouveaux médicaments ou thérapies à base d’ARN conçus pour éteindre sélectivement les versions géniques les plus nocives dans le cancer œsophagien.
Citation: Zhang, Y., Ntsiful, D.A., Israel, R. et al. Identification of isoform switching events linked with esophageal adenocarcinoma patient survival informs novel prognostic and therapeutic targets. Cell Death Dis 17, 305 (2026). https://doi.org/10.1038/s41419-026-08542-2
Mots-clés: cancer de l’œsophage, œsophage de Barrett, isoformes d’ARN, thérapie ciblée, autophagie