Clear Sky Science · zh
针对非小细胞肺癌脑转移的KRASG12C抑制剂及联合策略的治疗进展
这对患者及其家庭的重要性
来自肺癌的脑转移往往破坏性极大,导致严重的神经功能障碍和短暂的生存期。本文回顾了一波针对非小细胞肺癌(NSCLC)中一种特定基因改变——KRAS G12C的精准药物。这些药物不仅旨在缩小肺内原发肿瘤,还能进入大脑并攻击那里的转移灶——这是许多传统化疗和早期靶向药难以做到的。对患者和家庭而言,这项工作指向了更有效、持续时间更长且更符合每位患者肿瘤生物学特征的治疗方案。
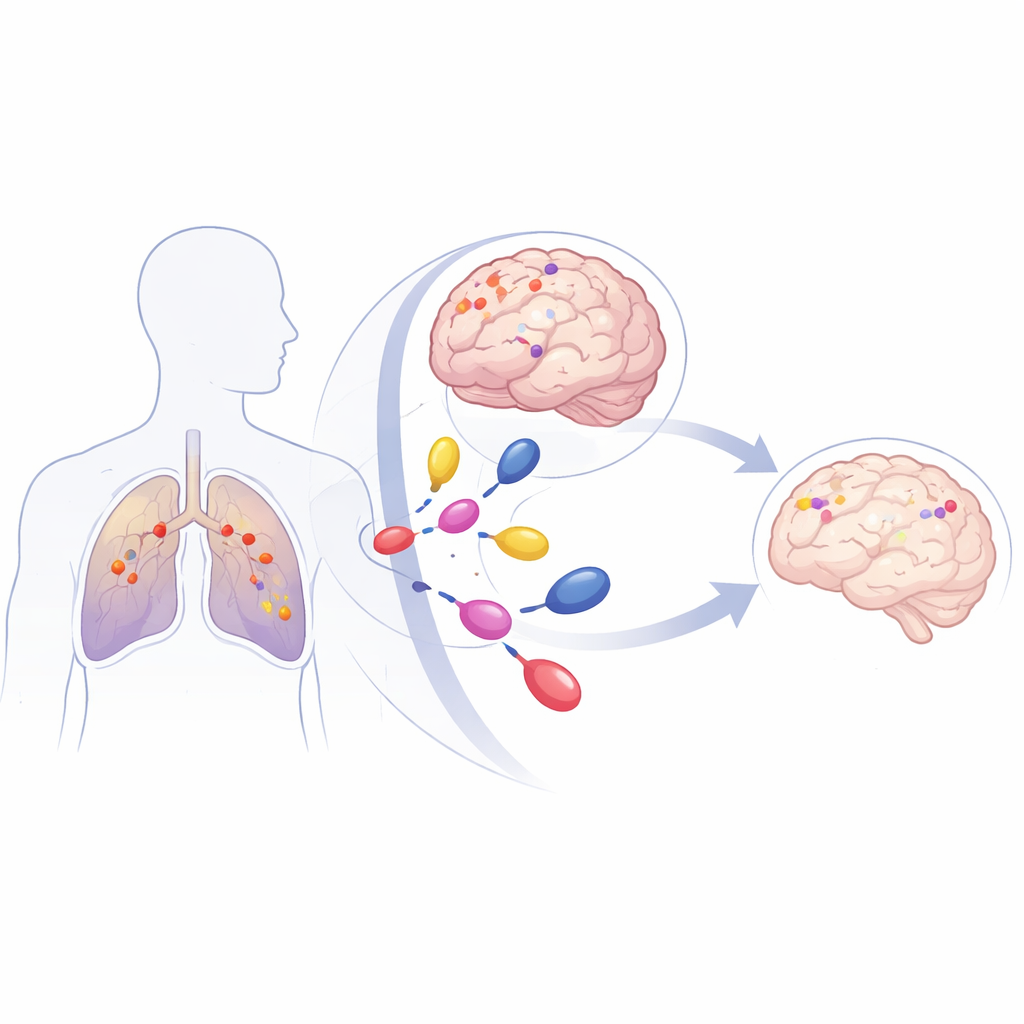
一种常见但具危险转移模式的肺癌
NSCLC是最常见的肺癌类型,也是癌症死亡的主要原因之一。高达40%的患者会出现脑转移,这类病灶难以治疗,因为它们位于大脑的保护屏障——血脑屏障之后。许多NSCLC肿瘤携带KRAS基因突变,该基因类似于细胞生长的“卡住的油门”。其中一种变体,称为KRAS G12C,大约占KRAS突变型NSCLC的40%。携带该突变的患者在病程早期就有较高的发生脑转移的风险,而传统治疗如全脑放疗或立体定向放射外科通常只能在数个月内控制病情。
KRAS G12C如何助长肿瘤生长
正常情况下,KRAS在“开启”和“关闭”状态之间转换,以调节细胞生长、生存和代谢的信号。G12C突变使KRAS锁定在活跃状态,持续向主要通路发送增长信号,促进细胞分裂、抗凋亡、血管新生并在肿瘤周围形成免疫抑制性环境。这种持续信号不仅加速肺部肿瘤生长,还帮助癌细胞扩散并适应像大脑这样的新生境。其他基因的共突变,例如CDKN2A、KEAP1、LKB1和SMARCA4,可能使肿瘤更具侵袭性,并在局部治疗后更容易在大脑复发。
能够进入大脑的新药
数十年来,KRAS被认为是“不可成药”的,但现在已有几类小分子能够特异性靶向KRAS G12C。有些药物结合蛋白的非活性形式并使其保持关闭,而更新一代的制剂也能作用于活性形式。诸如sotorasib和adagrasib的药物率先进入临床,在晚期NSCLC中显示出明确益处,包括对有脑转移的患者。特别是adagrasib,有强有力的证据表明它能穿越血脑屏障,并在相当比例的患者中使未经治疗的脑病灶缩小,许多患者实现了数月的颅内疾病控制。下一代药物——如olomorasib、fulzerasib、garsorasib、divarasib、D3S-001和RMC‑6236——正在被测试以期获得更强的活性、更好的脑穿透性以及对多种KRAS突变的更广泛效能。
联合出击以克服耐药
即便有了这些进展,仅用KRAS G12C抑制剂治疗的大多数患者在数月内仍会出现疾病进展。综述强调了肿瘤如何通过继发性KRAS突变、生长通路再激活以及肿瘤微环境变化来适应治疗,并描述了旨在阻断这些逃逸途径的联合策略。将KRAS抑制剂与免疫疗法联合,可增强免疫系统对肿瘤的攻击;与针对MEK、CDK4/6或SHP2的药物联合,则进一步关闭下游信号通路。在临床前模型和早期临床研究中,这些联合方案已带来更深更持久的反应,包括对脑转移的控制。研究者们还在测试将KRAS抑制剂与放疗联合使用,看看是否能使肿瘤更易感,从而在维持或改善颅内控制的同时使用更低的放疗剂量。
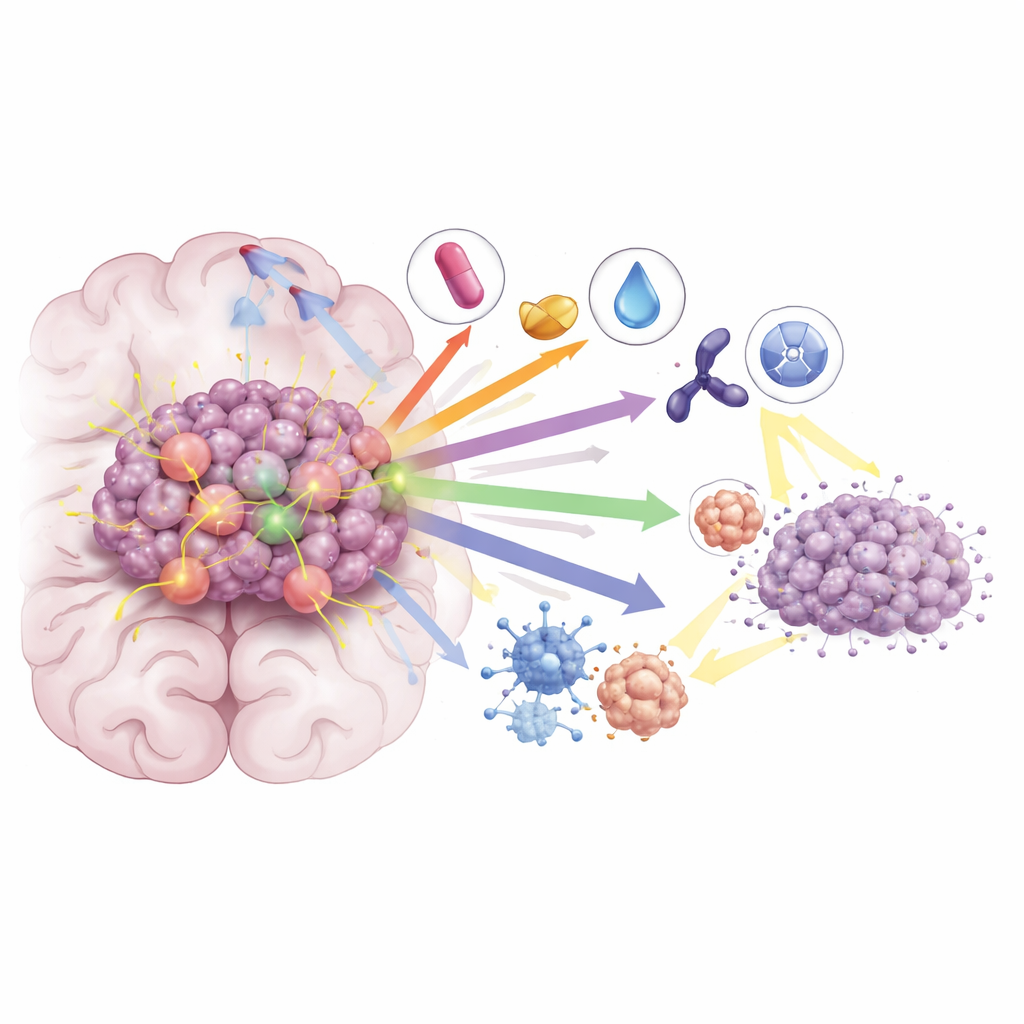
这对未来意味着什么
总体而言,文章得出结论:KRAS G12C不再是不可触及的靶点。一组不断扩展的可进入大脑的抑制剂工具箱,特别是在与免疫治疗、其他靶向药物和放疗进行合理组合时,正开始改变带有脑转移的NSCLC患者的预后。尽管仍面临挑战——尤其是药物耐药性和需要获得更持久疗效——作者认为,聚焦于既针对癌细胞又作用于其周围环境的合理联合策略,提供了将短暂反应转变为更持久疾病控制和延长生存的最佳希望。
引用: Bhattacharya, D., Roman, B. & Reddy, S. Therapeutic advances with KRASG12C inhibitors and combination strategies in non-small cell lung cancer brain metastases. Cancer Gene Ther 33, 323–337 (2026). https://doi.org/10.1038/s41417-026-01003-0
关键词: KRAS G12C, 非小细胞肺癌, 脑转移, 靶向治疗, 免疫治疗联合