Clear Sky Science · nl
Therapeutische doorbraken met KRASG12C-remmers en combinatiestrategieën bij hersenmetastasen van niet-kleincellig longkanker
Waarom dit belangrijk is voor patiënten en families
Hersenmetastasen door longkanker zijn vaak verwoestend: ze veroorzaken ernstige neurologische problemen en gaan vaak gepaard met een korte levensverwachting. Dit artikel bespreekt een nieuwe generatie precisiegeneesmiddelen die een specifieke genetische afwijking, KRAS G12C, bij niet-kleincellig longkanker (NSCLC) richten. Deze middelen zijn ontworpen om niet alleen longtumoren te verkleinen, maar ook de hersenen binnen te dringen en daar metastasen aan te pakken — een terrein waar oudere chemotherapieën en veel gerichte middelen moeite mee hebben gehad. Voor patiënten en families wijst dit werk op behandelingsstrategieën die effectiever, duurzamer en beter afgestemd zijn op de biologische kenmerken van ieders tumor.
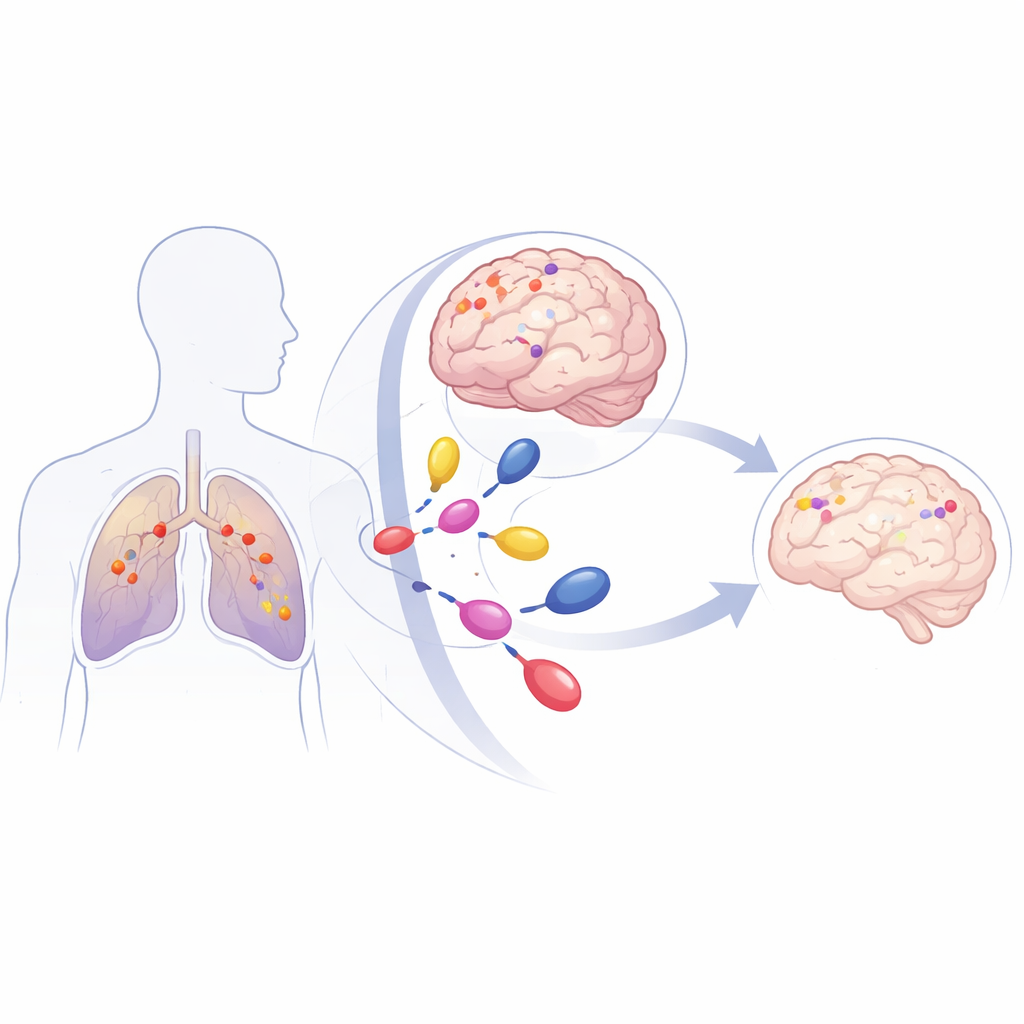
Een veelvoorkomende longkanker met een gevaarlijk patroon
NSCLC is de meest voorkomende vorm van longkanker en een belangrijke doodsoorzaak door kanker. Tot 40% van de patiënten krijgt metastasen in de hersenen, die moeilijk te behandelen zijn omdat ze zich achter de beschermende barrière van de hersenen bevinden, de bloed-hersenbarrière. Veel NSCLC-tumoren dragen mutaties in het gen KRAS, dat fungeert als een vastzittend gaspedaal voor celgroei. Eén specifieke variant, KRAS G12C, vormt ongeveer 40% van de KRAS-gemuteerde NSCLC. Patiënten met deze mutatie lopen een hoog risico om vroeg in het ziekteverloop hersenmetastasen te ontwikkelen, en traditionele behandelingen zoals bestraling van de hele hersenen of gerichte radioschirurgie controleerden de ziekte meestal slechts enkele maanden.
Hoe KRAS G12C tumorgroei aanjaagt
KRAS schakelt normaal tussen een "aan"- en "uit"-stand om celsignalen voor groei, overleving en metabolisme te reguleren. De G12C-mutatie vergrendelt KRAS in de actieve vorm, waardoor continu groeisignalen worden gestuurd via belangrijke paden die celdeling, resistentie tegen celdood, aanleg van nieuwe bloedvaten en een immuunonderdrukkende omgeving rond de tumor bevorderen. Deze voortdurende signalering versnelt niet alleen de tumorgroei in de long, maar helpt kankercellen ook zich te verspreiden en zich aan te passen aan nieuwe locaties zoals de hersenen. Co-mutaties in andere genen, zoals CDKN2A, KEAP1, LKB1 en SMARCA4, kunnen tumoren nog agressiever maken en de kans vergroten dat ze na lokale behandelingen terugkeren in de hersenen.
Nieuwe middelen die de hersenen bereiken
Gedurende decennia werd KRAS als "onberekenbaar" beschouwd, maar verschillende klassen kleine moleculen richten zich nu specifiek op KRAS G12C. Sommige binden aan de inactieve vorm van het eiwit en houden het uitgeschakeld, terwijl nieuwere middelen ook de actieve vorm aanvallen. Middelen zoals sotorasib en adagrasib waren de eersten die de kliniek bereikten en hebben duidelijke voordelen getoond bij gevorderde NSCLC, ook bij patiënten met hersenmetastasen. Adagrasib heeft met name sterke aanwijzingen dat het de bloed-hersenbarrière passeert en krimp van onbehandelde hersenlaesies veroorzaakt bij een aanzienlijk deel van de patiënten, waarbij velen maandenlang gecontroleerde intracraniële ziekte bereikten. Next-generation middelen — zoals olomorasib, fulzerasib, garsorasib, divarasib, D3S-001 en RMC‑6236 — worden getest op grotere potentie, betere hersendoordringbaarheid en bredere activiteit tegen diverse KRAS-mutaties.
De krachten bundelen om resistentie te overwinnen
Zelfs met deze vooruitgang zien de meeste patiënten die alleen met KRAS G12C-remmers worden behandeld hun kanker binnen enkele maanden weer progressie vertonen. De review belicht hoe tumoren zich aanpassen — via secundaire KRAS-mutaties, reactivatie van groeipaden en veranderingen in de tumoromgeving — en beschrijft combinatiestrategieën die zijn ontworpen om deze ontsnappingsroutes te blokkeren. Het combineren van KRAS-remmers met immunotherapie kan het immuunsysteem versterken in de aanval op tumoren, terwijl combinaties met middelen die MEK, CDK4/6 of SHP2 remmen de downstream-signalen verder stilleggen. In preklinische modellen en vroege klinische studies hebben deze combinaties geleid tot diepere en duurzamere responsen, ook bij hersenmetastasen. Onderzoekers onderzoeken ook of het toevoegen van KRAS-remmers aan bestraling tumoren kan sensitiveren, zodat lagere bestralingdoses mogelijk zijn terwijl de controle in de hersenen behouden blijft of verbetert.
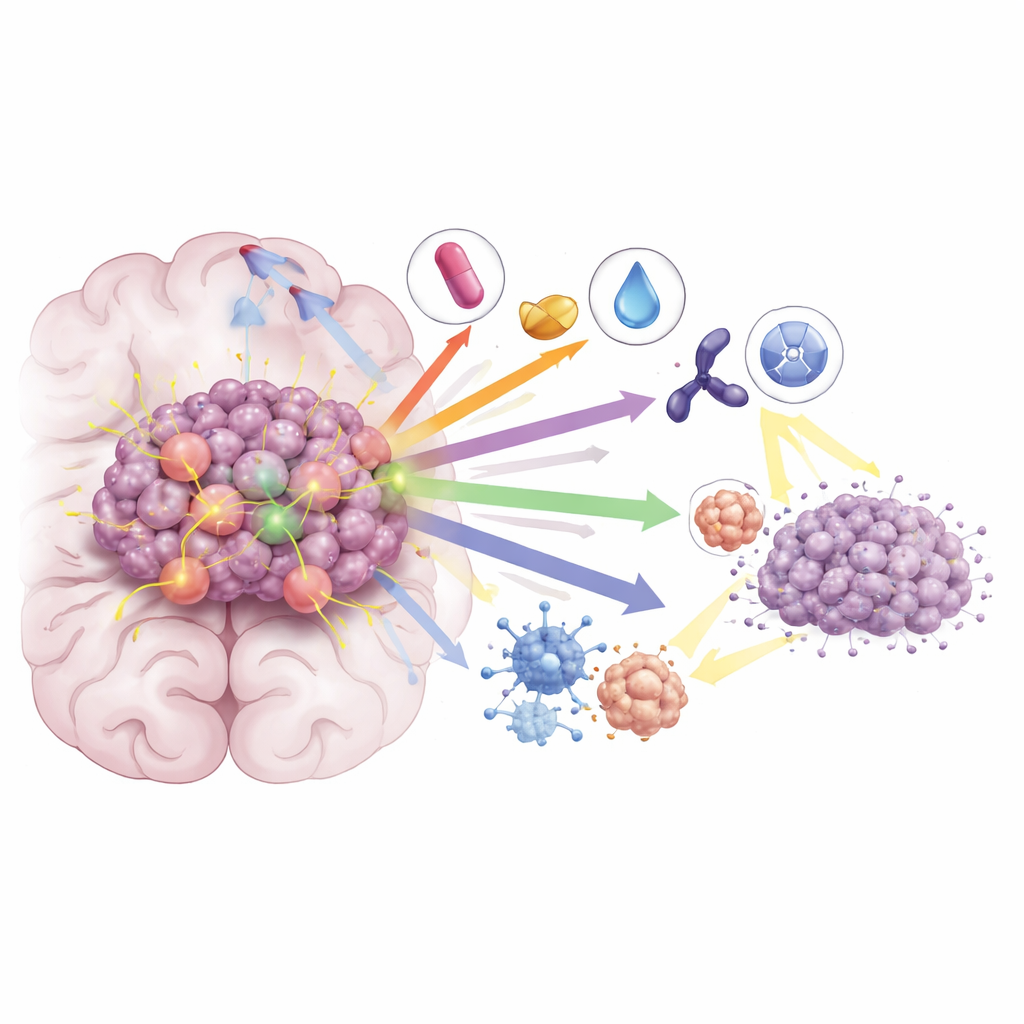
Wat dit betekent voor de toekomst
Al met al concludeert het artikel dat KRAS G12C niet langer een onaantastbaar doelwit is. Een groeiende gereedschapskist van hersendoordringende remmers, vooral wanneer ze bedachtzaam worden gecombineerd met immunotherapie, andere gerichte middelen en bestraling, begint het vooruitzicht voor NSCLC-patiënten met hersenmetastasen te veranderen. Hoewel uitdagingen blijven — met name geneesmiddelresistentie en de behoefte aan langduriger voordeel — betogen de auteurs dat rationele combinatiestrategieën die zowel de kankercel als zijn omringende omgeving aanspreken de beste kans bieden om kortdurende responsen om te zetten in duurzamere ziektecontrole en langere overleving.
Bronvermelding: Bhattacharya, D., Roman, B. & Reddy, S. Therapeutic advances with KRASG12C inhibitors and combination strategies in non-small cell lung cancer brain metastases. Cancer Gene Ther 33, 323–337 (2026). https://doi.org/10.1038/s41417-026-01003-0
Trefwoorden: KRAS G12C, niet-kleincellig longkanker, hersenmetastasen, gerichte therapie, combinaties met immunotherapie