Clear Sky Science · ru
Терапевтические достижения с ингибиторами KRASG12C и комбинированные стратегии при метастазах немелкоклеточного рака легкого в мозг
Почему это важно для пациентов и их семей
Метастазы в мозг при раке легкого часто оказываются разрушительными: они приводят к тяжёлым неврологическим нарушениям и короткой продолжительности жизни. В этой статье рассматривается новая волна точечных препаратов, направленных на специфическое генетическое изменение — KRAS G12C — при немелкоклеточном раке легкого (НМРЛ). Эти препараты созданы не только для уменьшения лёгочных опухолей, но и для проникновения в мозг и борьбы с метастазами там — область, в которой старые химиотерапии и многие таргетные препараты испытывали трудности. Для пациентов и их близких это направление работы означает более эффективные, более длительные и лучше адаптированные к биологии каждого конкретного рака варианты лечения.
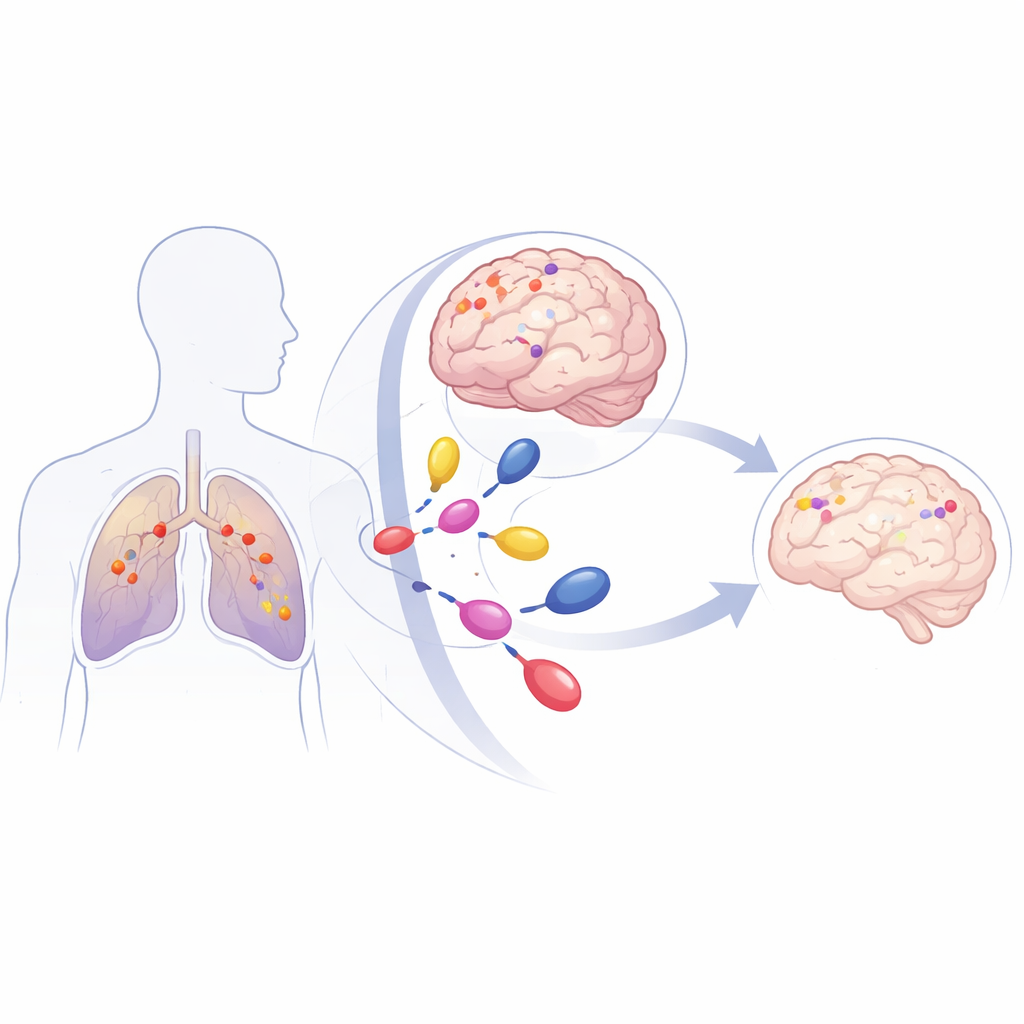
Распространённый рак легкого с опасным сценарием
НМРЛ — самая распространённая форма рака легкого и одна из ведущих причин смертности от рака. У части пациентов — до 40% — развиваются метастазы в мозг, которые сложно лечить, поскольку они находятся за защитным фильтром мозга — гематоэнцефалическим барьером. Во многих опухолях НМРЛ обнаруживаются мутации в гене KRAS, который действует как застрявшая педаль газа для роста клеток. Один конкретный вариант, KRAS G12C, составляет около 40% всех опухолей с мутацией KRAS. У пациентов с этой мутацией высокий риск раннего появления метастаз в мозг, а традиционные методы, такие как облучение всего мозга или фокусированная радиохирургия, обычно контролируют болезнь лишь в течение нескольких месяцев.
Как KRAS G12C подпитывает рост опухоли
В норме KRAS переключается между состояниями «включено» и «выключено», регулируя сигналы клетки для роста, выживания и метаболизма. Мутация G12C фиксирует KRAS в активной форме, постоянно передавая сигналы роста через ключевые пути, которые стимулируют деление клеток, устойчивость к гибели, формирование новых сосудов и создание иммунной супрессивной среды вокруг опухоли. Такое постоянное сигнализирование не только ускоряет рост опухоли в легком, но и помогает раковым клеткам распространяться и адаптироваться к новым местам, таким как мозг. Сопутствующие мутации в других генах — например, CDKN2A, KEAP1, LKB1 и SMARCA4 — могут делать опухоли ещё более агрессивными и способными к рецидиву в мозге после локальных вмешательств.
Новые препараты, которые достигают мозга
Долгое время KRAS считался «неприступным» для лекарств, но теперь несколько классов малых молекул специально нацелены на KRAS G12C. Некоторые связываются с неактивной формой белка и удерживают его выключенным, тогда как новые препараты также нацелены на активную форму. Такие лекарства, как сотораasib и адраграсиб, первыми вышли в клинику и показали явную пользу при прогрессирующем НМРЛ, в том числе у пациентов с метастазами в мозг. В частности, адраграсиб имеет веские доказательства способности проникать через гематоэнцефалический барьер и вызывать уменьшение ранее не леченных мозговых очагов у существенной доли пациентов, многие из которых достигали нескольких месяцев контролируемого внутричерепного заболевания. Препараты следующего поколения — например, оломорасиб, фульзерасиб, гарсорасиб, диварасиб, D3S-001 и RMC‑6236 — тестируются на предмет большей активности, лучшей проницаемости для мозга и расширенной эффективности против разных вариантов мутаций KRAS.
Объединение усилий для преодоления резистентности
Даже при этих достижениях у большинства пациентов, получающих только ингибиторы KRAS G12C, болезнь прогрессирует снова в течение нескольких месяцев. В обзоре показано, как опухоли приспосабливаются — через вторичные мутации KRAS, реактивацию путей роста и изменения в микроокружении опухоли — и описываются комбинированные стратегии, направленные на блокирование этих путей ухода. Сочетание ингибиторов KRAS с иммунотерапией может усилить атаку иммунной системы на опухоли, а комбинации с препаратами, нацеленными на MEK, CDK4/6 или SHP2, дополнительно отключают сигналы вниз по каскаду. В доклинических моделях и ранних клинических исследованиях такие сочетания приводили к более глубоким и более длительным ответам, в том числе при метастазах в мозг. Исследователи также проверяют, может ли добавление ингибиторов KRAS к облучению повысить чувствительность опухолей, что позволит использовать меньшие дозы радиации при сохранении или улучшении контроля в мозге.
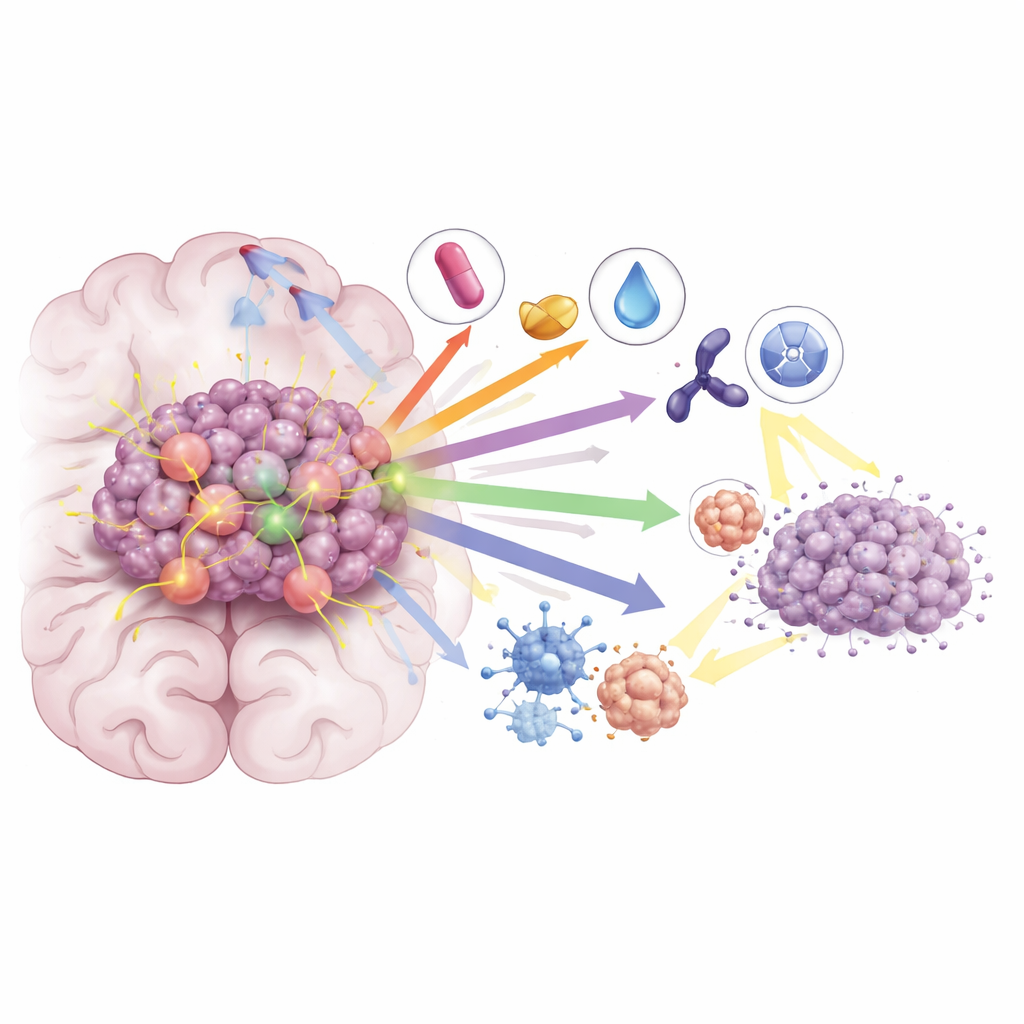
Что это значит для будущего
В целом статья делает вывод, что KRAS G12C перестал быть недосягаемой мишенью. Растущий набор ингибиторов с проникновением в мозг, особенно при продуманном сочетании с иммунотерапией, другими таргетными препаратами и радиотерапией, начинает менять прогноз для пациентов с НМРЛ и метастазами в мозг. Хотя остаются проблемы — в частности лекарственная резистентность и необходимость более длительного эффекта — авторы утверждают, что рационально подобранные комбинационные стратегии, нацеленные как на саму раковую клетку, так и на её окружение, предлагают наилучшие шансы превратить кратковременные ответы в более длительный контроль болезни и увеличение выживаемости.
Цитирование: Bhattacharya, D., Roman, B. & Reddy, S. Therapeutic advances with KRASG12C inhibitors and combination strategies in non-small cell lung cancer brain metastases. Cancer Gene Ther 33, 323–337 (2026). https://doi.org/10.1038/s41417-026-01003-0
Ключевые слова: KRAS G12C, немелкоклеточный рак легкого, метастазы в мозг, таргетная терапия, комбинации с иммунотерапией