Clear Sky Science · fr
Progrès thérapeutiques avec des inhibiteurs de KRASG12C et stratégies combinées dans les métastases cérébrales du cancer du poumon non à petites cellules
Pourquoi cela importe pour les patients et leurs familles
Les métastases cérébrales d’un cancer du poumon sont souvent dévastatrices, entraînant de graves troubles neurologiques et une espérance de vie réduite. Cet article passe en revue une nouvelle vague de médicaments de précision ciblant une altération génétique spécifique, KRAS G12C, dans le cancer du poumon non à petites cellules (CPNPC). Ces médicaments sont conçus non seulement pour réduire les tumeurs pulmonaires, mais aussi pour traverser le cerveau et attaquer les tumeurs métastatiques — un domaine où les chimiothérapies anciennes et de nombreux traitements ciblés ont peiné. Pour les patients et leurs proches, ces travaux ouvrent la voie à des plans de traitement plus efficaces, plus durables et mieux adaptés à la biologie de la tumeur de chaque personne.
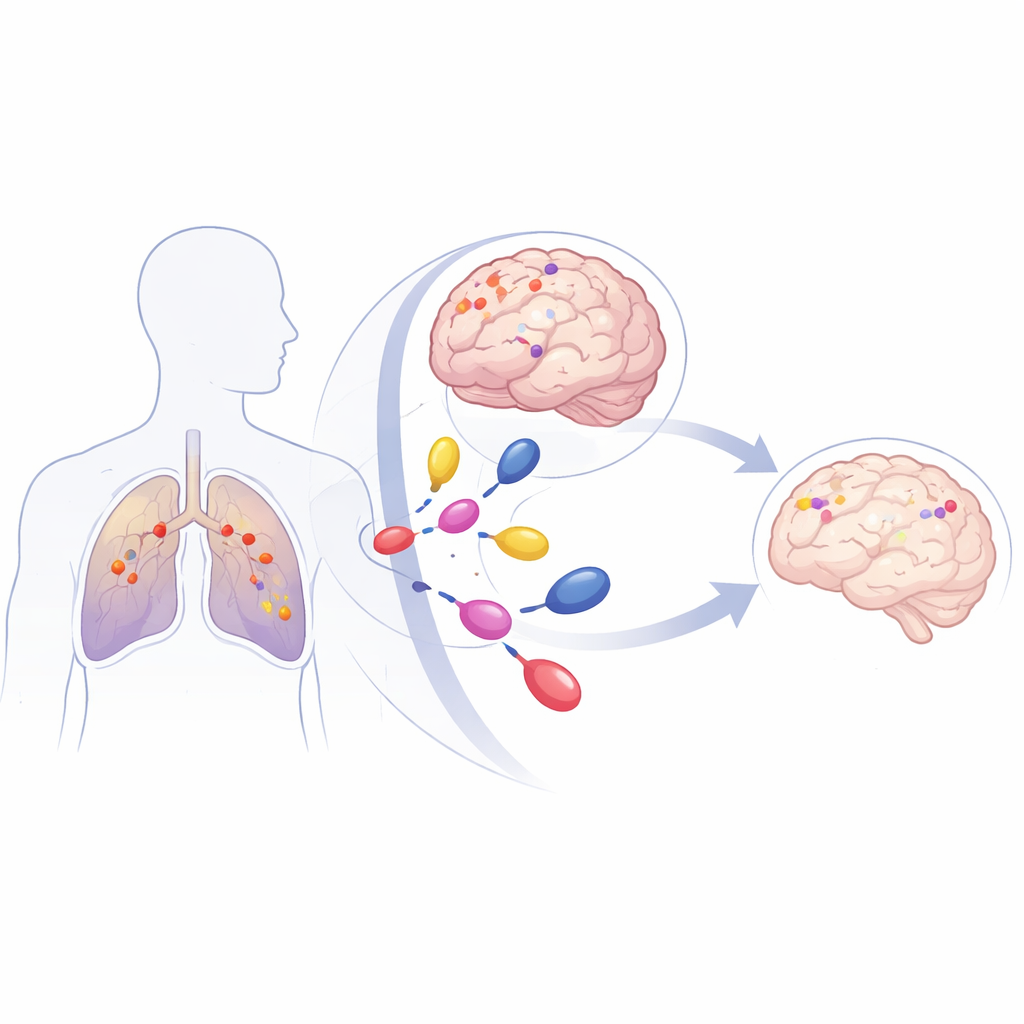
Un cancer du poumon fréquent avec un schéma dangereux
Le CPNPC est la forme la plus fréquente de cancer du poumon et une cause majeure de mortalité par cancer. Jusqu’à 40 % des patients développeront des métastases cérébrales, difficiles à traiter car elles se situent derrière le filtre protecteur du cerveau, la barrière hémato-encéphalique. De nombreuses tumeurs de CPNPC portent des mutations du gène KRAS, qui agit comme un accélérateur bloqué de la croissance cellulaire. Une variante particulière, appelée KRAS G12C, représente environ 40 % des CPNPC à mutation KRAS. Les patients porteurs de cette mutation ont un risque élevé de développer précocement des métastases cérébrales, et les traitements traditionnels tels que la radiothérapie cérébrale totale ou la radiochirurgie focalisée contrôlent généralement la maladie pendant seulement quelques mois.
Comment KRAS G12C alimente la croissance tumorale
KRAS bascule normalement entre des états « activé » et « inactivé » pour réguler les signaux cellulaires de croissance, de survie et de métabolisme. La mutation G12C bloque KRAS dans sa forme active, envoyant en continu des signaux de croissance via des voies majeures qui favorisent la division cellulaire, la résistance à la mort cellulaire, la néoangiogenèse et un environnement immunosuppresseur autour de la tumeur. Cette signalisation constante accélère non seulement la croissance tumorale pulmonaire, mais aide aussi les cellules cancéreuses à se propager et à s’adapter à de nouveaux sites comme le cerveau. Des co-mutations dans d’autres gènes, tels que CDKN2A, KEAP1, LKB1 et SMARCA4, peuvent rendre les tumeurs encore plus agressives et plus susceptibles de récidiver au niveau cérébral après des traitements locaux.
Nouveaux médicaments qui atteignent le cerveau
Pendant des décennies, KRAS a été considéré comme « impossible à cibler », mais plusieurs classes de petites molécules ciblent maintenant spécifiquement KRAS G12C. Certaines se lient à la forme inactive de la protéine et la maintiennent éteinte, tandis que des agents plus récents ciblent aussi la forme active. Des médicaments tels que sotorasib et adagrasib ont été les premiers à parvenir en clinique et ont montré un bénéfice net dans le CPNPC avancé, y compris chez des patients ayant des métastases cérébrales. L’adagrasib, en particulier, présente des preuves solides de traversée de la barrière hémato-encéphalique et provoque la régression de lésions cérébrales non traitées chez une fraction substantielle de patients, beaucoup obtenant plusieurs mois de contrôle intracrânien. Des agents de nouvelle génération — comme olomorasib, fulzerasib, garsorasib, divarasib, D3S-001 et RMC‑6236 — sont en essai pour une plus grande puissance, une meilleure pénétration cérébrale et une activité plus large contre diverses mutations KRAS.
Combiner les forces pour surmonter la résistance
Même avec ces progrès, la plupart des patients traités uniquement par des inhibiteurs de KRAS G12C voient leur cancer progresser de nouveau en quelques mois. La revue souligne comment les tumeurs s’adaptent — par des mutations secondaires de KRAS, la réactivation de voies de croissance et des modifications de l’environnement tumoral — et décrit des stratégies combinatoires conçues pour bloquer ces voies d’échappement. Associer les inhibiteurs de KRAS à l’immunothérapie peut renforcer l’attaque immunitaire contre les tumeurs, tandis que des combinaisons avec des médicaments ciblant MEK, CDK4/6 ou SHP2 ferment davantage la signalisation en aval. Dans des modèles précliniques et des premières études cliniques, ces combinaisons ont conduit à des réponses plus profondes et plus durables, y compris dans les métastases cérébrales. Les chercheurs évaluent aussi si l’ajout d’inhibiteurs de KRAS à la radiothérapie peut sensibiliser les tumeurs, permettant d’utiliser des doses de radiation plus faibles tout en maintenant ou en améliorant le contrôle au niveau cérébral.
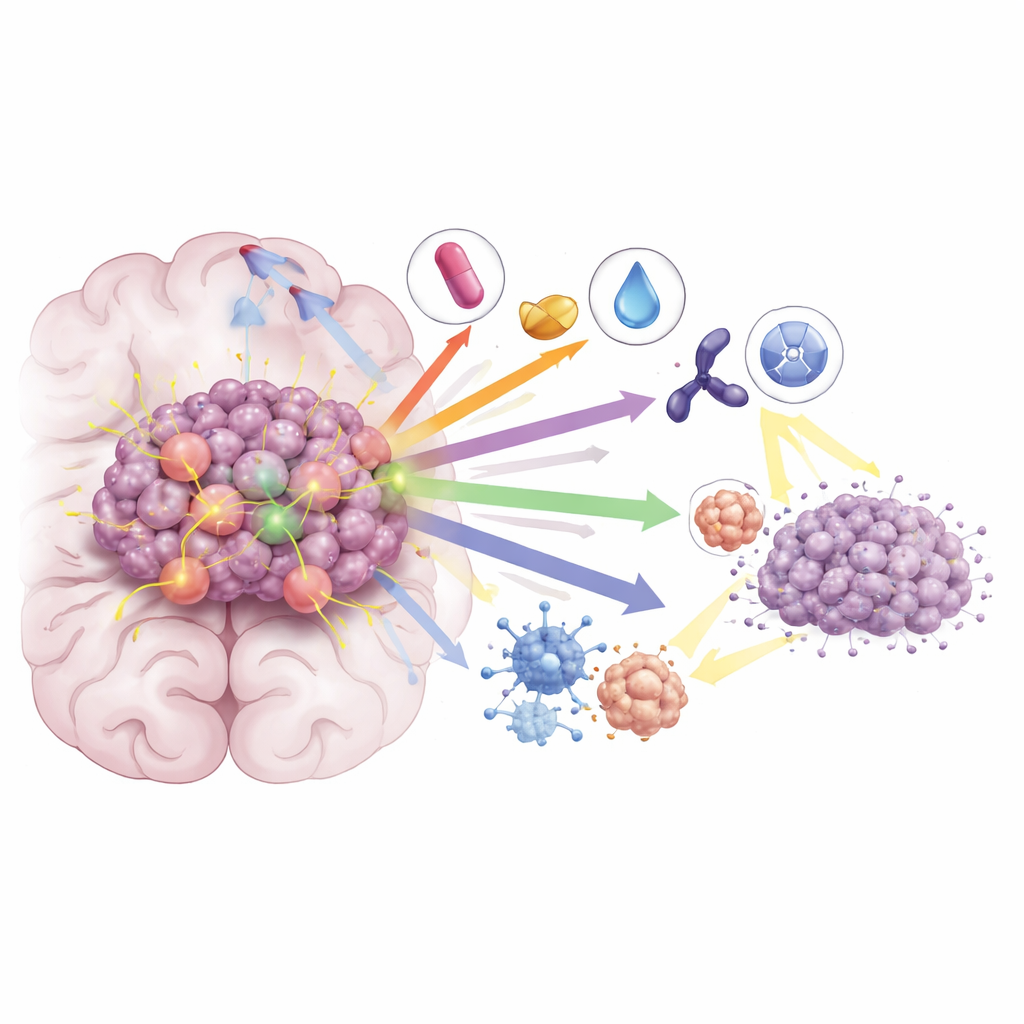
Quelles implications pour l’avenir
Dans l’ensemble, l’article conclut que KRAS G12C n’est plus une cible intouchable. Une boîte à outils croissante d’inhibiteurs pénétrant le cerveau, surtout lorsqu’ils sont combinés de manière réfléchie avec l’immunothérapie, d’autres médicaments ciblés et la radiothérapie, commence à modifier le pronostic des patients atteints de CPNPC avec métastases cérébrales. Si des défis demeurent — en particulier la résistance aux médicaments et le besoin d’une efficacité plus durable — les auteurs soutiennent que des stratégies combinatoires rationnelles, ciblant à la fois la cellule cancéreuse et son micro-environnement, offrent la meilleure chance de transformer des réponses de courte durée en un contrôle plus durable de la maladie et en une survie prolongée.
Citation: Bhattacharya, D., Roman, B. & Reddy, S. Therapeutic advances with KRASG12C inhibitors and combination strategies in non-small cell lung cancer brain metastases. Cancer Gene Ther 33, 323–337 (2026). https://doi.org/10.1038/s41417-026-01003-0
Mots-clés: KRAS G12C, cancer du poumon non à petites cellules, métastases cérébrales, thérapie ciblée, combinaisons avec immunothérapie