Clear Sky Science · tr
KRASG12C inhibitörleri ve kombinasyon stratejileri ile küçük hücre dışı akciğer kanserinde beyin metastazlarına yönelik terapötik ilerlemeler
Hastalar ve Aileler İçin Neden Önemli
Akciğer kanserinden kaynaklanan beyin metastazları sıklıkla yıkıcıdır; ciddi nörolojik sorunlara yol açar ve yaşam beklentisini kısaltır. Bu makale, küçük hücre dışı akciğer kanserinde (KHDAK) belirli bir genetik değişikliği, KRAS G12C’yi hedef alan yeni nesil kişiselleştirilmiş ilaçları gözden geçiriyor. Bu ilaçlar yalnızca akciğer tümörlerini küçültmeyi amaçlamakla kalmıyor; aynı zamanda beyne geçip oradaki metastatik tümörlere saldıracak şekilde tasarlanmışlar — eskiden birçok kemoterapi ve hedefe yönelik ilacın zorlandığı bir alan. Hastalar ve aileler açısından bu çalışmalar, daha etkili, daha kalıcı ve her bireyin kanser biyolojisine daha iyi uyarlanmış tedavi planlarına işaret ediyor.
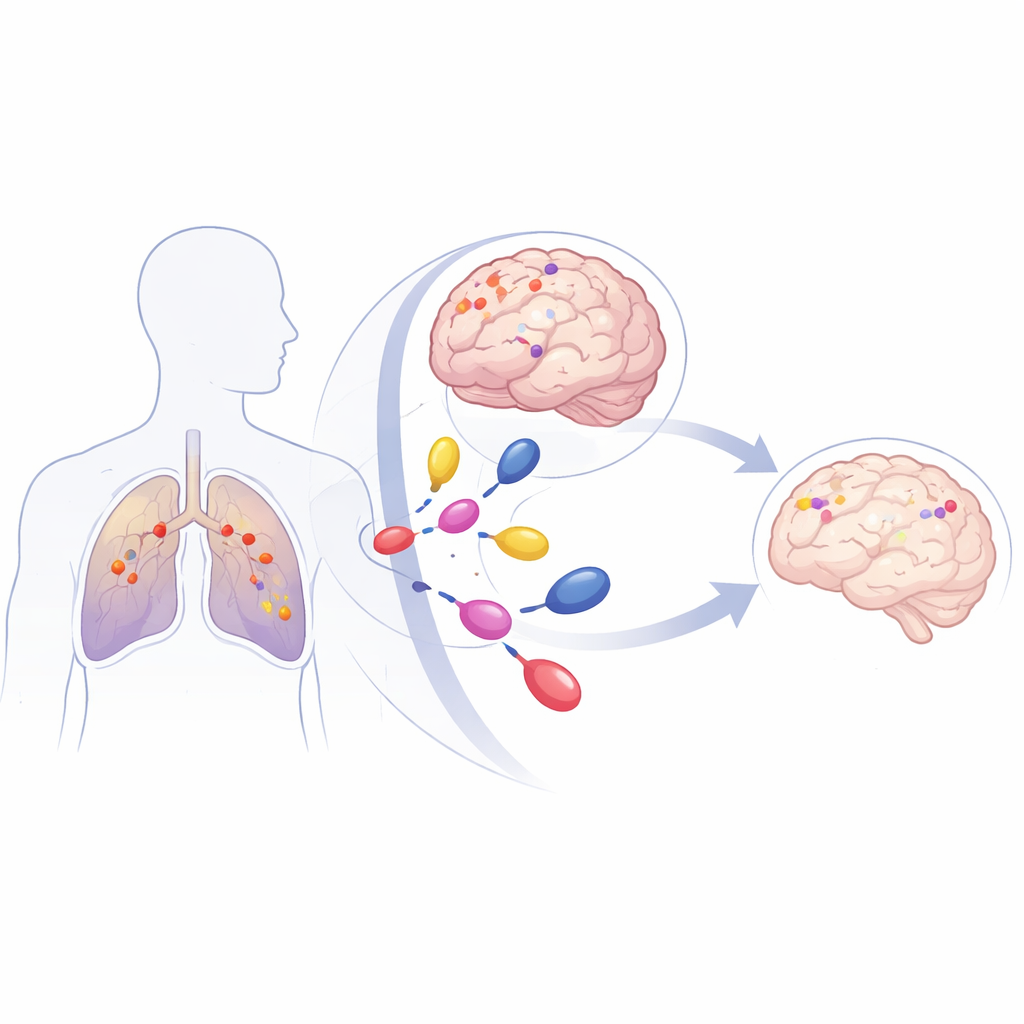
Yaygın Bir Akciğer Kanseri ve Tehlikeli Bir Seyir
KHDAK, akciğer kanserlerinin en yaygın biçimidir ve kanser ölümlerinin önde gelen nedenlerinden biridir. Hastaların %40’a varanı beyin metastazı geliştirebilir; bunlar kan–beyin bariyerinin arkasında yer aldıkları için tedavisi zordur. Birçok KHDAK tümörü, hücre büyümesi için sürekli gaz veren bir rol oynayan KRAS adlı bir gende mutasyon taşır. KRAS G12C adlı özel bir versiyon, KRAS-müta nt KHDAK’larının yaklaşık %40’ını oluşturur. Bu mutasyona sahip hastalar, hastalık seyri sırasında erken dönemde beyin metastazı geliştirme riski yüksektir ve tüm beyin ışınlaması veya odaklanmış radyocerrahi gibi geleneksel tedaviler genellikle hastalığı sadece birkaç ay kontrol altında tutar.
KRAS G12C’nin Tümör Büyümesini Nasıl Desteklediği
KRAS normalde büyüme, hayatta kalma ve metabolizmayı düzenlemek için “açık” ve “kapalı” durumlar arasında geçiş yapar. G12C mutasyonu KRAS’ı aktif formunda kilitler ve sürekli olarak hücre bölünmesini, hücre ölümü dirençliliğini, yeni damar oluşumunu ve tümör çevresinde bağışıklık baskılayıcı bir ortamı teşvik eden ana yolaklara büyüme sinyalleri gönderir. Bu sürekli sinyal verme yalnızca akciğerdeki tümör büyümesini hızlandırmakla kalmaz, aynı zamanda kanser hücrelerinin yayılmasını ve beyin gibi yeni alanlara uyum sağlamasını kolaylaştırır. CDKN2A, KEAP1, LKB1 ve SMARCA4 gibi diğer genlerdeki birlikte görülen mutasyonlar tümörleri daha agresif hale getirebilir ve yerel tedaviler sonrası beyinde nüks olasılığını artırabilir.
Beyne Ulaşan Yeni İlaçlar
On yıllarca KRAS “ilaçlanamaz” kabul edildi, ancak şimdi birkaç küçük molekül sınıfı KRAS G12C’yi spesifik olarak hedefliyor. Bazıları proteinin inaktif formuna bağlanarak onu kapalı tutarken, daha yeni ajanlar aktif formu da hedefliyor. Sotorasib ve adagrasib gibi ilaçlar kliniklere ilk ulaşanlar oldu ve ileri KHDAK’ta, beyin metastazı olan hastalar da dahil olmak üzere, belirgin fayda gösterdiler. Özellikle adagrasib’in kan–beyin bariyerini geçtiğine dair güçlü kanıtlar vardır ve tedavi edilmemiş beyin lezyonlarında belirgin bir hasta kesiminde küçülme sağladığı, birçok hastada aylar süren kontrol altında intrakraniyal hastalık elde edildiği gösterilmiştir. Olomorasib, fulzerasib, garsorasib, divarasib, D3S-001 ve RMC‑6236 gibi sonraki nesil ajanlar daha yüksek etkinlik, daha iyi beyin penetrasyonu ve çeşitli KRAS mutasyonlarına karşı daha geniş aktivite için test ediliyor.
Dirençle Başa Çıkmak İçin Güçlerin Birleştirilmesi
Bu ilerlemelere rağmen, KRAS G12C inhibitörleri tek başına tedavi edilen hastaların çoğunda kanser birkaç ay içinde yeniden ilerler. Derleme, tümörlerin ikincil KRAS mutasyonları, büyüme yolaklarının yeniden aktive olması ve tümör çevresindeki değişiklikler yoluyla nasıl uyum sağladığını vurguluyor; bu kaçış yollarını kapatmayı amaçlayan kombinasyon stratejilerini tanımlıyor. KRAS inhibitörlerini immünoterapi ile eşleştirmek bağışıklık sisteminin tümörlere saldırısını güçlendirebilirken, MEK, CDK4/6 veya SHP2’yi hedef alan ilaçlarla yapılan kombinasyonlar aşağı akış sinyalini daha da kapatır. Preklinik modellerde ve erken klinik çalışmalarda bu kombinasyonlar daha derin ve daha dayanıklı yanıtlar sağladı; bunlar arasında beyin metastazları da yer alıyor. Araştırmacılar ayrıca KRAS inhibitörlerinin radyasyonla birlikte eklenmesinin tümörleri hassaslaştırıp hassaslaştırmadığını test ediyor; böylece beyindeki kontrolü korurken veya iyileştirirken daha düşük radyasyon dozlarının kullanılabilmesi hedefleniyor.
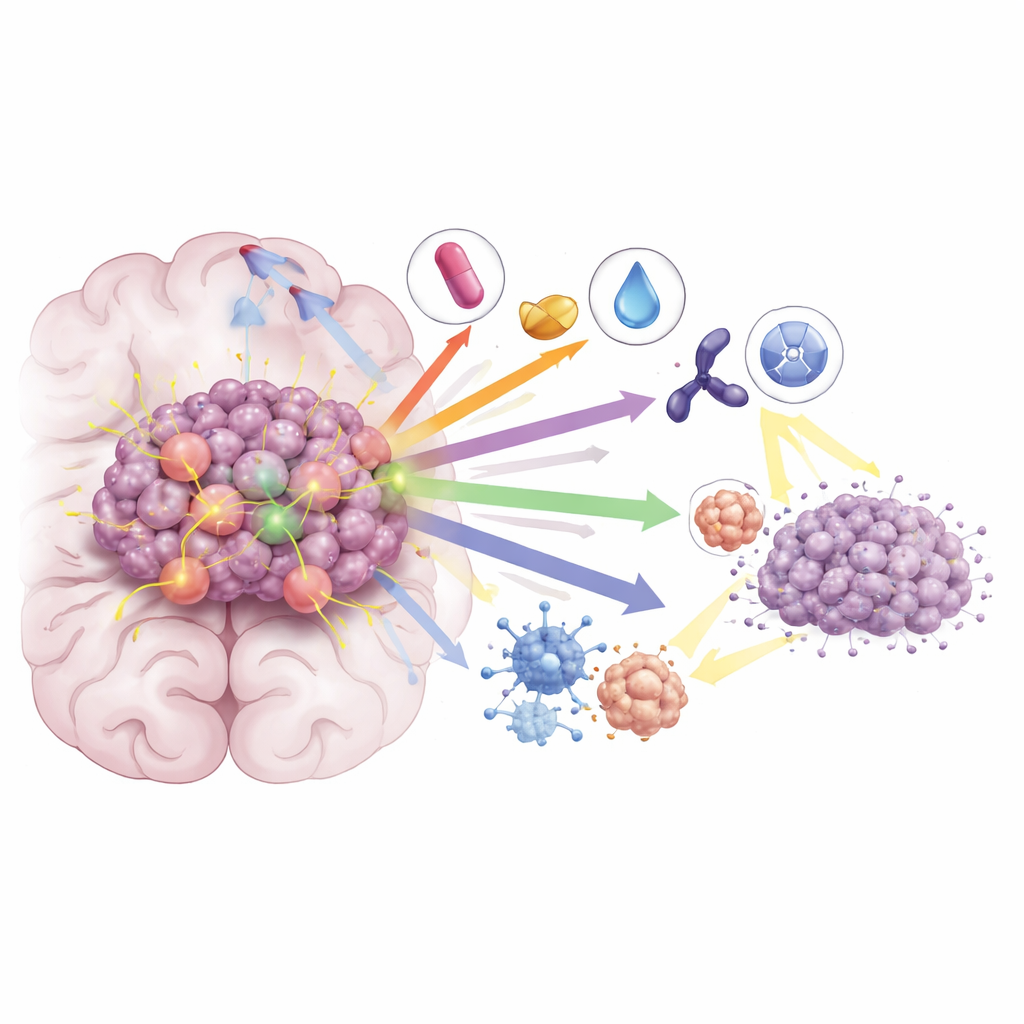
Gelecek İçin Anlamı
Genel olarak makale, KRAS G12C’nin artık dokunulmaz bir hedef olmadığını sonucuna varıyor. Beyne geçen inhibitörlerin büyüyen bir araç kutusu, özellikle immünoterapi, diğer hedefe yönelik ilaçlar ve radyasyonla akıllıca kombinasyonlandığında, beyin metastazı olan KHDAK hastalarının görünümünü değiştirmeye başlıyor. Zorluklar — özellikle ilaç direnci ve daha uzun süreli fayda ihtiyacı — devam etse de, yazarlar kanser hücresine ve çevresindeki ortama odaklanan rasyonel kombinasyon stratejilerinin kısa süreli yanıtları daha kalıcı hastalık kontrolü ve daha uzun sağkalım haline dönüştürme konusunda en iyi umut olduğunu savunuyor.
Atıf: Bhattacharya, D., Roman, B. & Reddy, S. Therapeutic advances with KRASG12C inhibitors and combination strategies in non-small cell lung cancer brain metastases. Cancer Gene Ther 33, 323–337 (2026). https://doi.org/10.1038/s41417-026-01003-0
Anahtar kelimeler: KRAS G12C, küçük hücre dışı akciğer kanseri, beyin metastazları, hedefe yönelik tedavi, immünoterapi kombinasyonları