Clear Sky Science · es
Avances terapéuticos con inhibidores de KRAS G12C y estrategias combinadas en metástasis cerebrales de cáncer de pulmón no microcítico
Por qué esto importa para pacientes y familias
Las metástasis cerebrales procedentes de cáncer de pulmón suelen ser devastadoras, provocando graves problemas neurológicos y una expectativa de vida breve. Este artículo revisa una nueva ola de medicamentos de precisión que apuntan a un cambio genético específico, KRAS G12C, en el cáncer de pulmón no microcítico (CPNM). Estos fármacos están diseñados no solo para reducir los tumores pulmonares sino también para atravesar el cerebro y atacar las metástasis allí —un ámbito donde las quimioterapias antiguas y muchos fármacos dirigidos han tenido dificultades. Para pacientes y familias, este trabajo apunta hacia planes de tratamiento más efectivos, de mayor duración y mejor adaptados a la biología del cáncer de cada persona.
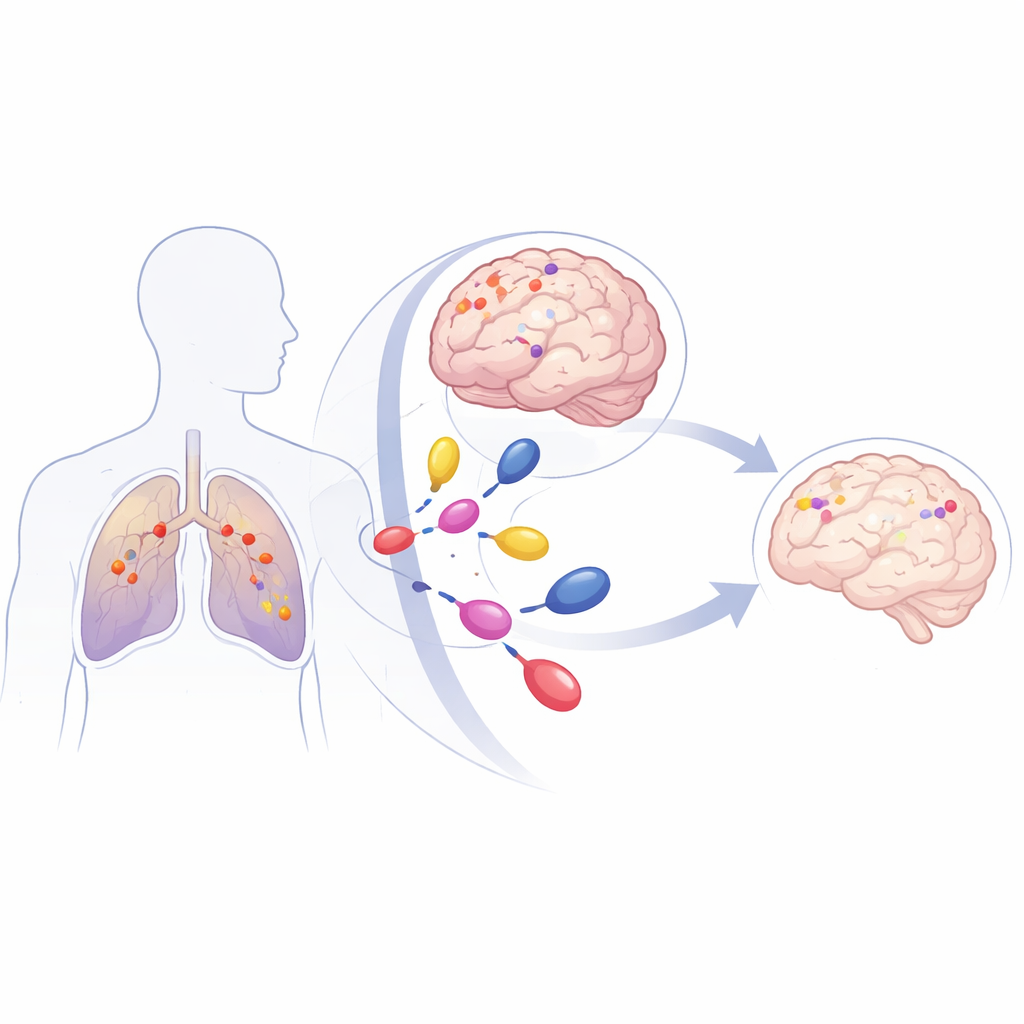
Un cáncer de pulmón común con un patrón peligroso
El CPNM es la forma más común de cáncer de pulmón y una de las principales causas de muerte por cáncer. Hasta un 40 % de los pacientes desarrollará metástasis en el cerebro, que son difíciles de tratar porque se encuentran detrás del filtro protector del cerebro, la barrera hematoencefálica. Muchos tumores de CPNM portan mutaciones en un gen llamado KRAS, que actúa como un acelerador atascado para el crecimiento celular. Una versión particular, denominada KRAS G12C, representa alrededor del 40 % de los CPNM con mutación en KRAS. Los pacientes con esta mutación tienen un alto riesgo de desarrollar metástasis cerebrales temprano en el curso de su enfermedad, y los tratamientos tradicionales como la radiación cerebral total o la radiocirugía focal suelen controlar la enfermedad solo durante unos meses.
Cómo KRAS G12C impulsa el crecimiento tumoral
KRAS normalmente alterna entre estados de “encendido” y “apagado” para regular las señales celulares de crecimiento, supervivencia y metabolismo. La mutación G12C bloquea a KRAS en su forma activa, enviando de forma continua señales de crecimiento a través de vías principales que favorecen la división celular, la resistencia a la muerte celular, la formación de nuevos vasos sanguíneos y un entorno inmunosupresor alrededor del tumor. Esta señalización constante no solo acelera el crecimiento tumoral en el pulmón, sino que también ayuda a las células cancerosas a diseminarse y adaptarse a nuevos sitios como el cerebro. Co-mutations en otros genes, como CDKN2A, KEAP1, LKB1 y SMARCA4, pueden hacer los tumores aún más agresivos y con mayor probabilidad de recurrir en el cerebro tras tratamientos locales.
Nuevos fármacos que alcanzan el cerebro
Durante décadas, KRAS se consideró “indefinible” para fármacos, pero varias clases de pequeñas moléculas ahora apuntan específicamente a KRAS G12C. Algunas se unen a la forma inactiva de la proteína y la mantienen apagada, mientras que agentes más recientes también atacan la forma activa. Fármacos como sotorasib y adagrasib fueron los primeros en llegar a la clínica y han mostrado un beneficio claro en CPNM avanzado, incluidos pacientes con metástasis cerebrales. Adagrasib, en particular, cuenta con evidencia sólida de que cruza la barrera hematoencefálica y provoca reducción de lesiones cerebrales no tratadas en una fracción sustancial de pacientes, con muchos logrando meses de control intracraneal. Agentes de nueva generación —como olomorasib, fulzerasib, garsorasib, divarasib, D3S-001 y RMC‑6236— se están evaluando por su mayor potencia, mejor penetración cerebral y actividad más amplia frente a diversas mutaciones de KRAS.
Unir fuerzas para superar la resistencia
Incluso con estos avances, la mayoría de los pacientes tratados solo con inhibidores de KRAS G12C ven su cáncer progresar de nuevo en varios meses. La revisión destaca cómo los tumores se adaptan —mediante mutaciones secundarias en KRAS, reactivación de vías de crecimiento y cambios en el microentorno tumoral— y describe estrategias combinadas diseñadas para bloquear estas rutas de escape. Asociar inhibidores de KRAS con inmunoterapia puede potenciar el ataque inmunitario contra los tumores, mientras que las combinaciones con fármacos que inhiben MEK, CDK4/6 o SHP2 cierran aún más la señalización downstream. En modelos preclínicos y en estudios clínicos tempranos, estas combinaciones han llevado a respuestas más profundas y duraderas, incluso en metástasis cerebrales. Los investigadores también están probando si añadir inhibidores de KRAS a la radiación puede sensibilizar los tumores, permitiendo dosis de radiación más bajas mientras se mantiene o mejora el control en el cerebro.
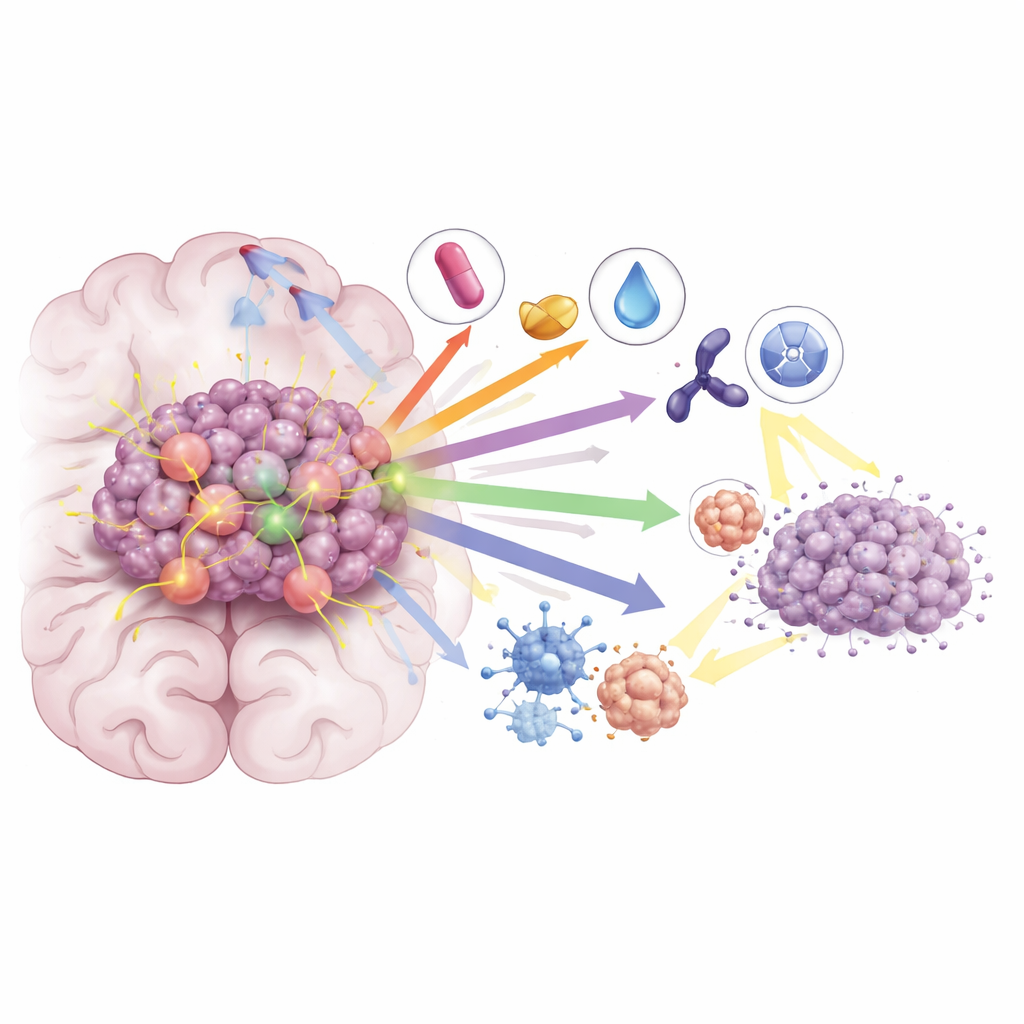
Qué significa esto para el futuro
En conjunto, el artículo concluye que KRAS G12C ya no es un objetivo inalcanzable. Un conjunto creciente de inhibidores con penetración cerebral, especialmente cuando se combinan de forma racional con inmunoterapia, otros fármacos dirigidos y radiación, está empezando a cambiar el pronóstico de los pacientes con CPNM y metástasis cerebrales. Aunque persisten desafíos —particularmente la resistencia a los medicamentos y la necesidad de beneficios más duraderos—, los autores sostienen que las estrategias combinadas basadas en la biología tanto de la célula tumoral como de su entorno ofrecen la mejor esperanza para convertir respuestas de corta duración en un control más sostenido de la enfermedad y una supervivencia mayor.
Cita: Bhattacharya, D., Roman, B. & Reddy, S. Therapeutic advances with KRASG12C inhibitors and combination strategies in non-small cell lung cancer brain metastases. Cancer Gene Ther 33, 323–337 (2026). https://doi.org/10.1038/s41417-026-01003-0
Palabras clave: KRAS G12C, cáncer de pulmón no microcítico, metástasis cerebrales, terapia dirigida, combinaciones con inmunoterapia