Clear Sky Science · pl
Postępy terapeutyczne z inhibitorami KRASG12C i strategią łączenia terapii w przerzutach do mózgu z niedrobnokomórkowego raka płuca
Dlaczego to ma znaczenie dla pacjentów i ich rodzin
Przerzuty do mózgu z raka płuca często mają niszczący wpływ — prowadzą do poważnych zaburzeń neurologicznych i krótkiego czasu przeżycia. Artykuł ten omawia nową falę leków precyzyjnych, które celują w określoną zmianę genetyczną KRAS G12C w niedrobnokomórkowym raku płuca (NSCLC). Leki te zostały zaprojektowane nie tylko po to, by zmniejszać guzy płucne, lecz także przenikać do mózgu i atakować tam przerzuty — obszar, w którym starsze chemioterapie i wiele terapii celowanych miało ograniczoną skuteczność. Dla pacjentów i rodzin oznacza to perspektywę planów leczenia, które są skuteczniejsze, trwalsze i lepiej dopasowane do biologii nowotworu danego pacjenta.
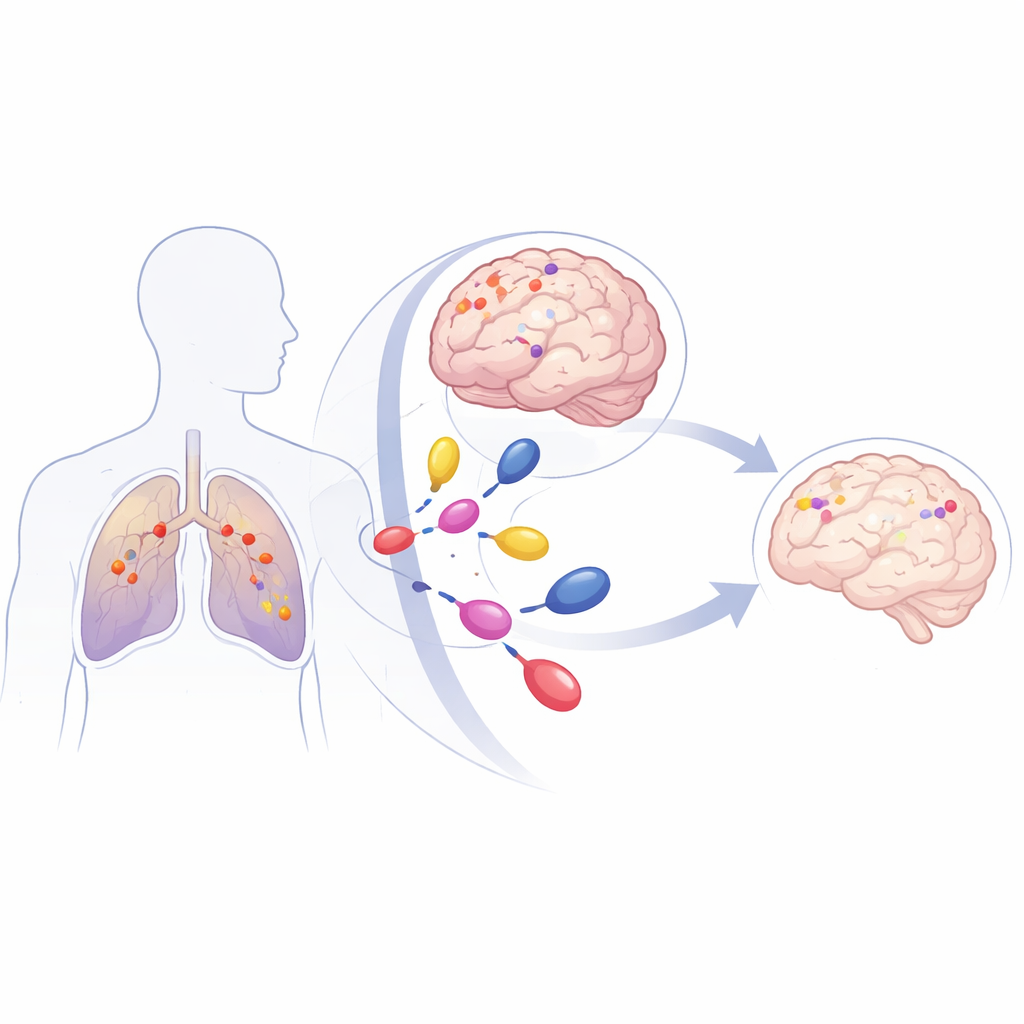
Najczęstszy rak płuca z niebezpiecznym schematem rozwoju
NSCLC jest najczęstszą postacią raka płuca i jedną z głównych przyczyn zgonów z powodu nowotworów. U nawet 40% pacjentów rozwijają się przerzuty do mózgu, które trudno leczyć, ponieważ znajdują się za ochronną barierą mózgowo-naczyniową. Wiele guzów NSCLC niesie mutacje w genie KRAS, który działa jak „zatarty pedał przyspieszenia” dla wzrostu komórek. Jedna z odmian, KRAS G12C, stanowi około 40% przypadków raków NSCLC z mutacją KRAS. Pacjenci z tą mutacją mają wysokie ryzyko wczesnego rozwoju przerzutów do mózgu, a tradycyjne terapie, takie jak napromienianie całego mózgu czy stereotaktyczna radioterapia, zazwyczaj kontrolują chorobę tylko przez kilka miesięcy.
Jak KRAS G12C napędza wzrost guza
KRAS normalnie przełącza się między stanami „włączonym” i „wyłączonym”, regulując sygnały komórkowe związane z wzrostem, przeżyciem i metabolizmem. Mutacja G12C blokuje KRAS w aktywnej formie, stale wysyłając sygnały wzrostu przez główne szlaki promujące podziały komórek, oporność na apoptozę, tworzenie naczyń oraz środowisko immunosupresyjne wokół guza. To ciągłe sygnalizowanie nie tylko przyspiesza wzrost guza w płucu, lecz także pomaga komórkom nowotworowym rozprzestrzeniać się i adaptować do nowych miejsc, takich jak mózg. Współwystępujące mutacje w innych genach, takich jak CDKN2A, KEAP1, LKB1 czy SMARCA4, mogą sprawić, że nowotwory będą jeszcze bardziej agresywne i bardziej skłonne do nawrotów w mózgu po leczeniu miejscowym.
Nowe leki, które docierają do mózgu
Przez dekady KRAS uważano za „nieuleczalny”, jednak teraz kilka klas małych cząsteczek celuje specyficznie w KRAS G12C. Niektóre wiążą formę nieaktywną białka i utrzymują je w stanie wyłączonym, podczas gdy nowsze związki atakują także formę aktywną. Leki takie jak sotorasib i adagrasib były pierwszymi, które trafiły do kliniki i wykazały wyraźne korzyści u chorych z zaawansowanym NSCLC, w tym u pacjentów z przerzutami do mózgu. Adagrasib ma szczególnie mocne dowody na przenikanie bariery krew–mózg i powodowanie zmniejszenia nieleczonych zmian mózgowych u znaczącej części pacjentów, z wieloma osiągającymi miesiące kontroli choroby wewnątrzczaszkowej. Leki następnej generacji — takie jak olomorasib, fulzerasib, garsorasib, divarasib, D3S-001 i RMC‑6236 — są testowane pod kątem większej mocy działania, lepszego przenikania do mózgu i szerszej aktywności przeciw różnym mutacjom KRAS.
Łączenie sił, by pokonać oporność
Nawet w obliczu tych postępów większość pacjentów leczonych wyłącznie inhibitorami KRAS G12C doświadcza ponownego postępu choroby w ciągu kilku miesięcy. Przegląd opisuje, jak guzy adaptują się — przez wtórne mutacje KRAS, reaktywację szlaków wzrostu i zmiany w mikrośrodowisku guza — oraz przedstawia strategie łączenia terapii zaprojektowane, by zablokować te drogi ucieczki. Łączenie inhibitorów KRAS z immunoterapią może wzmocnić odpowiedź układu odpornościowego wobec guza, podczas gdy kombinacje z lekami celującymi MEK, CDK4/6 czy SHP2 dodatkowo wyłączają sygnalizację w dół szlaku. W modelach przedklinicznych i we wczesnych badaniach klinicznych takie kombinacje prowadziły do głębszych i trwalszych odpowiedzi, także w przerzutach mózgowych. Badacze sprawdzają też, czy dodanie inhibitorów KRAS do radioterapii może uwrażliwić guzy, pozwalając na stosowanie niższych dawek promieniowania przy zachowaniu lub poprawie kontroli w mózgu.
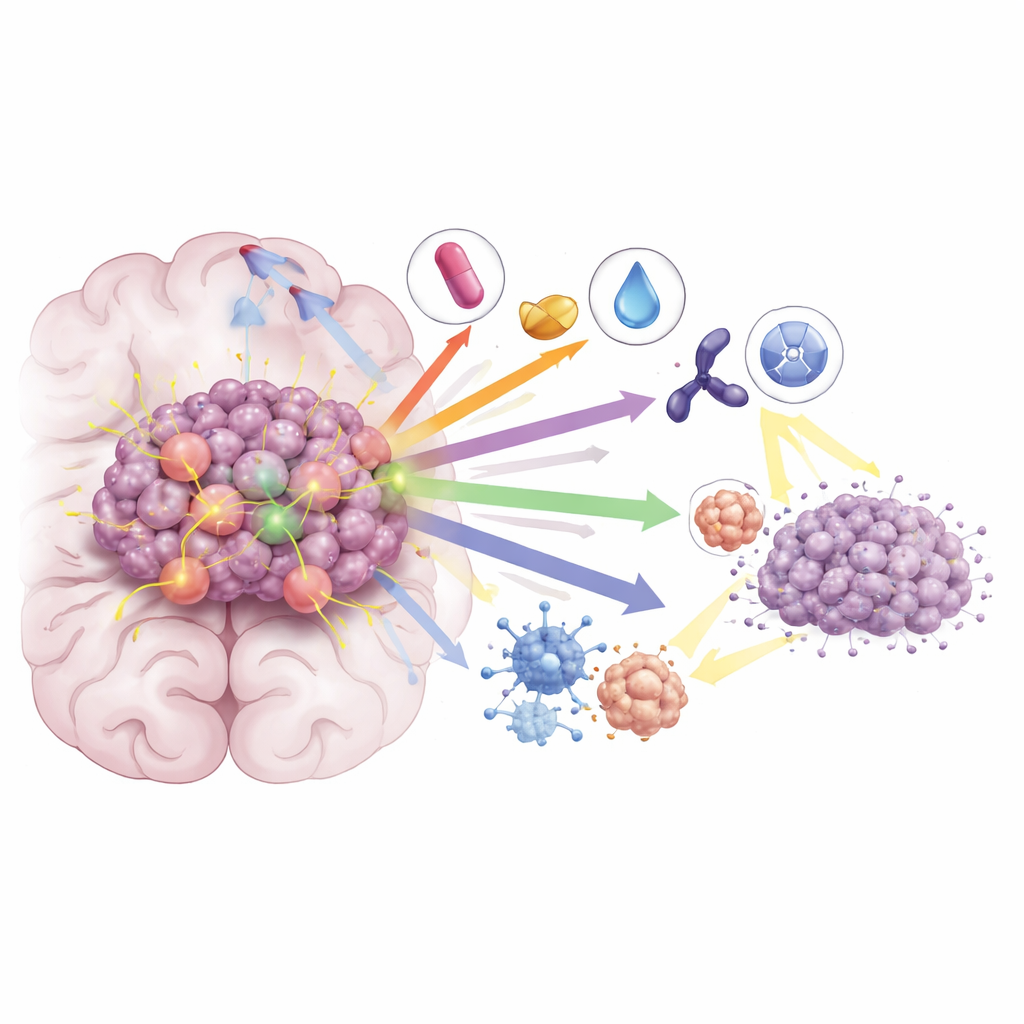
Co to oznacza na przyszłość
Ogólnie artykuł konkluduje, że KRAS G12C nie jest już celem niedostępnym. Rosnący zestaw inhibitorów przenikających do mózgu, zwłaszcza gdy są rozsądnie łączone z immunoterapią, innymi lekami celowanymi i radioterapią, zaczyna zmieniać perspektywy dla chorych z NSCLC z przerzutami do mózgu. Choć wyzwania pozostają — w szczególności oporność na leki i potrzeba dłużej utrzymujących się korzyści — autorzy argumentują, że racjonalne strategie łączone, skupione zarówno na komórce nowotworowej, jak i jej otoczeniu, oferują najlepszą nadzieję na przekształcenie krótkotrwałych odpowiedzi w trwalszą kontrolę choroby i dłuższe przeżycie.
Cytowanie: Bhattacharya, D., Roman, B. & Reddy, S. Therapeutic advances with KRASG12C inhibitors and combination strategies in non-small cell lung cancer brain metastases. Cancer Gene Ther 33, 323–337 (2026). https://doi.org/10.1038/s41417-026-01003-0
Słowa kluczowe: KRAS G12C, niedrobnokomórkowy rak płuca, przerzuty do mózgu, terapia celowana, kombinacje z immunoterapią