Clear Sky Science · zh
CpG岛甲基化表型减弱与WNT信号激活缺失限制Kras突变性肠道肿瘤发生
为何部分肠道增生会变得危险
结肠癌常起源于肠道内的微小增生,但并非所有这些增生表现相同。本研究提出了一个细微却重要的问题:当两个密切相关且与癌症相关的基因发生异常时,为什么其中一个异常会强烈推动细胞走向癌变,而另一个常常停滞不前?通过在小鼠身上追踪这些基因变化数月乃至更久,研究者们揭示了为何某些早期肠道锯齿状息肉比其他息肉更有可能进展为癌症。
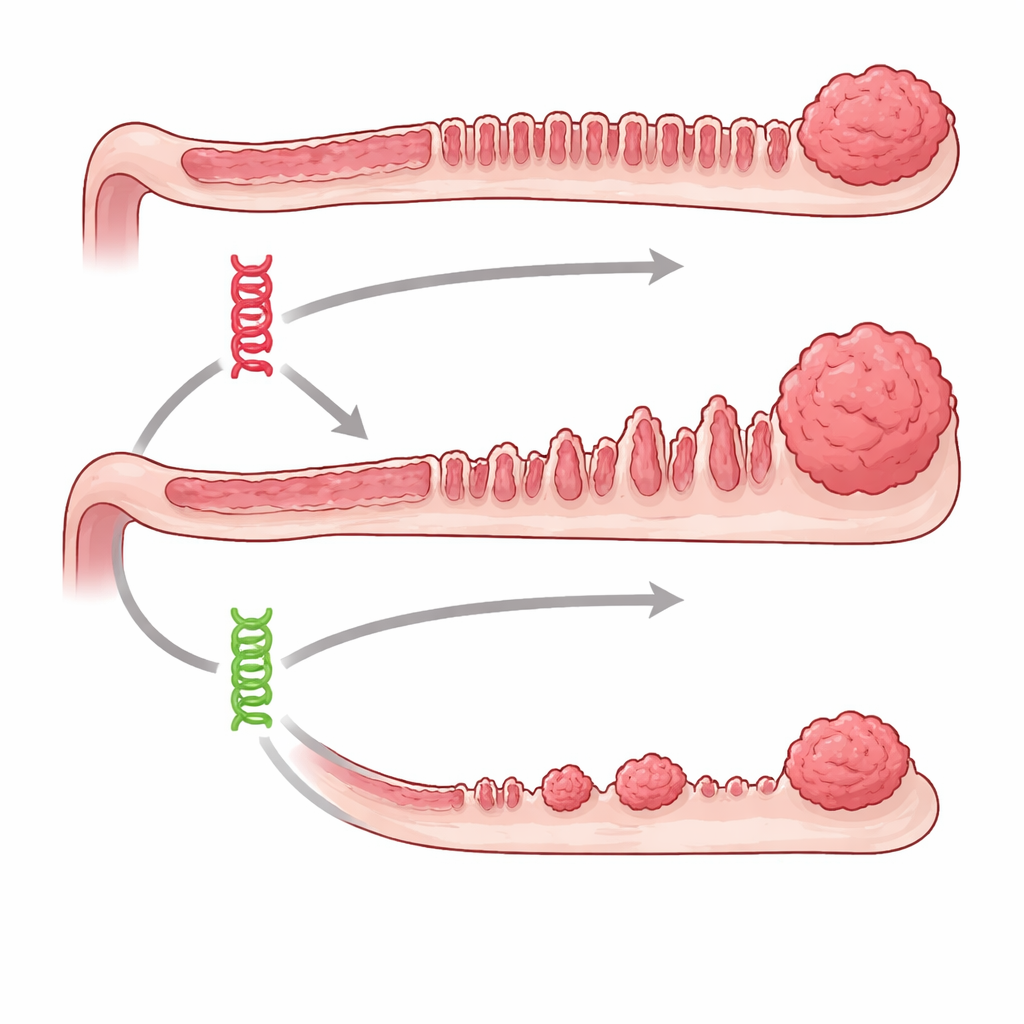
两个故障开关导致截然不同的结果
团队聚焦于两个著名的致癌驱动基因BRAF和KRAS,它们位于细胞内相同的生长控制通路中。在人类结肠肿瘤中,这两基因的错误都很常见,尤其是在源自锯齿状、呈锯齿状外观的息肉的肿瘤中。通过改造小鼠,研究者可以在特定时间点在肠道上皮中特异性启动Braf或Kras的突变,并追踪长达一年半的后果。两种突变最终都会产生锯齿型病变,但Braf驱动的小鼠产生了更多的癌前增生,而且发生得更早、更一致;而Kras驱动的小鼠则少得多。晚期锯齿状肿瘤和侵犯性癌在Braf组常见,而仅有Kras突变时则明显罕见。
生长模式与性别差异的风险
在显微镜下观察组织时,研究者发现Braf突变的肠道变得更长、增厚,伴有典型的充满粘液的扩大隐窝,这些是锯齿状疾病的特征。Kras突变的肠道结构变化不那么明显,尽管单个隐窝的分裂实际上更为活跃(以细胞分裂标志物测量)。这表明单纯的快速增生不足以形成危险病变。值得注意的是,性别也起作用:在Kras模型中,晚期锯齿状病变几乎仅出现在雄性小鼠,而Braf突变小鼠在两性中受影响情况相似。这与人类模式相呼应:某些BRAF突变的结肠癌在女性中更常见,而KRAS突变的锯齿状癌相对罕见。
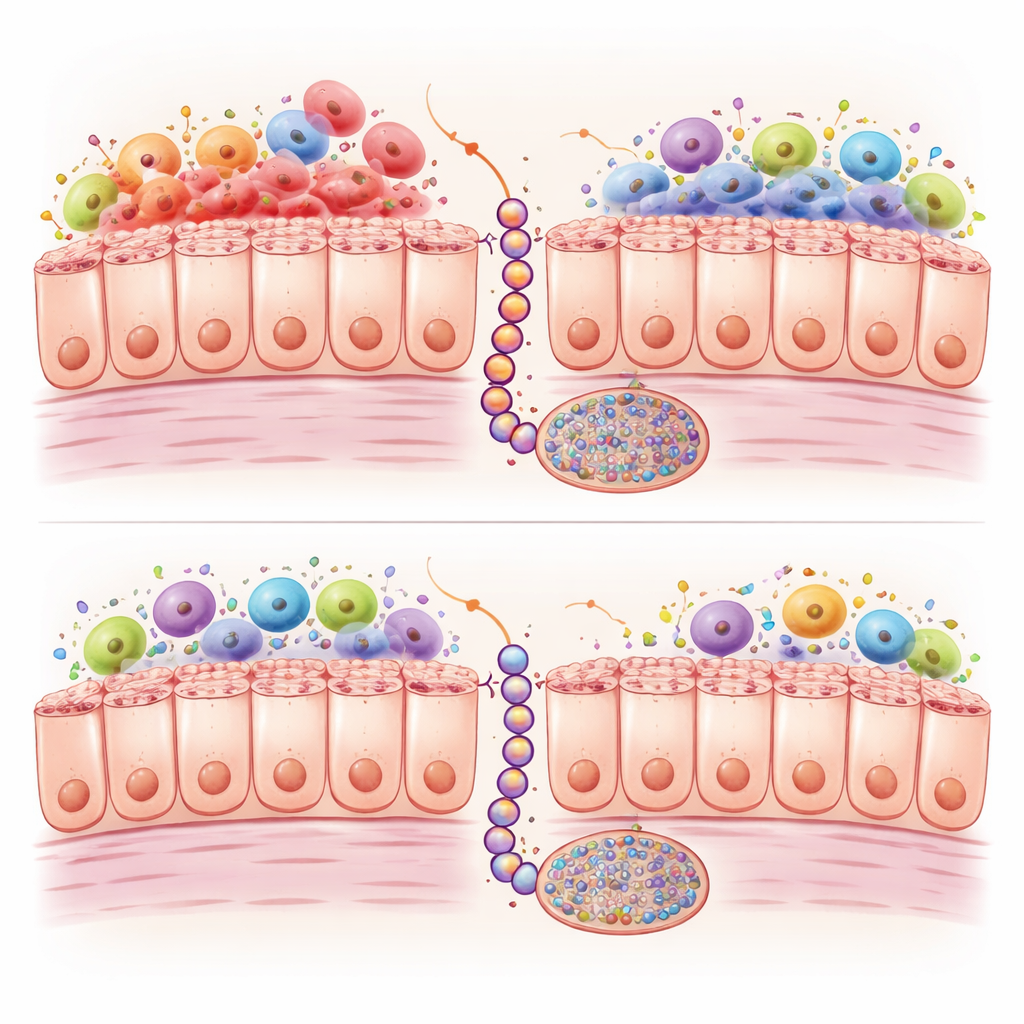
炎症与DNA上的化学标记
进一步深入分析时,科学家比较了两种模型随时间变化的基因活性和DNA上的化学标记。Braf突变的肠道显示出免疫与炎症程序的强烈激活,特别是M1型巨噬细胞显著增多,这类白细胞释放强烈的炎性信号。Kras突变的肠道则此类细胞较少,免疫激活也较弱。与此同时,两种突变都会导致大量DNA位点上甲基基团的积累;在人类肿瘤中,这种所谓的CpG岛甲基化表型(CIMP)可以关闭一些保护性基因。然而在Kras小鼠中,这种甲基化积累速度更慢、程度也较轻,涉及超过一千个位点,尤其集中在与细胞生长调控、细胞间接触以及WNT信号相关的基因上,而WNT通路对将锯齿状病变推向癌变至关重要。
一个主要通路大体保持沉默
最明显的差异之一涉及WNT通路,该通路在结肠肿瘤中常变得过度活跃。此前的研究表明,在Braf突变小鼠中,许多病变最终会获得驱动WNT过度活化的改变,表现为β-连环蛋白(β-catenin)进入细胞核。在本研究中,当团队对Kras突变的锯齿状病变进行β-连环蛋白染色时,几乎所有病变仅显示正常模式,只有一个病变呈现微弱的异常核染色。这意味着在Kras背景下,通常推动锯齿状息肉迈向癌变的关键WNT“第二击”很少发生,可能因为较弱的DNA甲基化和不同的基因表达环境使得此类改变不易稳定存在。
这对肠癌风险的意义
综合来看,结果显示尽管BRAF和KRAS位于同一信号通路,但它们使肠道上皮沿着非常不同的长期轨迹发展。Braf突变结合了强烈的炎性信号、明显的DNA甲基化以及频繁的WNT激活,为锯齿状病变向癌变进展提供了有利条件。单纯的Kras突变虽然也能产生锯齿状增生,但起病更慢、发生率更低、DNA甲基化变化更少且WNT激活罕见,因此大多数病变被限制住。对于患者而言,这项工作有助于解释为什么携带BRAF突变的锯齿状息肉被视为更高风险,而携带KRAS突变的锯齿状病变则既更少见也不易恶变,除非发生额外的损伤性事件。
引用: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
关键词: 结直肠癌, 锯齿状息肉, BRAF与KRAS, DNA甲基化, WNT信号通路