Clear Sky Science · pl
Osłabienie fenotypu metylatora wysp CpG i brak aktywacji szlaku WNT ograniczają nowotworzenie jelitowe z mutacją Kras
Dlaczego niektóre zmiany w jelicie stają się niebezpieczne
Rak okrężnicy często zaczyna się od drobnych narośli w jelicie, ale nie wszystkie te zmiany zachowują się jednakowo. W tym badaniu zadano subtelne, lecz istotne pytanie: gdy dwie genetycznie bliskie geny związane z rakiem zawodzą, dlaczego jedna zmiana silnie popycha komórki w kierunku nowotworu, podczas gdy druga najczęściej zatrzymuje się w rozwoju? Śledząc te zmiany genetyczne u myszy przez wiele miesięcy, badacze wyjaśniają, dlaczego niektóre wczesne polipy ząbkowane w jelicie znacznie częściej przechodzą w raka niż inne.
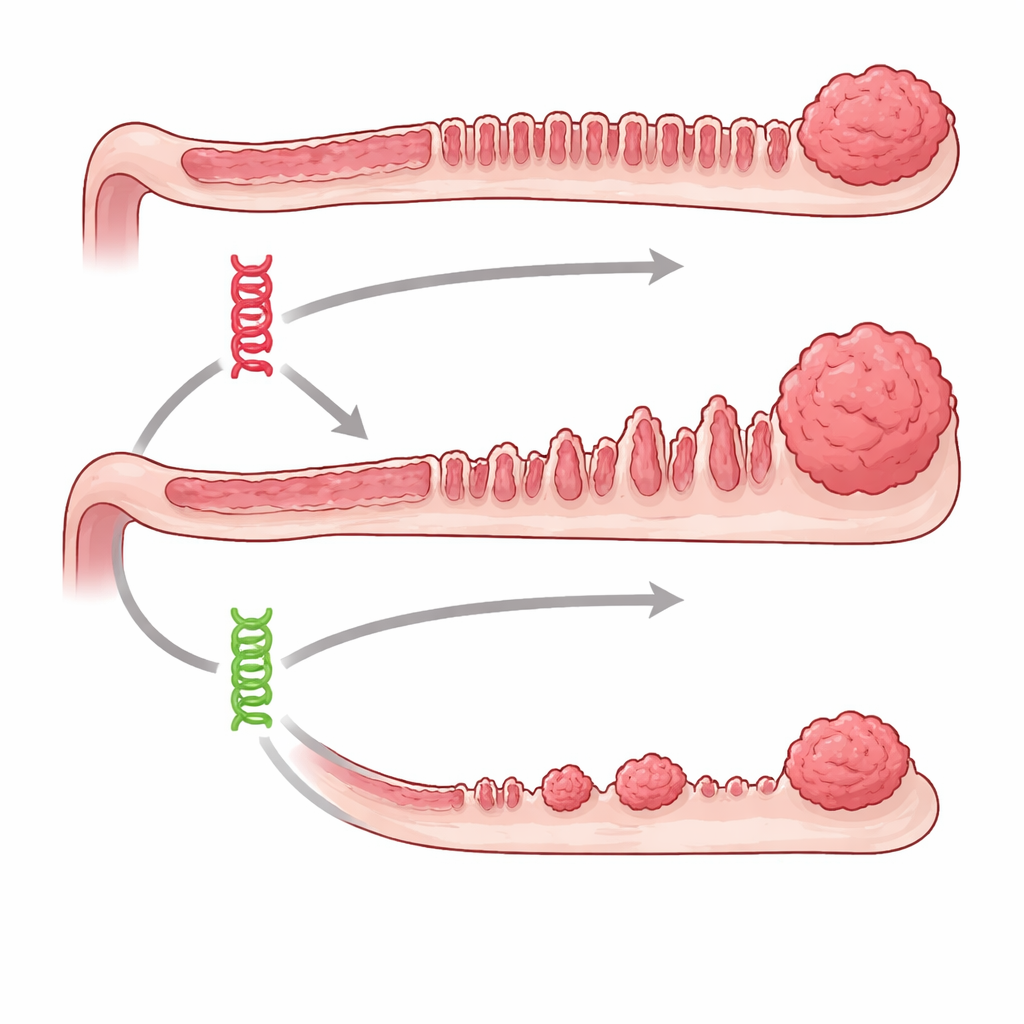
Dwa wadliwe przełączniki o bardzo różnych skutkach
Zespół skupił się na dwóch dobrze znanych czynnikach napędzających raka, BRAF i KRAS, które działają w tym samym wewnątrzkomórkowym szlaku kontroli wzrostu. U ludzi błędy w tych genach są częste w nowotworach okrężnicy, szczególnie tych wywodzących się z polipów o ząbkowanej strukturze. Dzięki myszom inżynieryjnym badacze mogli włączyć albo mutację Braf, albo Kras specyficznie w nabłonku jelita w wybranym momencie, a następnie obserwować efekty przez okres do półtora roku. Obie mutacje w końcu powodowały zmiany typu ząbkowanego, ale myszy z mutacją Braf rozwijały znacznie więcej zmian przednowotworowych, i robiły to znacznie szybciej oraz bardziej konsekwentnie niż myszy z mutacją Kras. Zaawansowane guzy ząbkowane i nowotwory inwazyjne były częste w grupie Braf, podczas gdy znacznie rzadziej występowały przy samej mutacji Kras.
Wzorce wzrostu i różnice związane z płcią
W mikroskopowym obrazie tkanek badacze zaobserwowali, że jelita z mutacją Braf stawały się dłuższe i pogrubione, z powiększonymi, wypełnionymi śluzem kryptami typowymi dla choroby ząbkowanej. Jelita z mutacją Kras wykazywały mniej dramatyczne zmiany strukturalne, choć pojedyncze krypty faktycznie dzieliły się szybciej, mierzone markerem podziału komórek. Sugeruje to, że sam szybki wzrost nie wystarcza, by powstały groźne zmiany. Co uderzające, istotna była też płeć: w modelu Kras zaawansowane zmiany ząbkowane pojawiały się niemal wyłącznie u myszy płci męskiej, podczas gdy myszy z mutacją Braf obu płci były podobnie dotknięte. Odbija to wzorce obserwowane u ludzi, gdzie niektóre nowotwory okrężnicy z mutacją BRAF występują częściej u kobiet, a nowotwory z mutacją KRAS są względnie rzadkie.
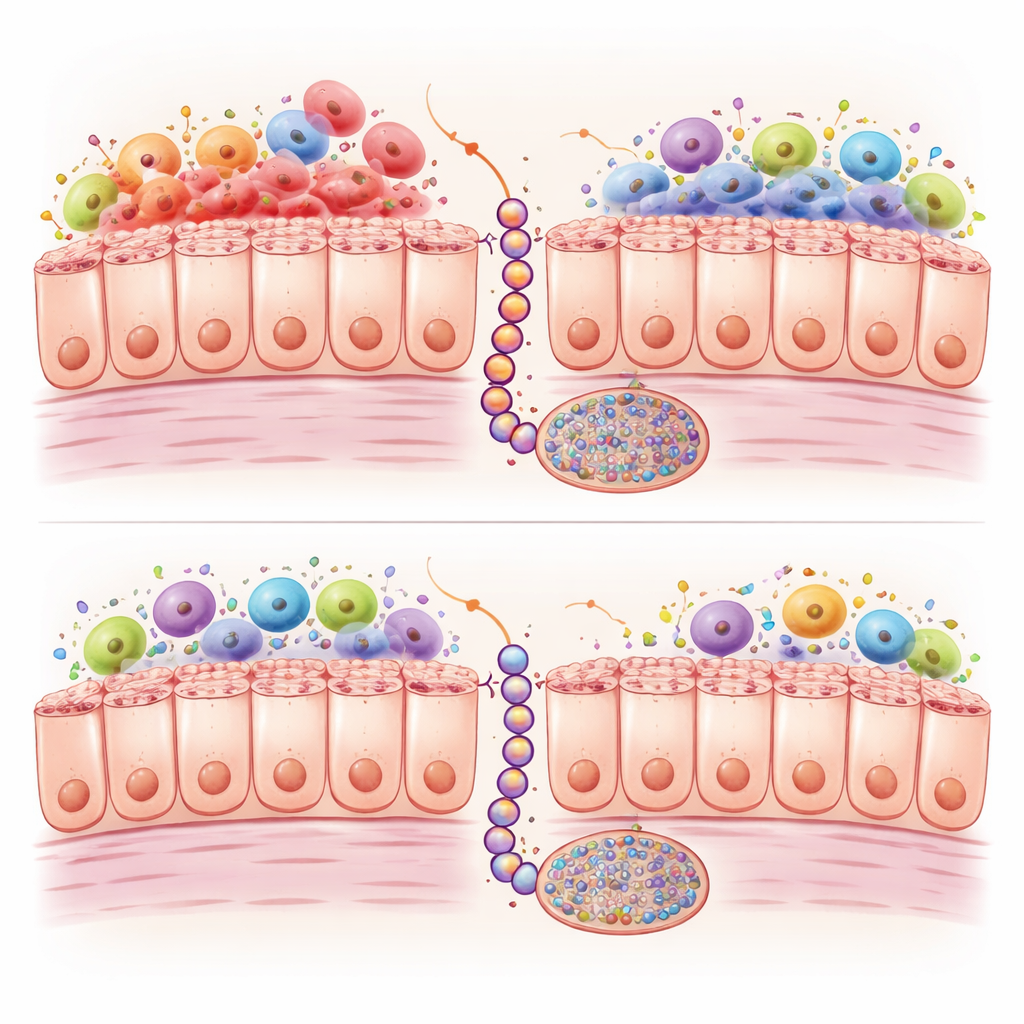
Zapalenie i chemiczne znaczniki na DNA
Pogłębiając analizę, naukowcy porównali aktywność genów i chemiczne oznaczenia DNA w obu modelach w czasie. Jelita z mutacją Braf wykazywały silną aktywację programów odpornościowych i zapalnych, ze szczególnie dużą obecnością makrofagów typu M1 — odmiany białych krwinek wydzielających silne sygnały zapalne. Jelita z mutacją Kras miały mniej tych komórek i słabszą aktywację układu odpornościowego. Jednocześnie obie mutacje powodowały dodatkowe chemiczne znaczniki, zwane grupami metylowymi, gromadzące się w wielu miejscach na DNA; u ludzi tzw. fenotyp metylatora wysp CpG (CIMP) może wyłączać geny ochronne. Jednak u myszy Kras ta metylacja narastała wolniej i w mniejszym stopniu w ponad tysiącu miejsc, szczególnie w genach związanych z kontrolą wzrostu, kontaktem międzykomórkowym i sygnalizacją WNT — szlakiem kluczowym do popychania zmian ząbkowanych w kierunku pełnowymiarowego raka.
Kluczowy szlak, który pozostaje przeważnie cichy
Jedna z najbardziej wyraźnych różnic dotyczyła szlaku WNT, który często ulega nadmiernej aktywacji w guzach okrężnicy. W modelach z mutacją Braf wcześniejsze prace wykazały, że wiele zmian ostatecznie nabywa alteracje, które napędzają nadaktywność WNT, widoczną jako przemieszczanie się białka β-kateniny do jąder komórkowych. W obecnym badaniu, gdy zespół barwił zmiany ząbkowane z mutacją Kras pod kątem β-kateniny, niemal wszystkie wykazywały tylko normalny wzorzec, a tylko jedna zmiana wykazała słabe nieprawidłowe barwienie jądrowe. Oznacza to, że w kontekście Kras kluczowy „drugi cios” w postaci aktywacji WNT, który zwykle popycha polipy ząbkowane do raka, rzadko się pojawia — najpewniej dlatego, że słabsza metylacja DNA i inny profil ekspresji genów czynią takie zmiany mniej prawdopodobnymi do utrwalenia.
Co to oznacza dla ryzyka raka jelita
Podsumowując, wyniki pokazują, że choć BRAF i KRAS znajdują się w tym samym szlaku sygnalizacyjnym, wyznaczają bardzo różne długoterminowe drogi dla nabłonka jelita. Mutacja Braf łączy silne sygnały zapalne, intensywną metylację DNA i częstą aktywację WNT, tworząc żyzne warunki dla przechodzenia zmian ząbkowanych w raka. Sama mutacja Kras może powodować zmiany ząbkowane, ale z wolniejszym początkiem, mniejszą częstością, mniejszą liczbą zmian metylacji DNA i niewielką aktywacją WNT, więc większość zmian pozostaje ograniczona. Dla pacjentów praca ta pomaga wyjaśnić, dlaczego polipy ząbkowane z mutacją BRAF uważa się za wyższe ryzyko, podczas gdy zmiany z mutacją KRAS są rzadsze i mniej skłonne do zezłośliwienia, chyba że wystąpią dodatkowe, uszkadzające zdarzenia.
Cytowanie: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
Słowa kluczowe: rak jelita grubego, polipy ząbkowane, BRAF i KRAS, metylacja DNA, szlak WNT