Clear Sky Science · es
Atenuación del fenotipo de metilador de islas CpG y ausencia de activación de la señalización WNT limitan la neoplasia intestinal con mutación en Kras
Por qué algunas proliferaciones intestinales se vuelven peligrosas
El cáncer de colon suele comenzar a partir de pequeños crecimientos en el intestino, pero no todos estos crecimientos se comportan de la misma manera. Este estudio plantea una pregunta sutil pero importante: cuando dos genes estrechamente relacionados con el cáncer fallan, ¿por qué una de esas alteraciones empuja a las células con fuerza hacia el cáncer mientras que la otra a menudo se estanca? Al seguir estos cambios genéticos en ratones durante muchos meses, los investigadores revelan por qué algunos pólipos serrados tempranos en el intestino tienen mucha más probabilidad de progresar a cáncer que otros.
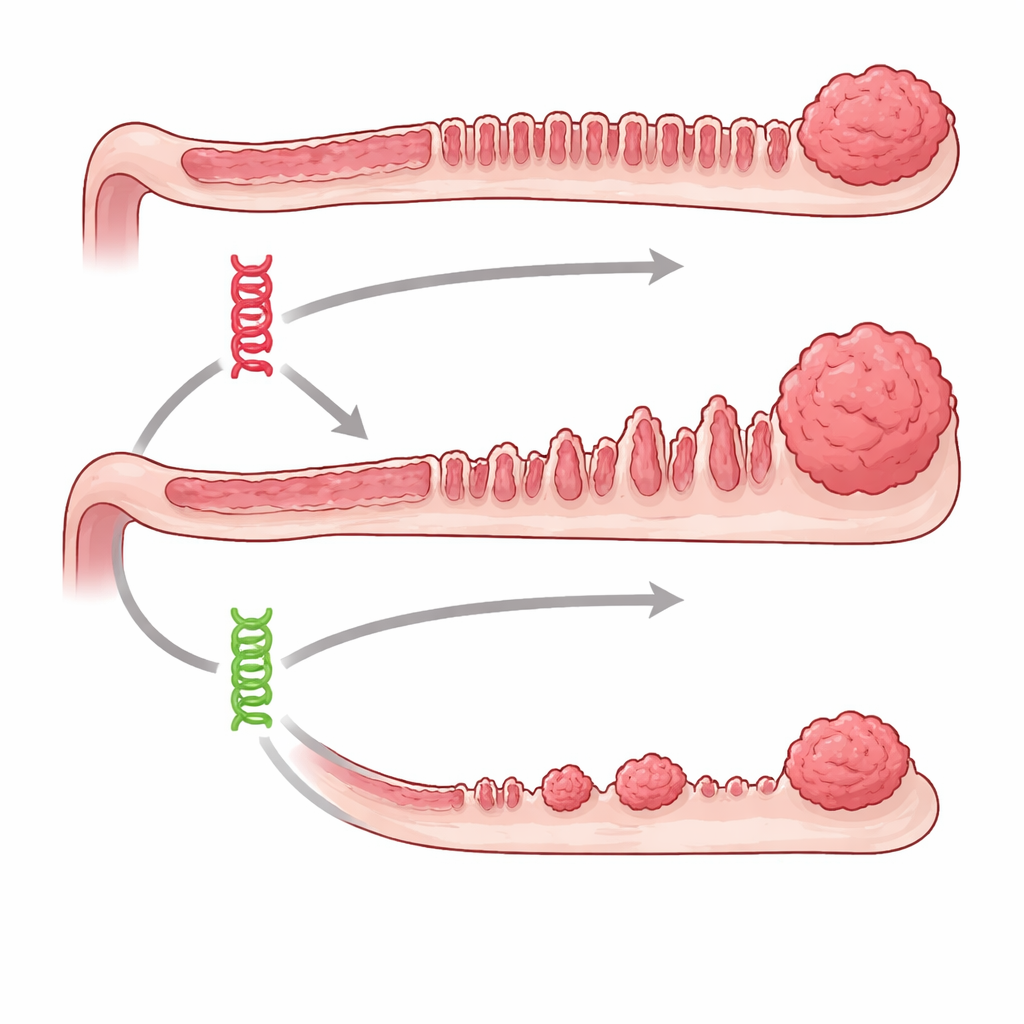
Dos interruptores defectuosos con resultados muy distintos
El equipo se centró en dos impulsores del cáncer bien conocidos, BRAF y KRAS, que actúan en la misma vía de control del crecimiento dentro de las células. En humanos, los errores en estos genes son comunes en tumores de colon, especialmente los que surgen de pólipos serrados con aspecto dentado. Usando ratones modificados, los investigadores pudieron activar bien la mutación en Braf o en Kras específicamente en el revestimiento intestinal en un momento elegido, y luego seguir lo que ocurría durante hasta un año y medio. Ambas mutaciones acabaron por producir lesiones de tipo serrado, pero los ratones con Braf activado desarrollaron muchos más crecimientos precancerosos, y lo hicieron mucho antes y de forma más consistente que los de Kras. Los tumores serrados avanzados y los cánceres invasivos fueron comunes en el grupo Braf pero claramente raros cuando solo Kras estaba mutado.
Patrones de crecimiento y diferencias por sexo en el riesgo
Al observar el tejido al microscopio, los investigadores vieron que los intestinos con mutación en Braf se volvían más largos y engrosados, con criptas agrandadas llenas de moco, típicas de la enfermedad serrada. Los intestinos con mutación en Kras mostraron cambios estructurales menos dramáticos, aunque las criptas individuales en realidad se dividían más rápidamente, según un marcador de división celular. Esto sugiere que el simple crecimiento acelerado no basta para formar lesiones peligrosas. De forma llamativa, el sexo también importó: en el modelo Kras, las lesiones serradas avanzadas surgieron casi exclusivamente en ratones machos, mientras que los ratones con mutación en Braf de ambos sexos se vieron afectados de manera similar. Esto refleja patrones humanos, donde ciertos cánceres colorrectales con mutación en BRAF son más frecuentes en mujeres y los cánceres serrados con mutación en KRAS son relativamente raros.
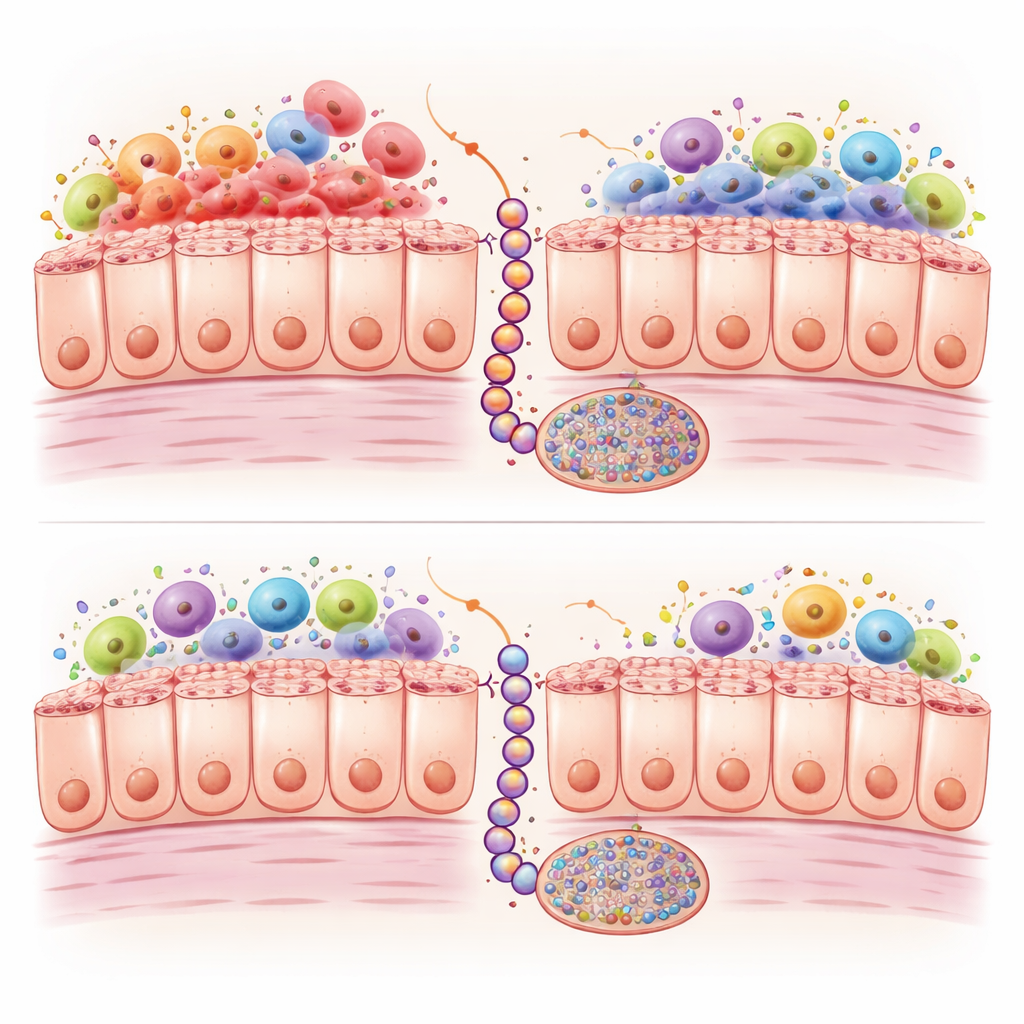
Inflamación y marcas químicas en el ADN
Indagando más, los científicos compararon la actividad génica y las marcas químicas en el ADN en los dos modelos a lo largo del tiempo. Los intestinos con mutación en Braf mostraron una fuerte activación de programas inmunitarios e inflamatorios, con una presencia especialmente alta de macrófagos de tipo M1, un tipo de glóbulo blanco que libera señales inflamatorias intensas. Los intestinos con mutación en Kras presentaron menos de estas células y una activación inmune más débil. Al mismo tiempo, ambas mutaciones provocaron la acumulación de etiquetas químicas adicionales, llamadas grupos metilo, en muchos sitios del ADN; en los cánceres humanos, este denominado fenotipo de metilador de islas CpG (CIMP) puede silenciar genes protectores. Sin embargo, en los ratones Kras esta metilación se acumuló más lentamente y en menor grado en más de mil sitios, particularmente en genes relacionados con el control del crecimiento celular, las uniones entre células y la señalización WNT, una vía crucial para empujar las lesiones serradas hacia el cáncer completo.
Una vía clave que permanece mayormente silenciosa
Una de las diferencias más claras implicó la vía WNT, que con frecuencia se hiperactiva en tumores de colon. En ratones con mutación en Braf, trabajos previos habían mostrado que muchas lesiones acaban adquiriendo cambios que impulsan la WNT a un estado sobreactivado, visible como la proteína β‑catenina moviéndose al núcleo celular. En el estudio actual, cuando el equipo tiñó las lesiones serradas con mutación en Kras para β‑catenina, casi todas mostraron solo el patrón normal, con apenas una única lesión presentando una tinción nuclear anormal y débil. Esto significa que, en el contexto de Kras, el crucial “segundo golpe” en WNT que habitualmente propulsa a los pólipos serrados hacia el cáncer rara vez se consigue, probablemente porque la metilación del ADN más débil y el distinto entorno de expresión génica hacen que esos cambios tengan menos probabilidad de afianzarse.
Qué significa esto para el riesgo de cáncer intestinal
En conjunto, los hallazgos muestran que aunque BRAF y KRAS ocupan la misma vía de señalización, trazan caminos a largo plazo muy distintos en el revestimiento intestinal. La mutación en Braf combina fuertes señales inflamatorias, metilación intensa del ADN y activación frecuente de WNT, creando un terreno fértil para que las lesiones serradas progresen a cáncer. La mutación en Kras por sí sola puede generar crecimientos serrados, pero con aparición más lenta, menor frecuencia, menos cambios en la metilación del ADN y poca activación de WNT, por lo que la mayoría de las lesiones permanecen contenidas. Para los pacientes, este trabajo ayuda a explicar por qué los pólipos serrados con mutación en BRAF se consideran de mayor riesgo, mientras que las lesiones serradas con mutación en KRAS son tanto más raras como menos propensas a volverse malignas a menos que ocurran eventos dañinos adicionales.
Cita: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
Palabras clave: cáncer colorrectal, pólipos serrados, BRAF y KRAS, metilación del ADN, señalización WNT