Clear Sky Science · nl
Vermindering van het CpG-eiland-methyleringsfenotype en gebrek aan WNT-signaalactivatie beperken Kras-mutante intestinale neoplasie
Waarom sommige darmwoekeringen gevaarlijk worden
Dikke darmkanker begint vaak uit kleine gezwellen in het maag‑darmkanaal, maar niet al deze gezwellen gedragen zich hetzelfde. Deze studie onderzoekt een subtiele maar belangrijke vraag: wanneer twee nauw verwante genen die met kanker geassocieerd zijn defect raken, waarom duwt de een cellen sterk richting kanker terwijl de ander vaak stagneert? Door deze genetische veranderingen bij muizen gedurende vele maanden te volgen, leggen de onderzoekers bloot waarom sommige vroege serrated poliepen in de darm veel meer kans hebben om tot kanker te ontwikkelen dan andere.
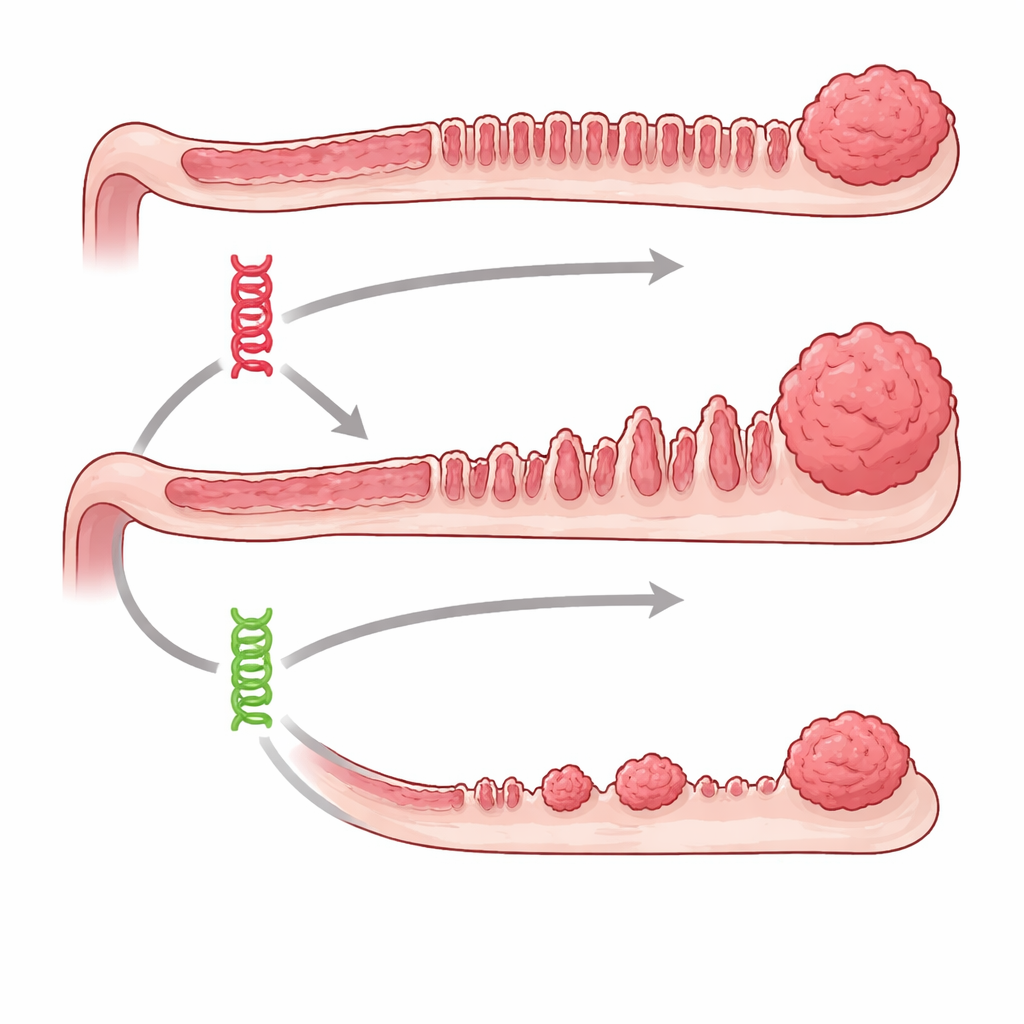
Twee kapotte schakelaars met heel verschillende uitkomsten
Het team richtte zich op twee goed bekende kankerdrijvers, BRAF en KRAS, die in dezelfde groeiregulerende signaalweg binnen cellen zitten. Bij mensen komen fouten in deze genen veel voor in colon tumoren, vooral die ontstaan uit serrated, zaagtandachtige poliepen. Met genetisch gemodificeerde muizen konden de onderzoekers op een gekozen tijdpunt ofwel de Braf‑ ofwel de Kras‑mutatie specifiek in het darmepitheel inschakelen en vervolgens tot anderhalf jaar volgen wat er gebeurde. Beide mutaties leverden uiteindelijk serrated‑achtige laesies op, maar bij Braf‑gedreven muizen ontwikkelden zich veel meer voorstadia van kanker, en dat veel eerder en consistenter dan bij Kras‑gedreven muizen. Geavanceerde serrated tumoren en invasieve kankers kwamen vaak voor in de Braf‑groep maar waren opvallend zeldzaam wanneer alleen Kras gemuteerd was.
Groeipatronen en sekseverschillen in risico
Onder de microscoop zagen de onderzoekers dat Braf‑gemuteerde darmen langer werden en meer verdikt raakten, met vergrote, met slijm gevulde crypten typisch voor serrated aandoening. Kras‑gemuteerde darmen toonden minder dramatische structurele veranderingen, hoewel individuele crypten daadwerkelijk sneller deelden, gemeten met een marker voor celdeling. Dit suggereert dat louter snel delen niet voldoende is om gevaarlijke laesies te vormen. Opvallend was dat geslacht ook een rol speelde: in het Kras‑model ontstonden geavanceerde serrated laesies vrijwel uitsluitend bij mannelijke muizen, terwijl Braf‑gemuteerde muizen van beide geslachten ongeveer evenveel waren getroffen. Dit weerspiegelt patronen bij mensen, waar bepaalde BRAF‑gemuteerde dikkedarmkankers vaker bij vrouwen voorkomen en KRAS‑gemuteerde serrated kankers relatief zeldzaam zijn.
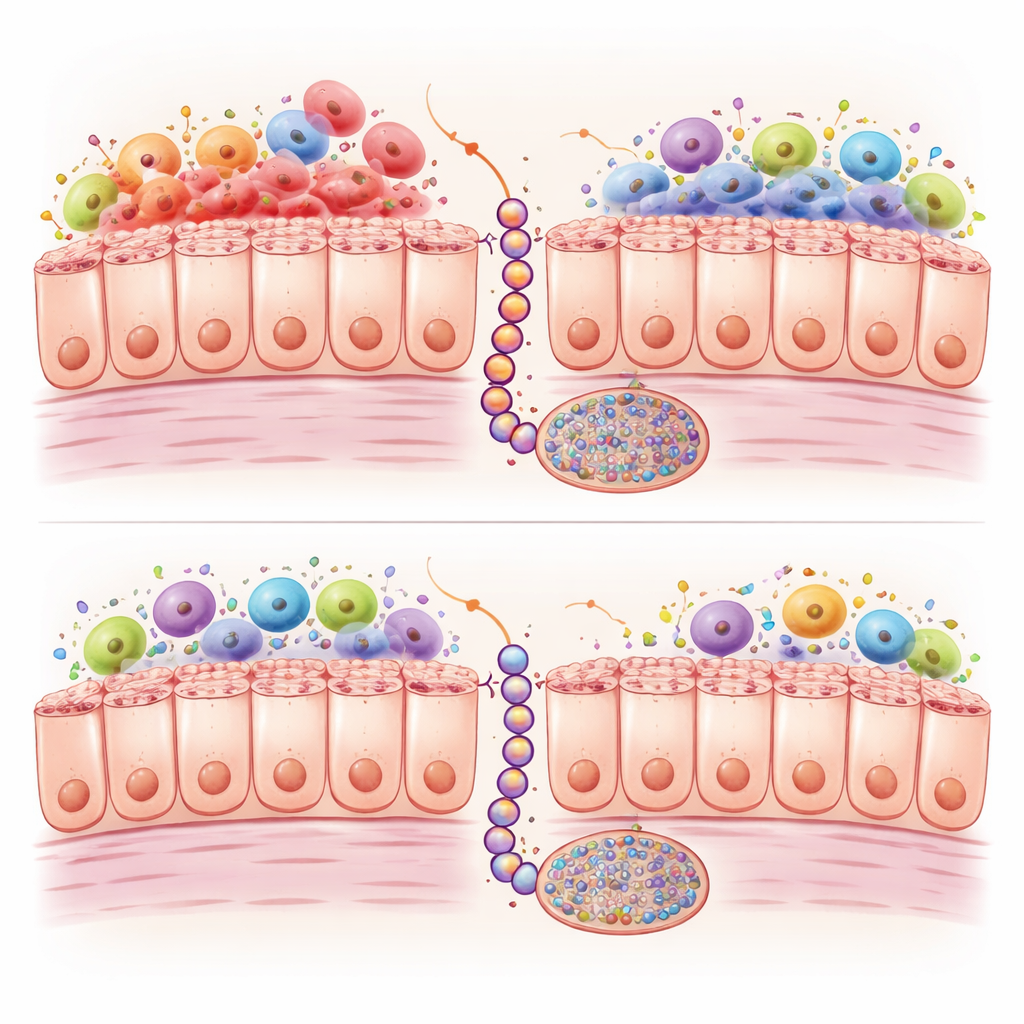
Ontsteking en chemische labels op DNA
Dieper gravend vergeleken de wetenschappers genactiviteit en chemische markers op DNA in de twee modellen in de tijd. Braf‑gemuteerde darmen toonden sterke activatie van immuun‑ en ontstekingsprogramma’s, met een bijzonder hoge aanwezigheid van M1‑type macrofagen, een type witte bloedcel dat krachtige ontstekingssignalen afgeeft. Kras‑gemuteerde darmen hadden minder van deze cellen en zwakkere immuunactivatie. Tegelijkertijd veroorzaakten beide mutaties extra chemische labels, methylgroepen genoemd, die zich op veel DNA‑plaatsen ophopen; bij menselijke kankers kan dit zogenaamde CpG-eiland‑methyleringsfenotype (CIMP) beschermende genen uitschakelen. Echter, bij de Kras‑muizen bouwde deze methylering zich langzamer en in mindere mate op op meer dan duizend locaties, met name in genen die betrokken zijn bij celgroeiregulatie, cel‑tot‑cel contact en WNT‑signalering — een pad dat cruciaal is om serrated laesies naar volledige kanker te duwen.
Een sleutelpad dat grotendeels stil blijft
Een van de duidelijkste verschillen betrof het WNT‑pad, dat vaak overactief wordt in colon tumoren. Bij de Braf‑gemuteerde muizen had eerder onderzoek laten zien dat veel laesies uiteindelijk veranderingen verwerven die WNT overactiveren, zichtbaar als het eiwit β‑catenine dat naar de celkernen verhuist. In de huidige studie, toen het team Kras‑gemuteerde serrated laesies kleurde voor β‑catenine, vertoonden bijna alle laesies alleen het normale patroon, en slechts één laesie liet een zwakke abnormale nucleaire kleuring zien. Dit betekent dat in het Kras‑scenario de cruciale WNT‑‘tweede klap’ die serrated poliepen meestal naar kanker duwt zelden wordt bereikt, waarschijnlijk omdat de zwakkere DNA‑methylering en de verschillende genexpressieomgeving zulke veranderingen minder waarschijnlijk maakt om zich te vestigen.
Wat dit betekent voor het risico op darmkanker
Gezamenlijk laten de bevindingen zien dat hoewel BRAF en KRAS in hetzelfde signaalpad zitten, ze het darmepitheel op zeer verschillende lange termijn paden zetten. Een Braf‑mutatie koppelt sterke ontstekingssignalen, intensieve DNA‑methylering en frequente WNT‑activatie, wat een vruchtbare voedingsbodem creëert voor serrated laesies om tot kanker te vorderen. Een Kras‑mutatie alleen kan serrated groeiën veroorzaken, maar met langzamere aanvang, lagere frequentie, minder DNA‑methyleringsveranderingen en weinig WNT‑activatie, zodat de meeste laesies beperkt blijven. Voor patiënten helpt dit werk verklaren waarom BRAF‑gemuteerde serrated poliepen als hoger risico worden beschouwd, terwijl KRAS‑gemuteerde serrated laesies zeldzamer zijn en minder snel kwaadaardig worden tenzij aanvullende schadelijke gebeurtenissen optreden.
Bronvermelding: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
Trefwoorden: dikkedarmkanker, gezaagde poliepen, BRAF en KRAS, DNA-methylering, WNT-signaalverlening