Clear Sky Science · it
Attenuazione del fenotipo CpG island methylator e assenza di attivazione della segnalazione WNT limitano la neoplasia intestinale mutata in Kras
Perché alcune escrescenze intestinali diventano pericolose
Il cancro del colon spesso inizia da piccole escrescenze nell’intestino, ma non tutte queste formazioni si comportano allo stesso modo. Questo studio pone una domanda sottile ma cruciale: quando due geni collegati al cancro, strettamente imparentati, vanno incontro a errori, perché una mutazione spinge fortemente le cellule verso il cancro mentre l’altra frequentemente si arresta? Seguendo questi cambi genetici nei topi per molti mesi, i ricercatori spiegano perché alcuni poli serrati precoci nell’intestino hanno una probabilità molto maggiore di progredire verso il cancro rispetto ad altri.
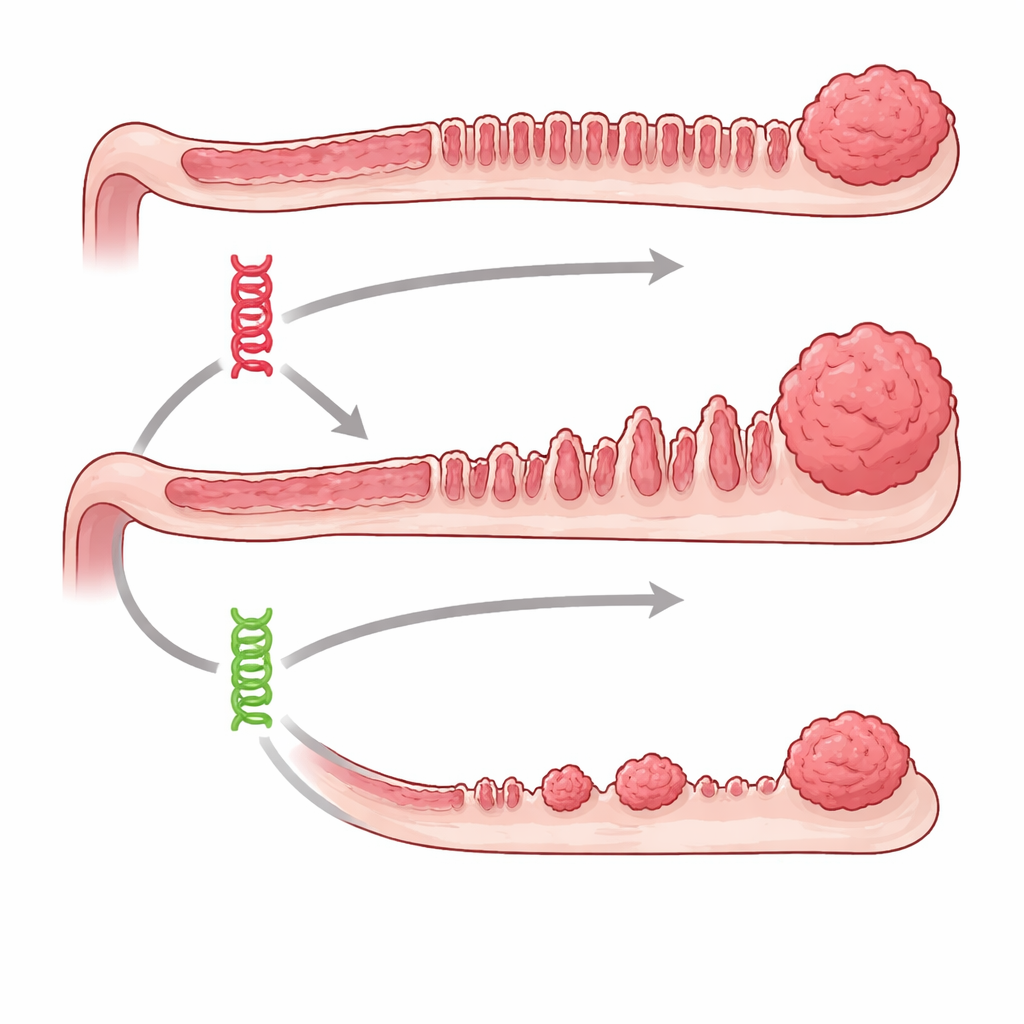
Due interruttori difettosi con esiti molto diversi
Il gruppo si è concentrato su due noti oncogeni, BRAF e KRAS, che operano nello stesso percorso di controllo della crescita all’interno delle cellule. Nell’uomo, errori in questi geni sono comuni nei tumori del colon, in particolare in quelli che originano da polipi serrati dall’aspetto seghettato. Utilizzando topi geneticamente modificati, i ricercatori hanno potuto attivare la mutazione in Braf o in Kras specificamente nell’epitelio intestinale in un momento scelto, quindi monitorare cosa accadeva per fino a un anno e mezzo. Entrambe le mutazioni produssero infine lesioni di tipo serrato, ma i topi con Braf mutato svilupparono molti più crecimientos precancerosi, e lo fecero molto prima e con maggiore consistenza rispetto ai topi con mutazione in Kras. Tumori serrati avanzati e carcinomi infiltranti erano comuni nel gruppo Braf ma visibilmente rari quando era mutato solo Kras.
Modelli di crescita e differenze legate al sesso
All’esame istologico, i ricercatori osservarono che gli intestini con Braf mutato diventavano più lunghi e ispessiti, con cripte ingrandite piene di muco tipiche della malattia serrata. Gli intestini con Kras mutato mostravano cambiamenti strutturali meno drammatici, anche se singole cripte si dividevano effettivamente più rapidamente, come misurato con un marcatore della divisione cellulare. Questo suggerisce che una semplice crescita accelerata non è sufficiente per generare lesioni pericolose. In modo sorprendente, anche il sesso influiva sul rischio: nel modello Kras, le lesioni serrate avanzate insorgevano quasi esclusivamente nei topi maschi, mentre i topi con Braf mutato di entrambi i sessi erano colpiti in modo simile. Questo riflette i modelli umani, dove alcuni tumori del colon con mutazione in BRAF sono più frequenti nelle donne e i tumori serrati con mutazione in KRAS sono relativamente rari.
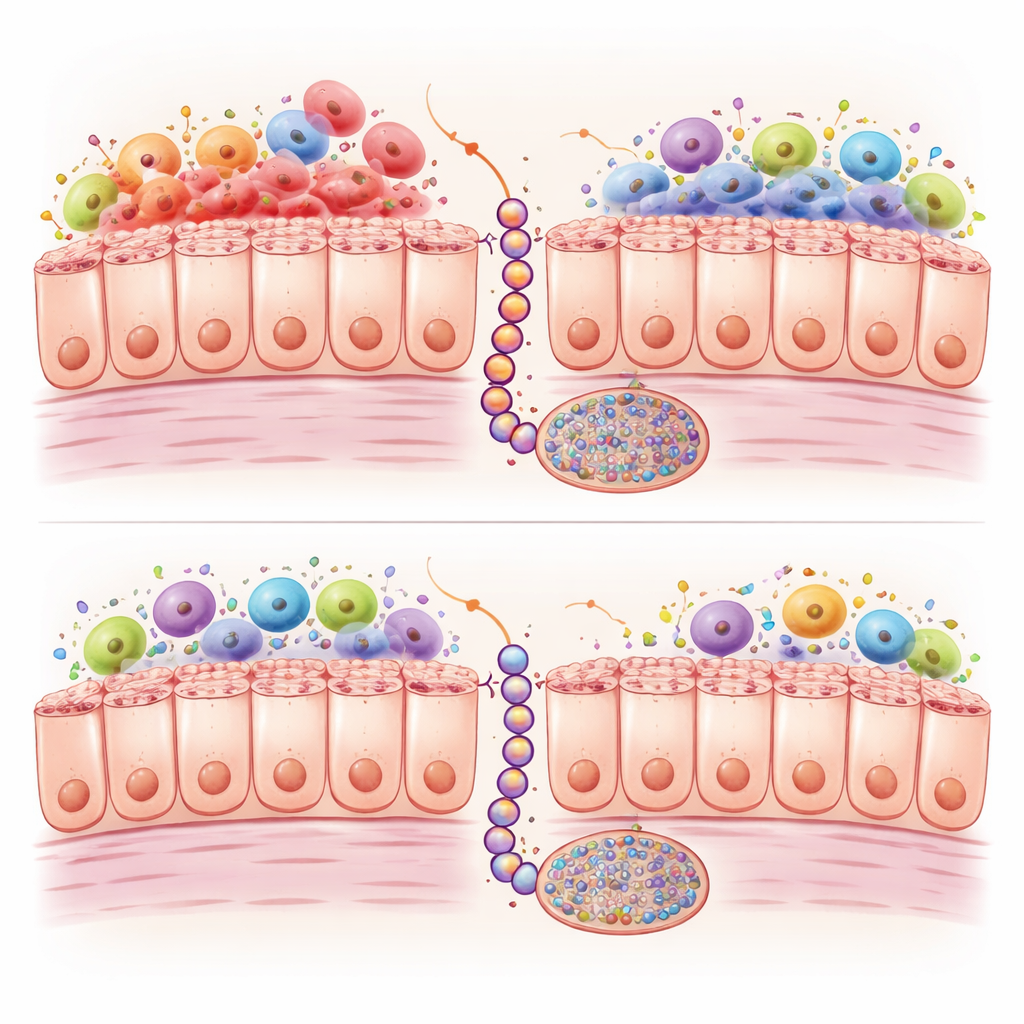
Infiammazione e tag chimici sul DNA
Approfondendo, gli scienziati confrontarono l’attività genica e le modifiche chimiche sul DNA nei due modelli nel tempo. Gli intestini con Braf mutato mostrarono una forte attivazione di programmi immunitari e infiammatori, con una presenza particolarmente elevata di macrofagi di tipo M1, una classe di globuli bianchi che rilascia segnali infiammatori intensi. Gli intestini con Kras mutato avevano meno di queste cellule e una più debole attivazione immunitaria. Allo stesso tempo, entrambe le mutazioni causarono un accumulo di gruppi metilici in molti siti del DNA; nei tumori umani questo cosiddetto fenotipo CpG island methylator, o CIMP, può silenziare geni protettivi. Tuttavia, nei topi Kras questa metilazione si sviluppò più lentamente e in misura minore in oltre mille siti, in particolare in geni legati al controllo della crescita cellulare, ai contatti cellula‑cellula e alla segnalazione WNT, un percorso cruciale per spingere le lesioni serrate verso il cancro pienamente sviluppato.
Un percorso chiave che resta per lo più silente
Una delle differenze più nette riguardava la via WNT, che spesso diventa iperattivata nei tumori del colon. Nei topi con Braf mutato, lavori precedenti avevano mostrato che molte lesioni acquisiscono alla fine cambiamenti che spingono WNT in sovraattivazione, visibili come il trasferimento della proteina β‑catenina nei nuclei cellulari. Nel presente studio, quando il gruppo colorò le lesioni serrate con mutazione in Kras per la β‑catenina, quasi tutte mostrarono solo il pattern normale, con una sola lesione che presentava una debole colorazione nucleare anomala. Ciò significa che, nello scenario Kras, il «secondo colpo» su WNT cruciale per propellere i polipi serrati verso il cancro si verifica raramente, probabilmente perché la metilazione del DNA più debole e l’ambiente di espressione genica differente rendono meno probabili tali alterazioni.
Cosa significa per il rischio di cancro intestinale
Nel complesso, i risultati mostrano che, pur essendo BRAF e KRAS parte dello stesso percorso di segnalazione, indirizzano l’epitelio intestinale su percorsi a lungo termine molto diversi. La mutazione in Braf combina forti segnali infiammatori, massiccia metilazione del DNA e frequente attivazione di WNT, creando un terreno fertile perché le lesioni serrate progrediscano verso il cancro. La sola mutazione in Kras può produrre escrescenze serrate, ma con insorgenza più lenta, minore frequenza, meno cambiamenti nella metilazione del DNA e scarsa attivazione di WNT, quindi la maggior parte delle lesioni rimane contenuta. Per i pazienti, questo lavoro aiuta a spiegare perché i polipi serrati con mutazione in BRAF sono considerati a rischio più elevato, mentre le lesioni serrate con mutazione in KRAS sono sia più rare sia meno inclini a diventare maligne a meno che non si verifichino eventi dannosi aggiuntivi.
Citazione: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
Parole chiave: cancro del colon-retto, polipi sorrisati, BRAF e KRAS, metilazione del DNA, segnalazione WNT