Clear Sky Science · fr
Atténuation du phénotype CpG island methylator et absence d’activation de la voie WNT limitent la néoplasie intestinale porteuse d’une mutation Kras
Pourquoi certaines excroissances intestinales deviennent dangereuses
Le cancer du côlon commence souvent à partir de petites excroissances dans l’intestin, mais toutes ne se comportent pas de la même façon. Cette étude pose une question subtile mais importante : lorsque deux gènes liés au cancer, très proches fonctionnellement, dysfonctionnent, pourquoi l’une de ces altérations pousse fortement les cellules vers le cancer alors que l’autre bute le plus souvent ? En suivant ces mutations chez la souris pendant de nombreux mois, les auteurs expliquent pourquoi certains polypes sésarrés précoces de l’intestin ont beaucoup plus de chances d’évoluer vers un cancer que d’autres.
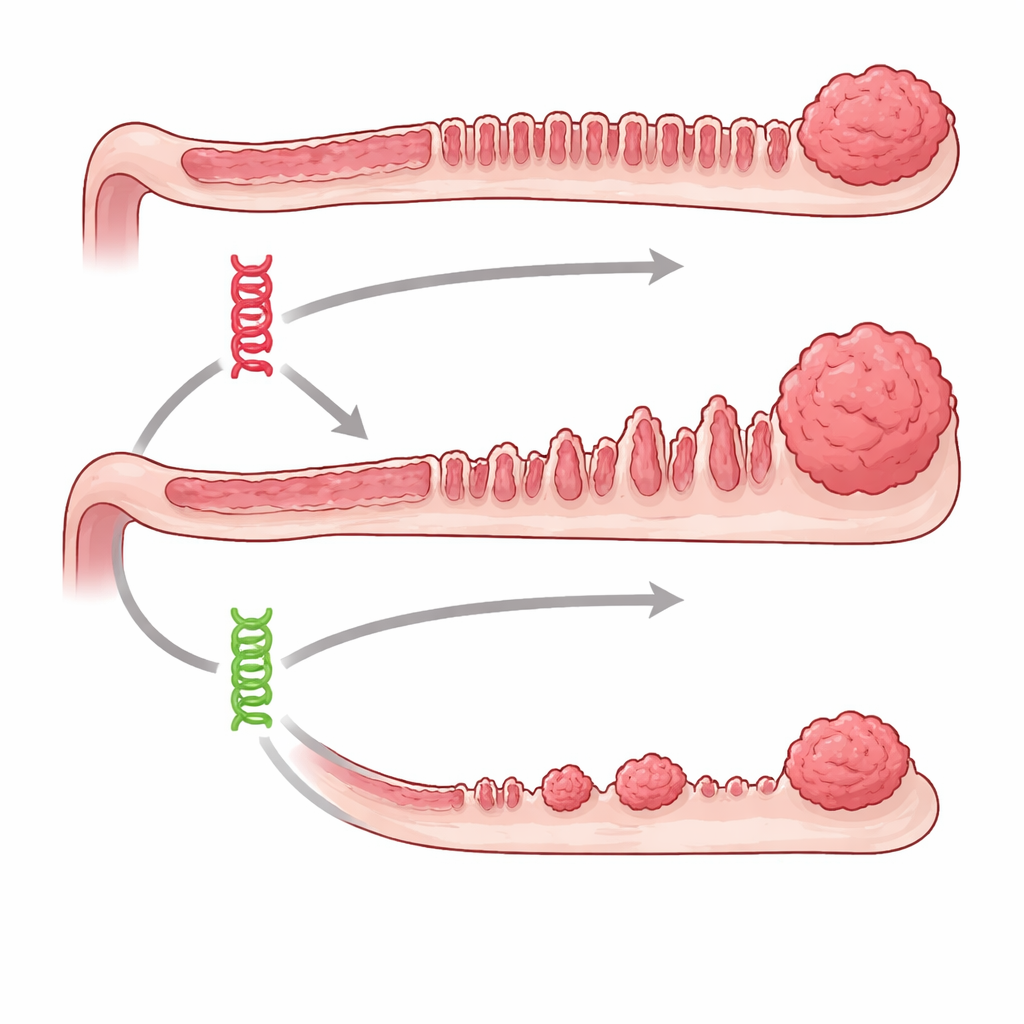
Deux interrupteurs défaillants aux conséquences très différentes
L’équipe s’est concentrée sur deux oncogènes bien connus, BRAF et KRAS, qui agissent dans la même voie de contrôle de la croissance cellulaire. Chez l’humain, des altérations de ces gènes sont fréquentes dans les tumeurs colorectales, en particulier celles issues de polypes au relief dentelé. En utilisant des souris génétiquement modifiées, les chercheurs ont pu activer soit la mutation Braf soit la mutation Kras spécifiquement dans l’épithélium intestinal à un moment choisi, puis suivre l’évolution jusqu’à un an et demi. Les deux mutations ont fini par produire des lésions de type sésarré, mais les souris porteuses de Braf ont développé beaucoup plus de croissances précancéreuses, et ce plus tôt et de façon plus régulière que les souris porteuses de Kras. Les tumeurs sésarrées avancées et les cancers invasifs étaient fréquents dans le groupe Braf mais nettement rares lorsque seule la mutation Kras était présente.
Modes de croissance et différences liées au sexe
À l’examen histologique, les intestins mutants pour Braf s’allongeaient et s’épaississaient, avec des cryptes agrandies et remplies de mucus, caractéristiques de la maladie sésarrée. Les intestins mutants pour Kras montraient des modifications structurelles moins marquées, même si les cryptes individuelles se divisaient en réalité plus rapidement, mesurées par un marqueur de prolifération. Cela suggère que la simple vitesse de croissance n’est pas suffisante pour générer des lésions dangereuses. Fait frappant, le sexe jouait aussi un rôle : dans le modèle Kras, les lésions sésarrées avancées survenaient presque exclusivement chez les mâles, alors que les souris Braf‑mutantes des deux sexes étaient touchées de manière similaire. Cela reflète des observations humaines, où certains cancers colorectaux à mutation BRAF sont plus fréquents chez les femmes et les cancers sésarrés à mutation KRAS sont relativement rares.
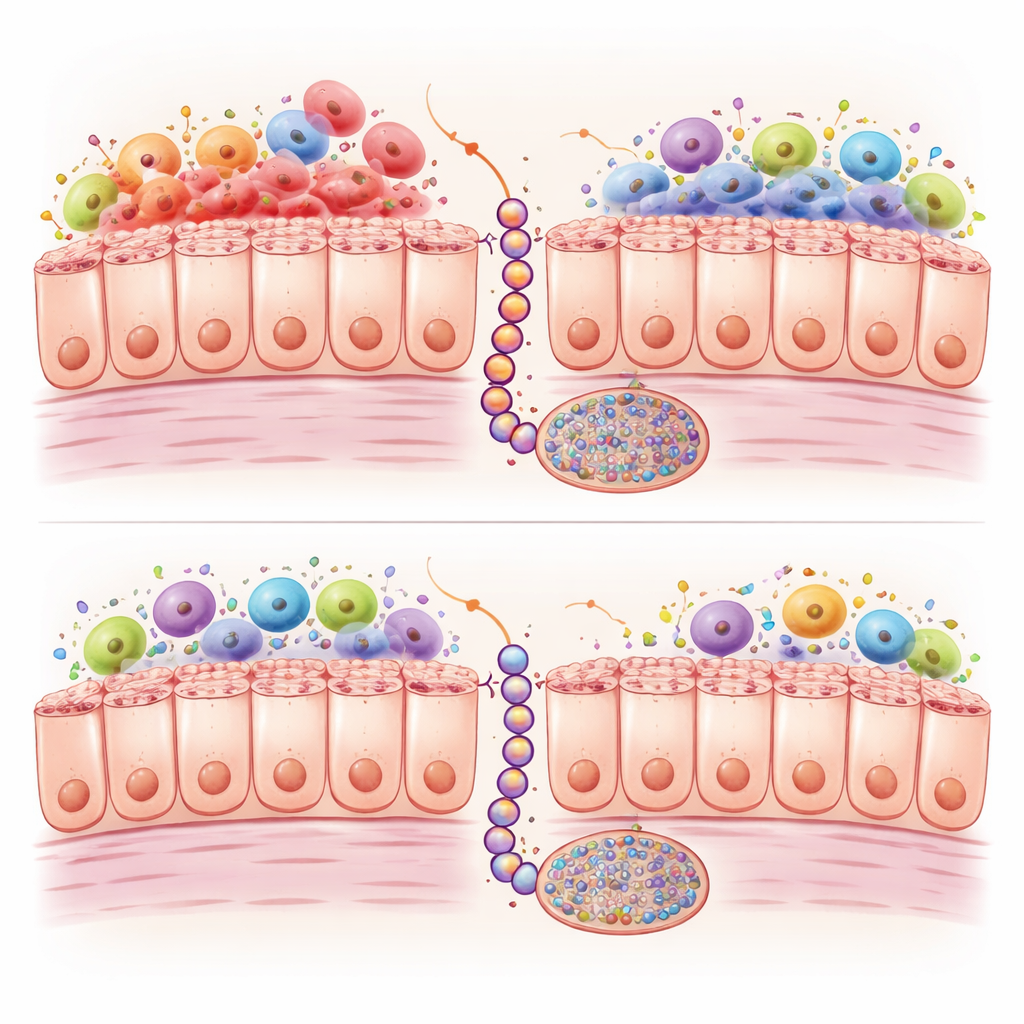
Inflammation et marques chimiques sur l’ADN
En creusant davantage, les chercheurs ont comparé l’activité génique et les marques chimiques sur l’ADN dans les deux modèles au fil du temps. Les intestins Braf‑mutants montraient une forte activation des programmes immunitaires et inflammatoires, avec une présence particulièrement élevée de macrophages de type M1, une catégorie de cellules blanches libérant des signaux inflammatoires intenses. Les intestins Kras‑mutants comptaient moins de ces cellules et présentaient une activation immunitaire plus faible. Parallèlement, les deux mutations entraînaient l’accumulation supplémentaire de groupes méthyle sur de nombreux sites de l’ADN ; chez l’humain, ce qu’on appelle le phénotype CpG island methylator (CIMP) peut réprimer des gènes protecteurs. Cependant, chez les souris Kras cette méthylation s’est installée plus lentement et de façon moins marquée sur plus d’un millier de sites, en particulier dans des gènes liés au contrôle de la croissance cellulaire, aux contacts intercellulaires et à la signalisation WNT, une voie cruciale pour pousser les lésions sésarrées vers un cancer établi.
Une voie clé qui reste pour l’essentiel silencieuse
Une des différences les plus nettes concernait la voie WNT, souvent surexcitée dans les tumeurs colorectales. Dans les souris Braf‑mutantes, des travaux antérieurs avaient montré que de nombreuses lésions acquièrent finalement des altérations qui entraînent la suractivation de la voie WNT, visible par la translocation nucléaire de la protéine β‑caténine. Dans l’étude actuelle, lorsqu’ils ont coloré les lésions sésarrées Kras‑mutantes pour la β‑caténine, presque toutes montraient seulement le motif normal, une seule lésion affichant une faible coloration nucléaire anormale. Cela signifie que, dans le contexte Kras, le « second coup » WNT crucial pour propulser les polypes sésarrés vers le cancer est rarement atteint, probablement parce que la méthylation de l’ADN plus faible et l’environnement d’expression génique différent rendent ces changements moins susceptibles de s’installer.
Ce que cela signifie pour le risque de cancer colorectal
Dans l’ensemble, ces résultats montrent que, bien que BRAF et KRAS agissent dans la même voie de signalisation, ils orientent l’épithélium intestinal sur des trajectoires à long terme très différentes. La mutation Braf associe des signaux inflammatoires puissants, une méthylation de l’ADN marquée et une activation fréquente de la voie WNT, créant un terreau favorable à la progression des lésions sésarrées vers le cancer. La mutation Kras seule peut engendrer des croissances sésarrées, mais avec un démarrage plus lent, une fréquence moindre, moins de modifications de méthylation et peu d’activation de WNT, de sorte que la plupart des lésions restent freinées. Pour les patients, ce travail aide à comprendre pourquoi les polypes sésarrés à mutation BRAF sont considérés comme plus à risque, alors que les lésions sésarrées à mutation KRAS sont à la fois plus rares et moins susceptibles de devenir malignes, sauf si des événements additionnels délétères surviennent.
Citation: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
Mots-clés: cancer colorectal, polypes sésarrés, BRAF et KRAS, méthylation de l’ADN, signalisation WNT