Clear Sky Science · de
Abschwächung des CpG‑Insel‑Methylator‑Phänotyps und fehlende Aktivierung der WNT‑Signalgebung begrenzen Kras‑mutante intestinale Neoplasien
Warum einige Darmpolypen gefährlich werden
Darmkrebs entsteht oft aus kleinen Veränderungen im Darm, doch nicht alle dieser Wucherungen verhalten sich gleich. Diese Studie stellt eine feine, aber wichtige Frage: Wenn zwei eng verwandte krebstreibende Gene fehlregulieren, warum treibt die eine Veränderung die Zellen stark in Richtung Krebs, während die andere häufig ins Stocken gerät? Indem die Forschenden diese Genveränderungen über viele Monate in Mäusen verfolgten, legen sie dar, weshalb einige frühe serratierte Polypen im Darm deutlich wahrscheinlicher zu Krebs fortschreiten als andere.
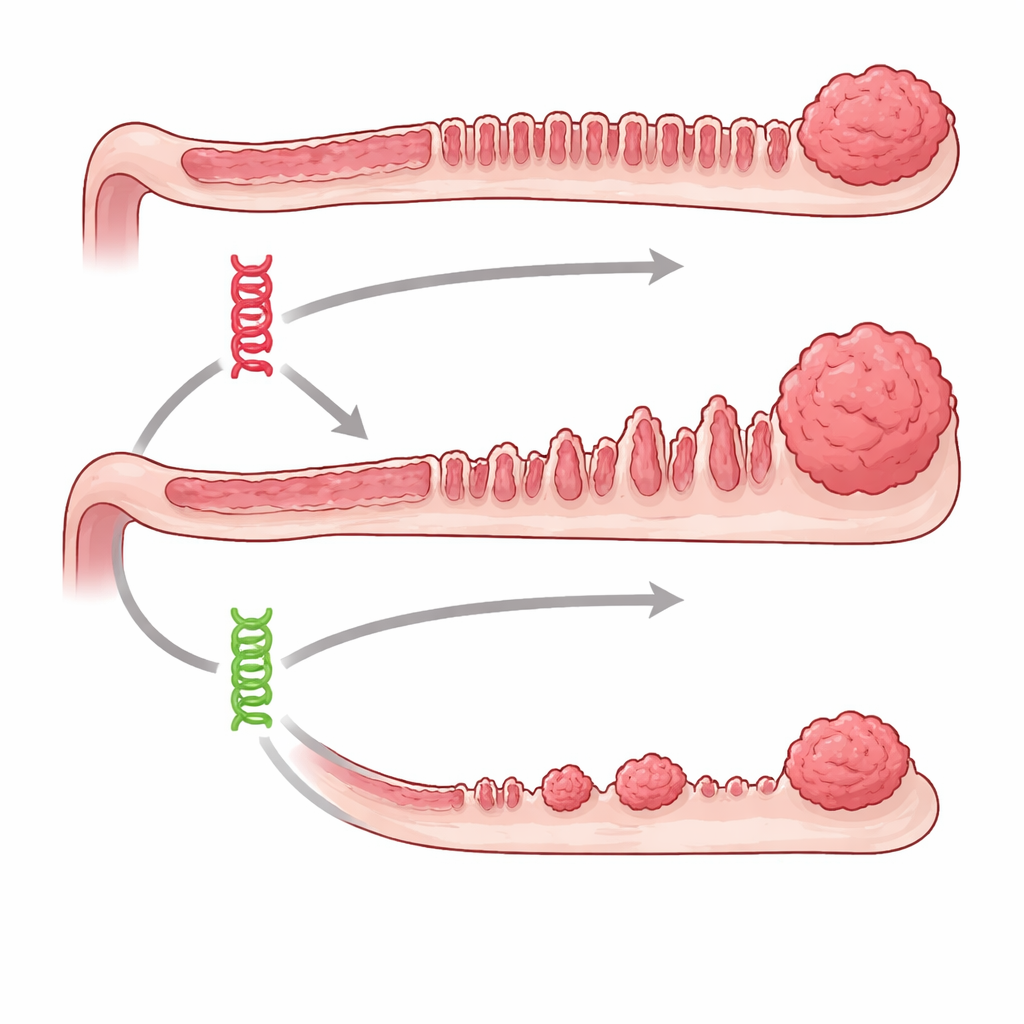
Zwei defekte Schalter mit sehr unterschiedlichen Folgen
Das Team konzentrierte sich auf zwei bekannte Krebs‑Treiber, BRAF und KRAS, die im selben wachstumssteuernden Signalweg innerhalb der Zelle sitzen. Beim Menschen treten Fehler in diesen Genen häufig bei Darmtumoren auf, insbesondere bei Tumoren, die aus serratierten, sägezahnartig aussehenden Polypen entstehen. In transgenen Mäusen konnten die Forschenden entweder die Braf‑ oder die Kras‑Mutation gezielt in der Darmepithelschicht zu einem gewählten Zeitpunkt einschalten und dann bis zu anderthalb Jahre verfolgen, was geschah. Beide Mutationen führten letztlich zu serratierten Läsionen, doch Mäuse mit Braf‑Mutation entwickelten deutlich mehr präkanzeröse Wucherungen, und das viel früher und beständiger als die Kras‑Mutanten. Fortgeschrittene serratierte Tumoren und invasive Karzinome waren in der Braf‑Gruppe häufig, bei alleiniger Kras‑Mutation hingegen auffallend selten.
Wachstumsmuster und Geschlechtsunterschiede im Risiko
Unter dem Mikroskop zeigte sich, dass die Darmabschnitte mit Braf‑Mutation länger und verdickter wurden, mit vergrößerten, schleimgefüllten Krypten, wie sie für serratierte Veränderungen typisch sind. Bei Kras‑mutierten Mäusen traten weniger dramatische strukturelle Veränderungen auf, obwohl einzelne Krypten tatsächlich schneller proliferierten, gemessen an einem Marker für Zellteilung. Das deutet darauf hin, dass reine erhöhte Teilungsrate nicht ausreicht, um gefährliche Läsionen zu erzeugen. Auffällig war auch, dass das Geschlecht eine Rolle spielte: Im Kras‑Modell traten fortgeschrittene serratierte Läsionen fast ausschließlich bei männlichen Mäusen auf, während Braf‑mutierte Mäuse beider Geschlechter ähnlich betroffen waren. Das spiegelt Beobachtungen beim Menschen wider, wo bestimmte BRAF‑mutante Darmkrebse häufiger bei Frauen vorkommen und KRAS‑mutante serratierte Karzinome relativ selten sind.
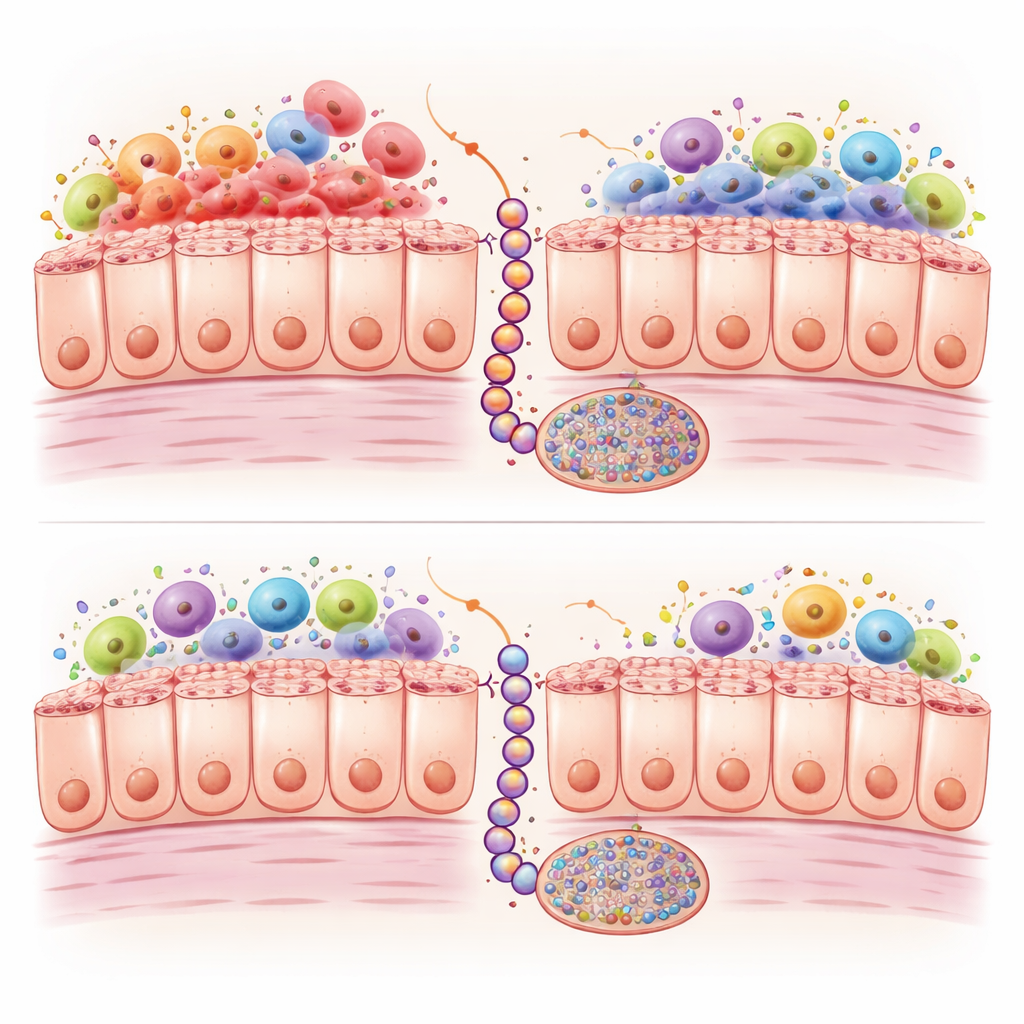
Entzündung und chemische Markierungen auf der DNA
Bei tiefergehender Analyse verglichen die Wissenschaftler die Genaktivität sowie chemische Markierungen auf der DNA in beiden Modellen über die Zeit. Braf‑mutierte Därme zeigten eine starke Aktivierung von Immun‑ und Entzündungsprogrammen, mit besonders hoher Präsenz von M1‑Makrophagen, einer weißen Blutzellvariante, die starke entzündliche Signale aussendet. Kras‑mutierte Därme wiesen weniger dieser Zellen und eine schwächere Immunaktivierung auf. Gleichzeitig führten beide Mutationen zu einer Anreicherung chemischer Anhängsel, sogenannter Methylgruppen, an vielen DNA‑Stellen; beim Menschen kann dieses CpG‑Insel‑Methylator‑Phänotyp (CIMP) schützende Gene abschalten. Bei den Kras‑Mäusen baute sich diese Methylierung jedoch langsamer und in geringerem Ausmaß an über tausend Stellen auf, besonders in Genen, die Zellwachstumskontrolle, Zell‑zu‑Zell‑Kontakte und die WNT‑Signalgebung betreffen — ein Weg, der entscheidend ist, um serratierte Läsionen in Richtung Krebs voranzutreiben.
Ein wichtiger Weg, der weitgehend still bleibt
Einer der klarsten Unterschiede betraf den WNT‑Signalweg, der bei Darmtumoren häufig überaktiv wird. Bei den Braf‑mutierten Mäusen hatte frühere Arbeit gezeigt, dass viele Läsionen schließlich Veränderungen erwerben, die WNT übermäßig aktivieren, sichtbar als Translokation des Proteins β‑Catenin in die Zellkerne. In der aktuellen Studie zeigten gefärbte Kras‑mutierte serratierte Läsionen für β‑Catenin fast ausschließlich das normale Muster; nur eine einzige Läsion wies eine schwache abnorme nukleäre Färbung auf. Das bedeutet, dass im Kras‑Setting der entscheidende WNT‑„zweite Schlag“, der serratierte Polypen üblicherweise zum Krebs treibt, selten erreicht wird — wahrscheinlich weil die abgeschwächte DNA‑Methylierung und das veränderte Genexpressionsumfeld solche Veränderungen weniger wahrscheinlich festigen.
Was das für das Darmkrebsrisiko bedeutet
In der Gesamtschau zeigen die Ergebnisse, dass obwohl BRAF und KRAS im gleichen Signalweg liegen, sie das Darmepithel auf sehr unterschiedliche langfristige Bahnen lenken. Die Braf‑Mutation verbindet starke entzündliche Signale, ausgeprägte DNA‑Methylierung und häufige WNT‑Aktivierung und schafft dadurch fruchtbaren Boden für das Fortschreiten serratierter Läsionen zu Krebs. Die Kras‑Mutation allein kann serratierte Wucherungen erzeugen, jedoch mit späterem Beginn, geringerer Häufigkeit, weniger DNA‑Methylierungsänderungen und kaum WNT‑Aktivierung, sodass die meisten Läsionen eingeschränkt bleiben. Für Patienten hilft diese Arbeit zu erklären, warum BRAF‑mutante serratierte Polypen als höheres Risiko eingestuft werden, während KRAS‑mutante serratierte Läsionen seltener sind und seltener entarten, sofern nicht zusätzliche schädigende Ereignisse eintreten.
Zitation: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
Schlüsselwörter: Kolorektales Karzinom, gesägte Polypen, BRAF und KRAS, DNA‑Methylierung, WNT‑Signalgebung