Clear Sky Science · ru
Ослабление фенотипа метилирования островков CpG и отсутствие активации сигнальной сети WNT сдерживают кишечную неоплазию с мутацией Kras
Почему одни образования в кишечнике становятся опасными
Рак толстой кишки часто начинается с крошечных новообразований в кишечнике, но не все такие образования ведут себя одинаково. В этом исследовании поставлен тонкий, но важный вопрос: когда два близких по функции гена, связанных с раком, дают сбой, почему одна мутация сильно толкает клетки к раку, тогда как другая чаще застревает на этапе незлокачественного роста? Наблюдая за этими изменениями генов у мышей в течение многих месяцев, авторы выяснили, почему одни ранние серратированные полипы в кишечнике существенно более склонны прогрессировать в рак, чем другие.
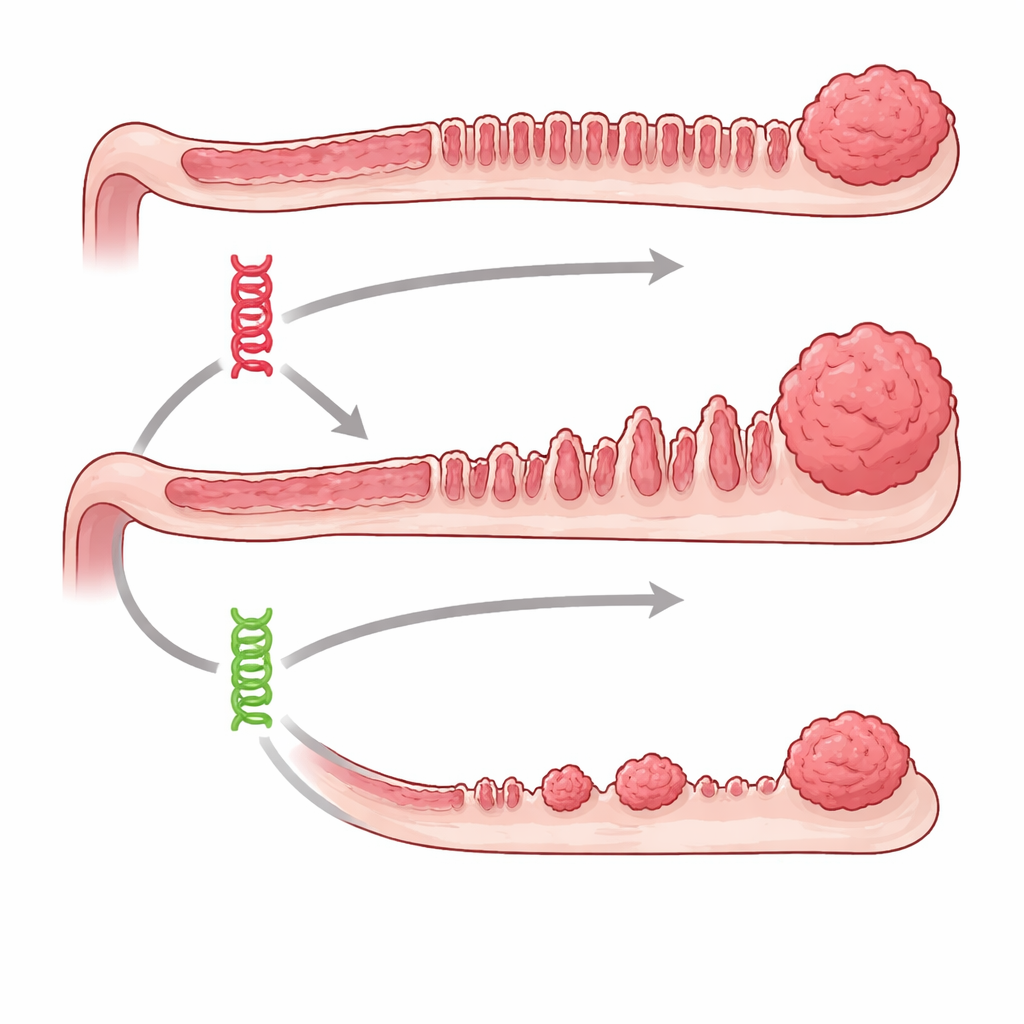
Два неисправных переключателя с очень разными последствиями
Группа сосредоточилась на двух известных драйверах рака — BRAF и KRAS, которые работают в одной и той же каскадной системе контроля роста внутри клетки. У людей ошибки в этих генах часто встречаются при опухолях толстой кишки, особенно тех, которые развиваются из серратированных, пилоподобных полипов. На модельных мышах исследователи могли включать либо мутацию Braf, либо Kras в эпителии кишечника в выбранный момент и затем наблюдать развитие событий до полутора лет. Обе мутации в конечном счёте приводили к появлению серратированного типа поражений, но у мышей с Braf‑мутацией возникало гораздо больше предраковых образований, и они появлялись значительно раньше и стабильнее, чем при Kras‑мутации. Продвинутые серратированные опухоли и инвазивные раки были обычным явлением в группе Braf, тогда как при изолированной мутации Kras они отмечались редко.
Модели роста и различия по полу
При микроскопическом изучении тканей исследователи обнаружили, что кишечник с Braf‑мутацией становился длиннее и утолщённее, с расширёнными криптами, заполненными слизью, типичными для серратированного поражения. У мышей с Kras‑мутацией структурные изменения были менее выражены, хотя отдельные крипты делились активнее, что было видно по маркёру клеточного деления. Это указывает на то, что просто быстрый рост сам по себе недостаточен для формирования опасных образований. Примечательно, что пол животных тоже имел значение: в модели Kras продвинутые серратированные поражения возникали почти исключительно у самцов, тогда как у Braf‑мутаций влияние наблюдалось в равной степени у особей обоих полов. Это коррелирует с человеческими наблюдениями: некоторые BRAF‑мутации в раке толстой кишки более часты у женщин, а серратированные раки с мутацией KRAS встречаются относительно редко.
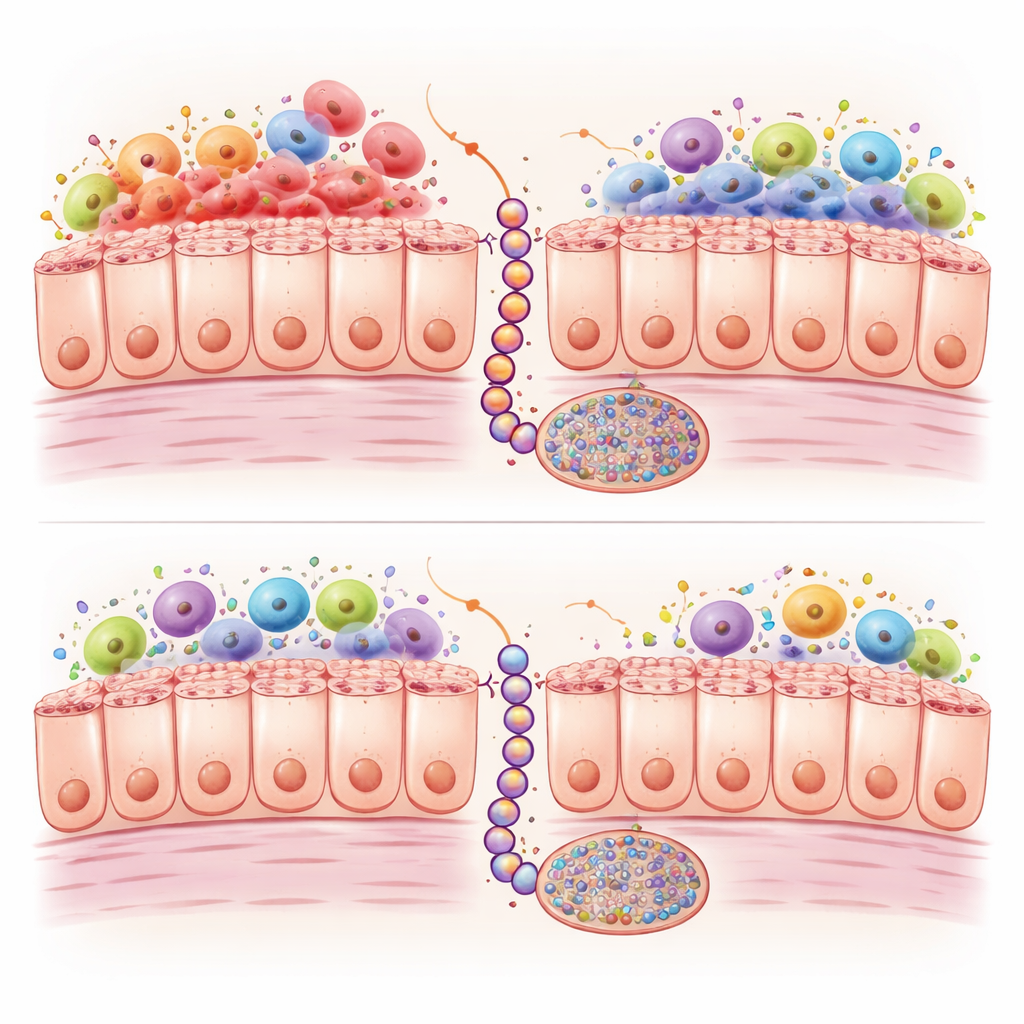
Воспаление и химические метки на ДНК
Углубляясь дальше, учёные сравнивали активность генов и химические метки на ДНК в обеих моделях с течением времени. У кишечника с Braf‑мутацией наблюдалась сильная активация иммунных и воспалительных программ, с особенно высоким присутствием макрофагов типа M1 — разновидности белых кровяных клеток, выделяющих сильные воспалительные сигналы. В тканях с Kras‑мутацией таких клеток было меньше и иммунная активация была слабее. Одновременно обе мутации приводили к накоплению дополнительных химических меток — метильных групп — в ряде участков ДНК; в человеческих опухолях этот так называемый фенотип метилирования островков CpG (CIMP) может выключать защитные гены. Однако у мышей с Kras это метилирование накапливалось медленнее и в меньшей степени на более чем тысяче локусов, особенно в генах, связанных с контролем роста, межклеточными контактами и WNT‑сигнальным путём — ключевым маршрутом, продвигающим серратированные поражения к инвазивному раку.
Ключевой путь, который остаётся в основном тихим
Одно из самых заметных различий касалось пути WNT, который часто гиперактивируется при опухолях толстой кишки. В предыдущих работах на Braf‑мутации показано, что многие поражения в итоге приобретают изменения, активирующие WNT, что видно по перемещению белка β‑катенина в ядра клеток. В текущем исследовании при окрашивании серратированных поражений с Kras‑мутацией на β‑катенин почти все образцы демонстрировали лишь нормальный распределённый рисунок, и лишь в одном случае наблюдалась слабая аномальная ядерная сигнализация. Это означает, что в условиях Kras ключевой «второй удар» по WNT, который обычно продвигает серратированные полипы к раку, достигается редко — вероятно потому, что более слабое метилирование ДНК и иная среда экспрессии генов делают такие изменения менее вероятными для закрепления.
Что это значит для риска рака кишечника
В сумме результаты показывают, что хотя BRAF и KRAS функционируют в одном сигнальном пути, они задают эпителию кишечника очень разные долгосрочные траектории. Мутация Braf связывает сильные воспалительные сигналы, интенсивное метилирование ДНК и частую активацию WNT, создавая благодатную почву для прогрессирования серратированных поражений в рак. Мутация Kras сама по себе способна вызывать серратированные образования, но с более поздним началом, меньшей частотой, менее выраженными изменениями метилирования ДНК и слабой активацией WNT, поэтому большинство поражений остаются сдержанными. Для пациентов эта работа помогает объяснить, почему серратированные полипы с мутацией BRAF считаются более рискованными, тогда как серратированные поражения с мутацией KRAS реже встречаются и менее склонны становиться злокачественными, если не происходят дополнительные повреждающие события.
Цитирование: Fennell, L., Liu, C., Kane, A. et al. Attenuation of the CpG island methylator phenotype and lack of WNT signalling activation restrains Kras mutant intestinal neoplasia. Br J Cancer 134, 1230–1239 (2026). https://doi.org/10.1038/s41416-025-03271-3
Ключевые слова: колоректальный рак, серратированные полипы, BRAF и KRAS, метилирование ДНК, WNT‑сигналинг