Clear Sky Science · zh
通过抑制胱天蛋白酶B防止吞噬作用可增强CAR T细胞功能
这项研究对未来癌症治疗的重要性
CAR T细胞疗法已经改变了某些血液癌症的治疗,使许多患者进入深度缓解。然而,大部分患者最终会复发,常常是因为癌细胞找到方法躲避这些经过工程改造的免疫细胞。本研究揭示了一条此前不清楚的逃逸途径——“吞噬作用”(trogocytosis),即癌细胞将关键表面标志转移给CAR T细胞的过程,并展示了阻断一种酶如何使CAR T细胞更持久、更有效。
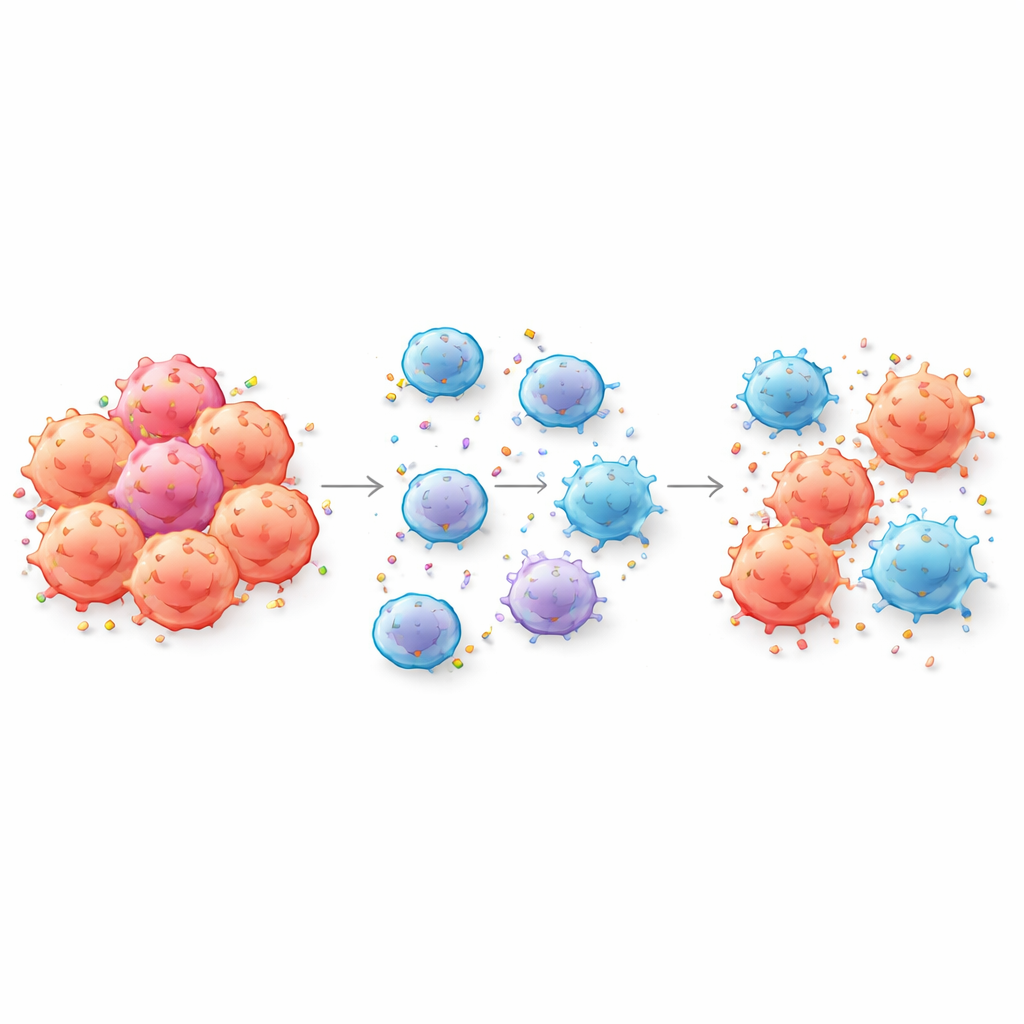
当癌细胞把它们的身份证交出去时
CAR T细胞被设计用来通过识别肿瘤细胞表面的特定标志物或抗原来识别癌症。作者表明,在近距离接触时,CAR T细胞可以实际撕下肿瘤细胞膜的一部分并将这些抗原并入自身表面——这一过程称为吞噬作用。随着这一过程发生,肿瘤细胞失去了CAR T细胞识别它们所需的标志,而CAR T细胞自身则被肿瘤抗原覆盖。研究团队在多种临床重要的靶点上确认了这种交换,包括CD19和BCMA,在血液癌症和实体瘤模型中均可观察到,甚至在CAR T治疗后的患者血液中也检测到了这一现象。
误伤:吞噬作用如何削弱CAR T细胞
一旦CAR T细胞在自身表面携带了肿瘤抗原,它们就会开始将彼此识别为靶点。这会导致“自相残杀”(fratricide),即CAR T细胞互相杀伤,并引发持续的自我刺激,使它们陷入耗竭、功能下降的状态。为证明吞噬作用是直接原因,研究者们构建了一个“吞噬抗原降解器”系统,选择性地摧毁CAR T细胞上被转移的抗原而不影响它们对正常靶标的识别。去除这些获取的抗原显著减少了自相残杀和耗竭标志物的积累,并使CAR T细胞在反复体外挑战中更有效地控制白血病细胞。
追踪并解析抗原窃取过程
为了实时研究吞噬作用,团队建立了一个分裂荧光素酶(split-luciferase)检测系统,仅当抗原片段从肿瘤细胞移动到CAR T细胞时才产生光信号。这个灵敏的读出使他们能够快速筛查可能驱动抗原转移的细胞过程。通过使用小分子抑制剂,他们发现蛋白酶胱天蛋白酶B是关键因素之一。胱天蛋白酶B迅速移动到CAR T细胞与肿瘤细胞接触的区域,其在细胞外的活性足以促进富含抗原的膜片的剥离与摄取。值得注意的是,抑制胱天蛋白酶B可强烈减少吞噬作用,而不会显著损伤CAR T细胞杀伤肿瘤细胞的能力。
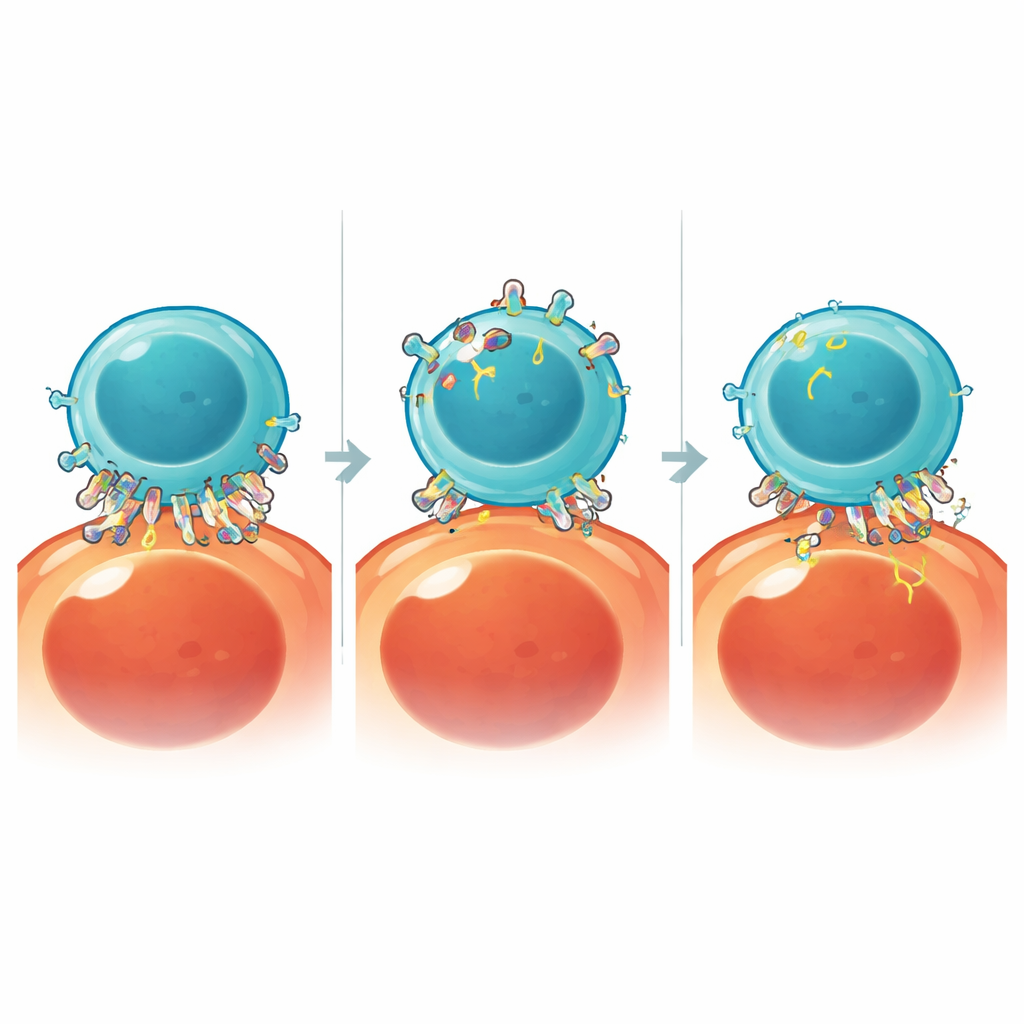
利用天然制动器保护CAR T细胞
体内已有抑制胱天蛋白酶B的天然分子,称为胱抑素。研究者在CAR T细胞内增强了其中一种胱抑素——胱抑素A的表达,结果表明这能安全地降低胱天蛋白酶B的活性,并在多种肿瘤模型中显著减少吞噬作用,包括来自患者的原代白血病细胞。随着抗原窃取减少,CAR T细胞存活更好、数量更多,并在体外培养和小鼠模型中维持更强的长期肿瘤控制。然而,长期表达胱抑素A出乎意料地触发了另一种内部制动——调节蛋白CISH的上调,促进了T细胞耗竭的迹象。通过在过表达胱抑素A的同时敲除CISH,团队得以在减少吞噬作用和自相残杀的同时,将耗竭影响降到最低,进一步延长了CAR T细胞的持久性。
这对患者意味着什么
该研究明确证明,CAR T细胞的抗原窃取不仅是一个有趣的副作用,而是导致治疗失败的直接驱动因素,既造成肿瘤逃逸,也导致治疗细胞自我毁灭。研究还表明,吞噬作用依赖于胱天蛋白酶B,并且可以通过药物或基因学手段(如胱抑素过表达)选择性地将其与抗癌杀伤活性分离开来。未来,预先设计以限制吞噬作用的CAR T产品——或与针对胱天蛋白酶B的精确抑制剂联合使用——可能更持久地保持活性,对癌细胞施加更持久的压力,并降低复发的风险。
引用: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
关键词: CAR T细胞疗法, 吞噬作用, 胱天蛋白酶B, 胱抑素A, 癌症免疫治疗