Clear Sky Science · fr
Prévenir la trogocytose par l’inhibition de la cathépsine B améliore la fonction des cellules CAR T
Pourquoi cette recherche compte pour les thérapies anticancéreuses à venir
La thérapie par cellules CAR T a transformé le traitement de certains cancers du sang, conduisant de nombreux patients à une rémission profonde. Pourtant, une grande proportion de ces patients rechutent finalement, souvent parce que les cellules cancéreuses trouvent des moyens d’échapper à ces cellules immunitaires modifiées. Cette étude met en lumière une voie d’évasion jusque-là mal comprise — la « trogocytose », un processus par lequel les cellules cancéreuses cèdent des marqueurs de surface clés aux cellules CAR T — et montre comment bloquer une seule enzyme peut rendre les cellules CAR T plus durables et plus efficaces.
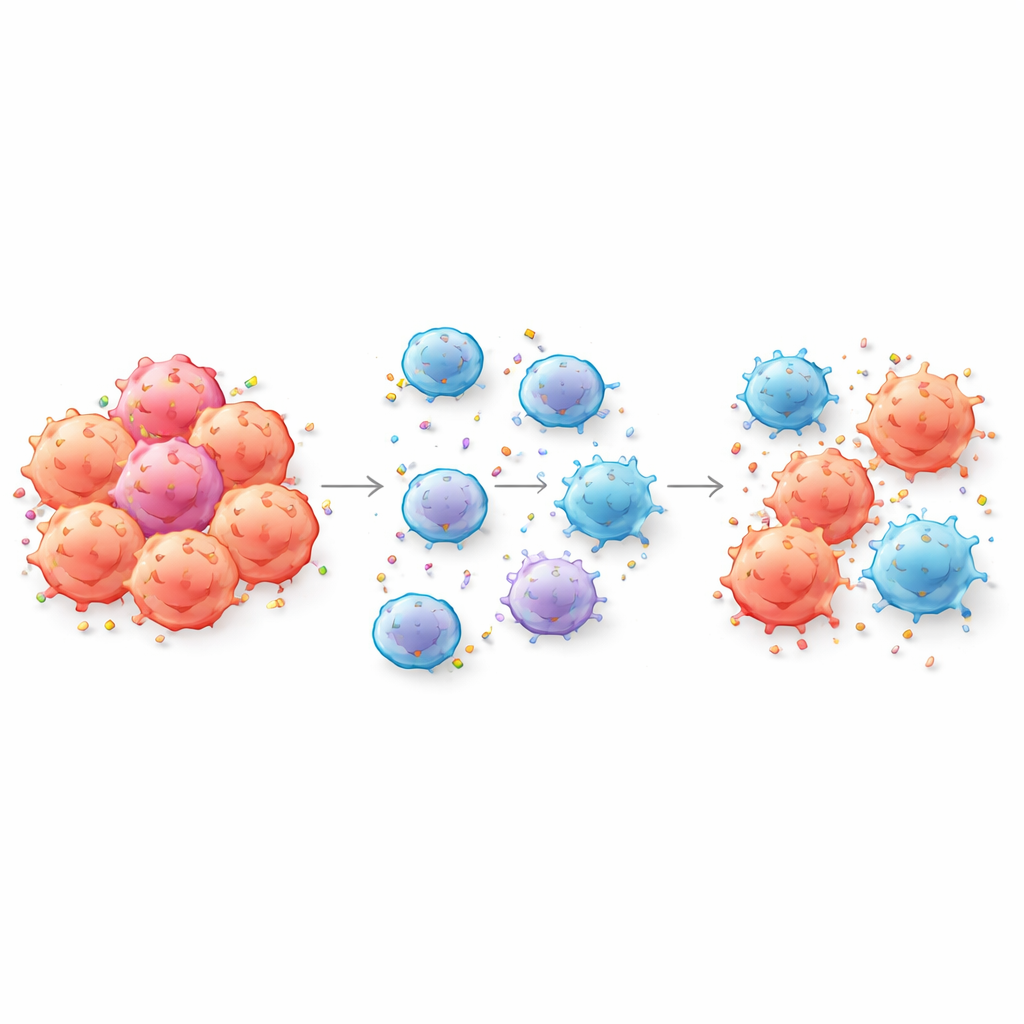
Quand les cellules cancéreuses remettent leurs badges d’identification
Les cellules CAR T sont conçues pour reconnaître le cancer en s’attachant à des marqueurs spécifiques, ou antigènes, à la surface des cellules tumorales. Les auteurs montrent que, lors d’un contact rapproché, les cellules CAR T peuvent littéralement arracher des morceaux de la membrane tumorale et incorporer ces antigènes à leur propre surface — un processus appelé trogocytose. Ce faisant, les cellules tumorales perdent les marqueurs mêmes dont les CAR T ont besoin pour les détecter, tandis que les cellules CAR T elles‑mêmes se retrouvent recouvertes d’antigènes tumoraux. L’équipe a confirmé cet échange pour plusieurs cibles d’intérêt clinique, y compris CD19 et BCMA, dans des modèles de cancers hématologiques et de tumeurs solides, et l’a même détecté dans le sang de patients après un traitement par CAR T.
Tir ami : comment la trogocytose affaiblit les cellules CAR T
Une fois que les cellules CAR T portent des antigènes tumoraux à leur propre surface, elles commencent à se reconnaître mutuellement comme des cibles. Cela conduit à une « fratricide », où les CAR T tuent d’autres CAR T, et à une auto‑stimulation chronique qui les mène à un état d’épuisement et de moindre fonctionnalité. Pour prouver que la trogocytose était la cause directe, les chercheurs ont conçu un système « dégradeur d’antigène trogocytique » qui détruit sélectivement l’antigène transféré sur les CAR T sans affecter leurs cibles normales. L’élimination de ces antigènes acquis a fortement réduit la fratricide et l’accumulation de marqueurs d’épuisement, et a permis aux CAR T de mieux contrôler des cellules leucémiques au cours de défis répétés en laboratoire.
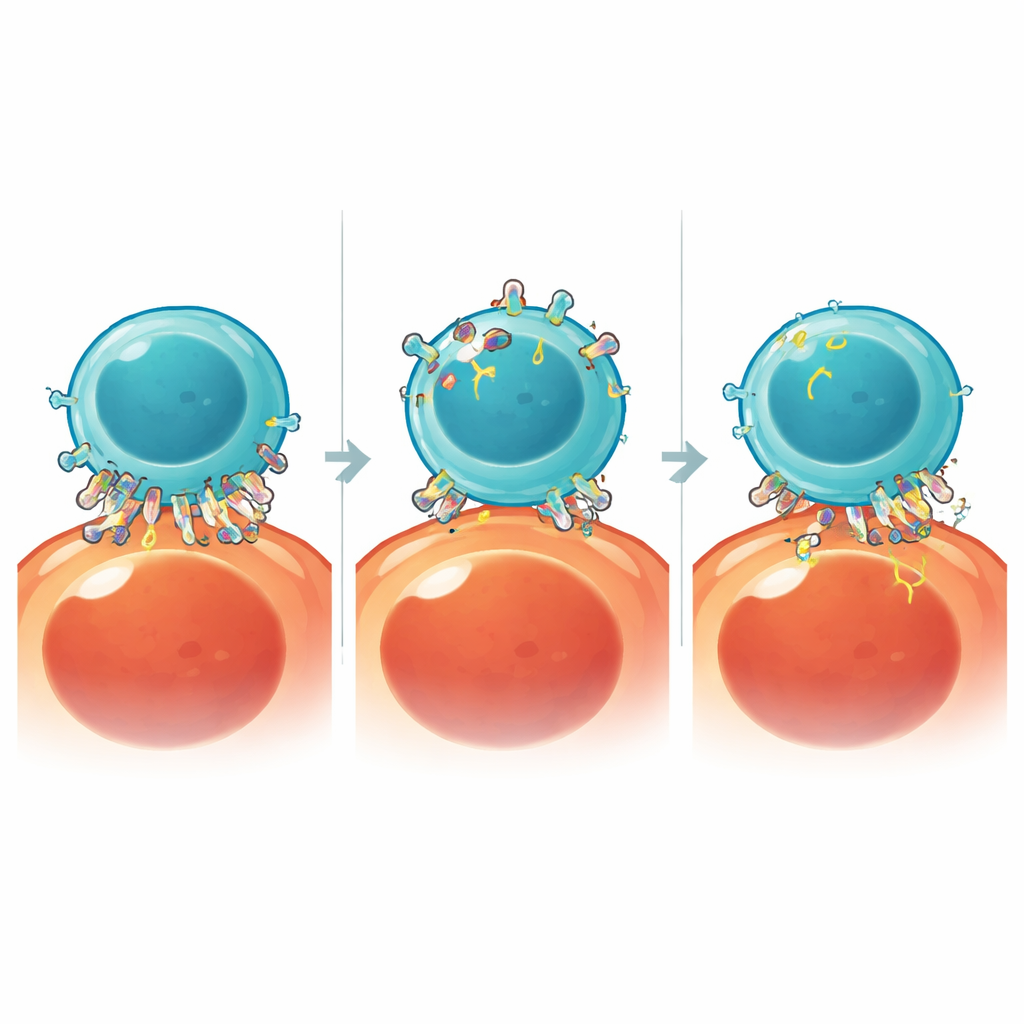
Suivre et disséquer le processus de vol d’antigène
Pour étudier la trogocytose en temps réel, l’équipe a mis au point un test à luciférase divisée dans lequel la lumière n’est produite que lorsque des fragments d’antigène passent des cellules tumorales aux cellules CAR T. Cette mesure sensible a permis le criblage rapide des processus cellulaires susceptibles de favoriser le transfert d’antigène. À l’aide d’inhibiteurs de petites molécules, ils ont découvert que l’enzyme cathépsine B, une protéase normalement impliquée dans la dégradation des protéines, joue un rôle clé. La cathépsine B se déplace rapidement vers la zone de contact où les CAR T interagissent avec les cellules tumorales, et son activité extracellulaire suffit à favoriser le décollage et l’absorption de fragments de membrane riches en antigènes. Fait remarquable, bloquer la cathépsine B a fortement réduit la trogocytose sans altérer de manière significative la capacité des CAR T à tuer les cellules tumorales.
Utiliser des freins naturels pour protéger les cellules CAR T
L’organisme contient déjà des inhibiteurs naturels de la cathépsine B, appelés cystatines. Les chercheurs ont augmenté l’expression d’une de ces cystatines, la cystatine A, à l’intérieur des cellules CAR T et ont montré que cela réduisait en toute sécurité l’activité de la cathépsine B et diminuait fortement la trogocytose dans plusieurs modèles tumoraux, y compris des cellules leucémiques primaires d’un patient. Avec moins de vol d’antigènes, les CAR T survivaient mieux, s’accumulaient en plus grand nombre et maintenaient un meilleur contrôle tumoral à long terme en culture et chez la souris. Cependant, l’expression chronique de la cystatine A a déclenché de façon inattendue un frein interne distinct — l’augmentation de l’expression de la protéine régulatrice CISH — qui favorisait des signes d’épuisement des cellules T. En supprimant CISH tout en surexprimant la cystatine A, l’équipe a pu conserver les bénéfices d’une trogocytose et d’une fratricide réduites tout en minimisant l’épuisement, prolongeant ainsi davantage la persistance des CAR T.
Ce que cela pourrait signifier pour les patients
Ce travail apporte une preuve nette que le vol d’antigène par les cellules CAR T n’est pas qu’un effet secondaire curieux mais un moteur direct d’échec thérapeutique, provoquant à la fois l’échappement tumoral et l’autodestruction des cellules thérapeutiques. Il montre également que la trogocytose dépend de la cathépsine B et peut être découplée sélectivement de l’activité cytotoxique contre le cancer à l’aide de médicaments ou de stratégies génétiques comme la surexpression de cystatine. À l’avenir, des produits CAR T pré-ingénierés pour limiter la trogocytose — ou associés à des inhibiteurs ciblés de la cathépsine B — pourraient rester actifs plus longtemps, exercer une pression plus soutenue sur les cellules cancéreuses et réduire les risques de rechute.
Citation: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
Mots-clés: thérapie par cellules CAR T, trogocytose, cathépsine B, cystatine A, immunothérapie contre le cancer