Clear Sky Science · pl
Zapobieganie trogocytozie przez hamowanie katepsyny B wzmacnia funkcję limfocytów CAR T
Dlaczego to badanie ma znaczenie dla przyszłych terapii przeciwnowotworowych
Terapia komórkami CAR T zrewolucjonizowała leczenie niektórych nowotworów krwi, doprowadzając wielu pacjentów do głębokiej remisji. Mimo to znaczna część tych pacjentów ostatecznie doświadcza nawrotu, często dlatego, że komórki nowotworowe znajdują sposoby, by ukryć się przed tymi zmodyfikowanymi komórkami odpornościowymi. W badaniu odkryto wcześniej niejasną ścieżkę ucieczki — „trogocytozę”, proces, w którym komórki nowotworowe oddają kluczowe markerowe powierzchniowe komórkom CAR T — oraz pokazano, że zablokowanie jednego enzymu może uczynić komórki CAR T bardziej trwałymi i skutecznymi.
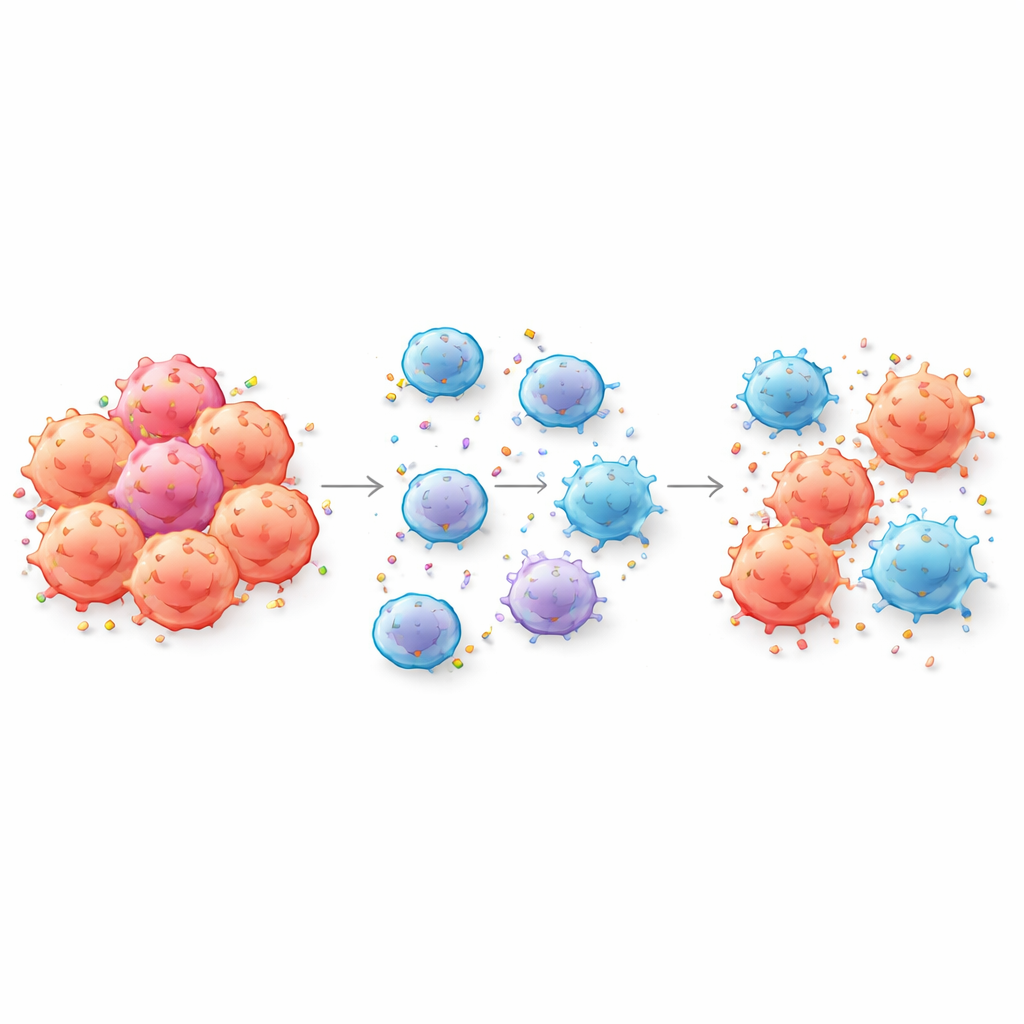
Kiedy komórki nowotworowe przekazują swoje identyfikatory
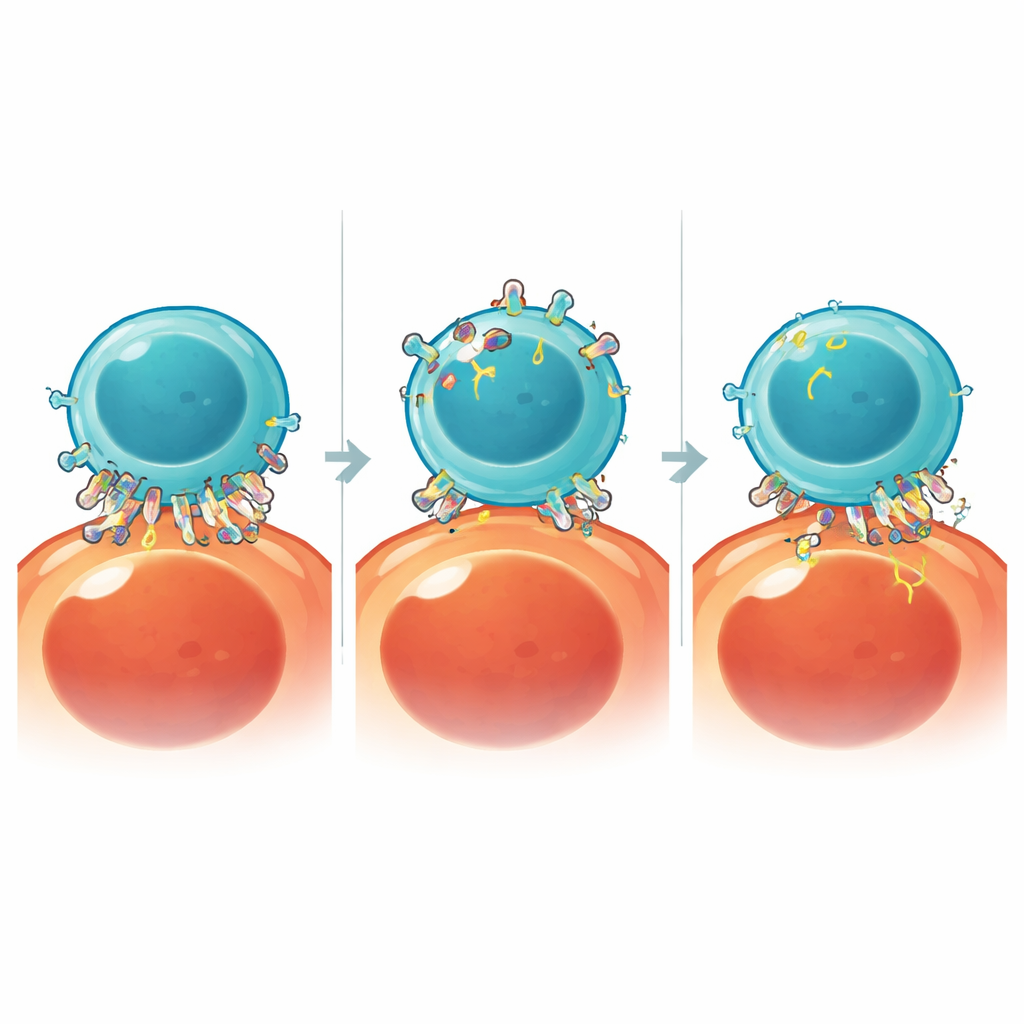
Komórki CAR T zaprojektowano tak, by rozpoznawały nowotwór poprzez chwytanie specyficznych markerów, czyli antygenów, na powierzchni komórek guza. Autorzy pokazują, że podczas ścisłego kontaktu komórki CAR T mogą dosłownie oderwać kawałki błony guza i włączyć te antygeny do własnej powierzchni — proces zwany trogocytozą. W wyniku tego komórki guza tracą te same markery, których CAR T potrzebują do ich wykrycia, podczas gdy same komórki CAR T stają się pokryte antygenami nowotworowymi. Zespół potwierdził tę wymianę dla kilku klinicznie istotnych celów, w tym CD19 i BCMA, zarówno w nowotworach krwi, jak i modelach guzów litych, a także wykrył ją we krwi pacjentów po leczeniu CAR T.
Friendly fire: jak trogocytoza osłabia komórki CAR T
Gdy komórki CAR T niosą antygeny nowotworowe na własnej powierzchni, zaczynają rozpoznawać siebie nawzajem jako cele. Prowadzi to do „bratobójstwa” (fratricide), czyli zabijania się komórek CAR T nawzajem, oraz do przewlekłej auto-stymulacji, która doprowadza je do stanu wyczerpania i mniejszej funkcjonalności. Aby dowieść, że trogocytoza jest bezpośrednią przyczyną, badacze skonstruowali system „degradera antygenu trogocytowego”, który selektywnie niszczy przeniesiony antygen na komórkach CAR T, nie wpływając na ich normalne cele. Usunięcie tych pozyskanych antygenów wyraźnie zmniejszyło bratobójstwo i narastanie markerów wyczerpania oraz pozwoliło komórkom CAR T skuteczniej kontrolować komórki białaczkowe podczas powtarzanych wyzwań w warunkach laboratoryjnych.
Śledzenie i rozkładanie procesu kradzieży antygenów
Aby badać trogocytozę w czasie rzeczywistym, zespół opracował test split-lucyferazy, w którym światło powstaje tylko wtedy, gdy fragmenty antygenu przemieszczają się z komórek guza do komórek CAR T. Ten czuły odczyt umożliwił szybkie przesiewanie procesów komórkowych, które mogą napędzać transfer antygenu. Przy użyciu inhibitorów w postaci małych cząsteczek odkryli, że enzym katepsyna B, proteaza zwykle zaangażowana w rozkład białek, jest kluczowym graczem. Katepsyna B szybko przemieszcza się do strefy kontaktu, gdzie komórki CAR T łączą się z komórkami guza, a jej aktywność na zewnątrz komórki jest wystarczająca, by promować odrywanie i pobieranie fragmentów błony bogatych w antygeny. Co ważne, zablokowanie katepsyny B znacząco zmniejszyło trogocytozę bez istotnego osłabienia zdolności komórek CAR T do zabijania komórek nowotworowych.
Wykorzystanie naturalnych hamulców do ochrony komórek CAR T
Organizm naturalnie zawiera inhibitorów katepsyny B, znanych jako cystatyny. Badacze zwiększyli poziom jednej z nich, cystatyny A, wewnątrz komórek CAR T i wykazali, że bezpiecznie zmniejszyło to aktywność katepsyny B oraz zdecydowanie ograniczyło trogocytozę w wielu modelach nowotworowych, w tym w pierwotnych komórkach białaczki od pacjenta. Przy mniejszej kradzieży antygenów komórki CAR T lepiej przetrwały, gromadziły się w większych liczbach i utrzymywały silniejszą długoterminową kontrolę guza zarówno w hodowlach, jak i w modelach mysich. Jednak przewlekła ekspresja cystatyny A nieoczekiwanie uruchomiła inny wewnętrzny hamulec — wzrost poziomu regulatorowego białka CISH — co sprzyjało oznakom wyczerpania limfocytów T. Poprzez wyeliminowanie CISH przy jednoczesnym nadekspresji cystatyny A zespół mógł zachować korzyści wynikające z ograniczenia trogocytozy i bratobójstwa, przy jednoczesnym zminimalizowaniu wyczerpania, co dodatkowo wydłużyło przetrwanie komórek CAR T.
Co to może znaczyć dla pacjentów
Praca ta dostarcza przekonujących dowodów, że kradzież antygenów przez komórki CAR T nie jest jedynie ciekawostką, lecz bezpośrednim czynnikiem prowadzącym do niepowodzenia leczenia, powodującym zarówno ucieczkę guza, jak i samodestrukcję komórek terapeutycznych. Pokazuje również, że trogocytoza zależy od katepsyny B i można ją selektywnie rozdzielić od aktywności zabijania nowotworu za pomocą leków lub genetycznych trików, takich jak nadekspresja cystatyny. W przyszłości produkty CAR T wstępnie zaprojektowane tak, by ograniczać trogocytozę — lub stosowane w połączeniu ze specyficznymi inhibitorami katepsyny B — mogą działać dłużej, utrzymywać silniejszą presję na komórki nowotworowe i zmniejszać ryzyko nawrotu.
Cytowanie: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
Słowa kluczowe: terapia CAR T, trogocytoza, katepsyna B, cystatyna A, immunoterapia nowotworów