Clear Sky Science · es
Prevenir la trogocitosis mediante la inhibición de la catepsina B potencia la función de las células CAR-T
Por qué esta investigación importa para las futuras terapias contra el cáncer
La terapia con células CAR-T ha transformado el tratamiento de ciertos cánceres hematológicos, llevando a muchos pacientes a remisiones profundas. Sin embargo, una gran proporción de esos pacientes acaba recayendo, a menudo porque las células cancerosas encuentran maneras de evadirse de estas células inmunitarias diseñadas. Este estudio desvela una vía de escape hasta ahora poco clara—la “trogocitosis”, un proceso en el que las células tumorales ceden marcadores superficiales clave a las células CAR-T—y muestra cómo bloquear una sola enzima puede hacer que las células CAR-T sean más duraderas y efectivas.
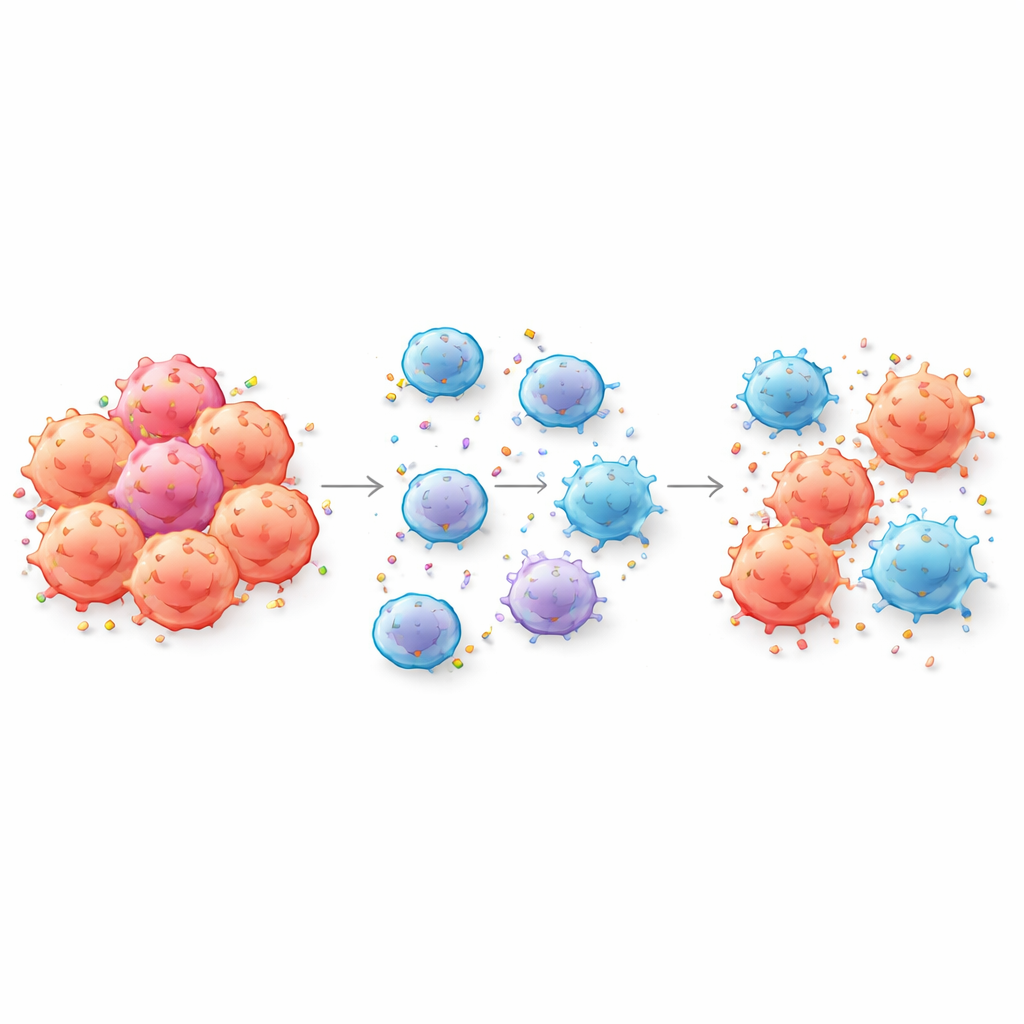
Cuando las células tumorales entregan sus etiquetas de identificación
Las células CAR-T están diseñadas para reconocer el cáncer aferrándose a marcadores específicos, o antígenos, en la superficie de las células tumorales. Los autores muestran que, durante el contacto estrecho, las células CAR-T pueden literalmente arrancar fragmentos de la membrana del tumor e incorporar esos antígenos en su propia superficie—un proceso llamado trogocitosis. A medida que esto ocurre, las células tumorales pierden los marcadores que las células CAR-T necesitan para detectarlas, mientras que las propias CAR-T quedan recubiertas de antígenos tumorales. El equipo confirmó este intercambio para varios dianas de relevancia clínica, incluyendo CD19 y BCMA, tanto en modelos de cáncers sanguíneos como de tumores sólidos, e incluso lo detectaron en la sangre de pacientes tras el tratamiento con CAR-T.
Fuego amigo: cómo la trogocitosis debilita a las células CAR-T
Una vez que las células CAR-T llevan antígenos tumorales en su propia superficie, comienzan a reconocerse entre sí como objetivos. Esto conduce a la “fratricida”, donde las CAR-T matan a otras CAR-T, y a una autoestimulación crónica que las empuja hacia un estado de agotamiento y menor funcionalidad. Para demostrar que la trogocitosis era la causa directa, los investigadores diseñaron un sistema “degradador de antígenos trogocíticos” que destruye selectivamente el antígeno transferido en las CAR-T sin afectar a sus dianas normales. Eliminando estos antígenos adquiridos se redujo drásticamente la fratricida y la acumulación de marcadores de agotamiento, y permitió a las CAR-T controlar las células leucémicas con mayor eficacia tras desafíos repetidos en el laboratorio.
Rastrear y diseccionar el proceso de robo de antígenos
Para estudiar la trogocitosis en tiempo real, el equipo construyó un ensayo de luciferasa dividida en el que se produce luz solo cuando fragmentos de antígeno se mueven de las células tumorales a las células CAR-T. Esta lectura sensible permitió cribar rápidamente los procesos celulares que podrían impulsar la transferencia de antígenos. Usando inhibidores de pequeñas moléculas, descubrieron que la enzima catepsina B, una proteasa normalmente implicada en la degradación de proteínas, es un actor clave. La catepsina B se desplaza rápidamente a la zona de contacto donde las CAR-T interactúan con las células tumorales, y su actividad extracelular es suficiente para promover el desprendimiento y la captación de fragmentos de membrana ricos en antígenos. De forma notable, bloquear la catepsina B redujo fuertemente la trogocitosis sin perjudicar de forma significativa la capacidad de las CAR-T para matar células tumorales.
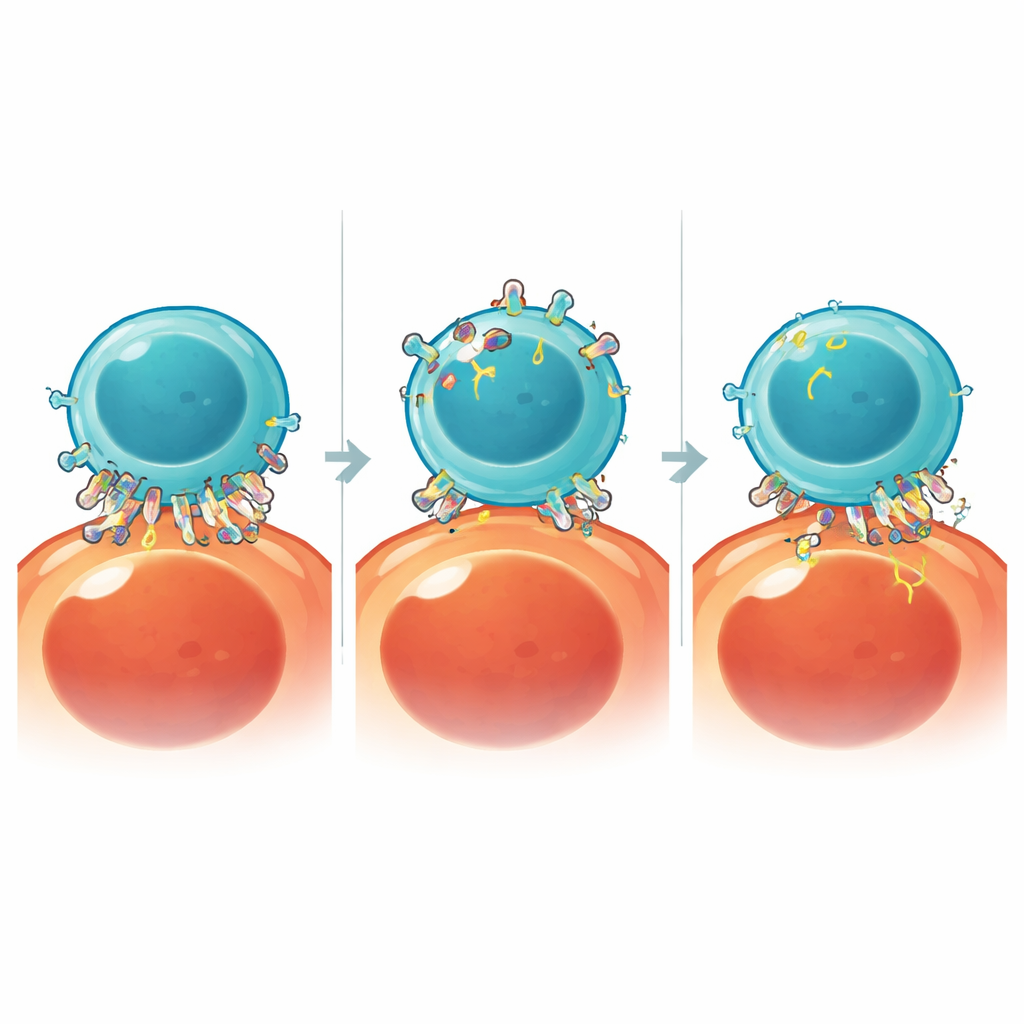
Usar frenos naturales para proteger a las células CAR-T
El organismo ya contiene inhibidores naturales de la catepsina B, conocidos como cistatinas. Los investigadores aumentaron uno de estos, la cistatina A, dentro de las células CAR-T y demostraron que esto reducía de forma segura la actividad de la catepsina B y disminuía notablemente la trogocitosis en múltiples modelos tumorales, incluidas células leucémicas primarias de un paciente. Con menos robo de antígenos, las CAR-T supervivieron mejor, se acumularon en mayor número y mantuvieron un control tumoral a largo plazo más sólido tanto en placas de cultivo como en modelos murinos. Sin embargo, la expresión crónica de cistatina A desencadenó de forma inesperada un freno interno separado—la regulación al alza de la proteína reguladora CISH—que promovió signos de agotamiento de las células T. Al eliminar CISH mientras sobreexpresaban cistatina A, el equipo pudo conservar los beneficios de reducir la trogocitosis y la fratricida, minimizando a la vez el agotamiento y prolongando aún más la persistencia de las CAR-T.
Qué podría significar esto para los pacientes
Este trabajo proporciona evidencia clara de que el robo de antígenos por parte de las células CAR-T no es solo un efecto secundario curioso, sino un impulsor directo del fracaso del tratamiento, provocando tanto la escapatoria tumoral como la autodestrucción de las células terapéuticas. También muestra que la trogocitosis depende de la catepsina B y puede desacoplarse selectivamente de la actividad citotóxica mediante fármacos o trucos genéticos como la sobreexpresión de cistatina. En el futuro, los productos CAR-T preingeniería dos para limitar la trogocitosis—o combinados con inhibidores inteligentes de la catepsina B—podrían permanecer activos por más tiempo, mantener una presión más sostenida sobre las células cancerosas y reducir las probabilidades de recaída.
Cita: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
Palabras clave: Terapia con células CAR-T, trogocitosis, catepsina B, cistatina A, inmunoterapia contra el cáncer