Clear Sky Science · it
Prevenire la trogocitosi mediante l’inibizione della cathepsina B potenzia la funzione delle cellule CAR T
Perché questa ricerca conta per le terapie oncologiche future
La terapia con cellule CAR T ha rivoluzionato il trattamento di alcuni tumori del sangue, portando molti pazienti in remissione profonda. Tuttavia una grande parte di questi pazienti va incontro a recidiva, spesso perché le cellule tumorali trovano modi per sfuggire a queste cellule immunitarie ingegnerizzate. Questo studio mette in luce una via di fuga finora poco chiara — la “trogocitosi”, un processo in cui le cellule tumorali cedono marcatori di superficie chiave alle CAR T — e mostra come bloccare un singolo enzima possa rendere le CAR T più durature ed efficaci.
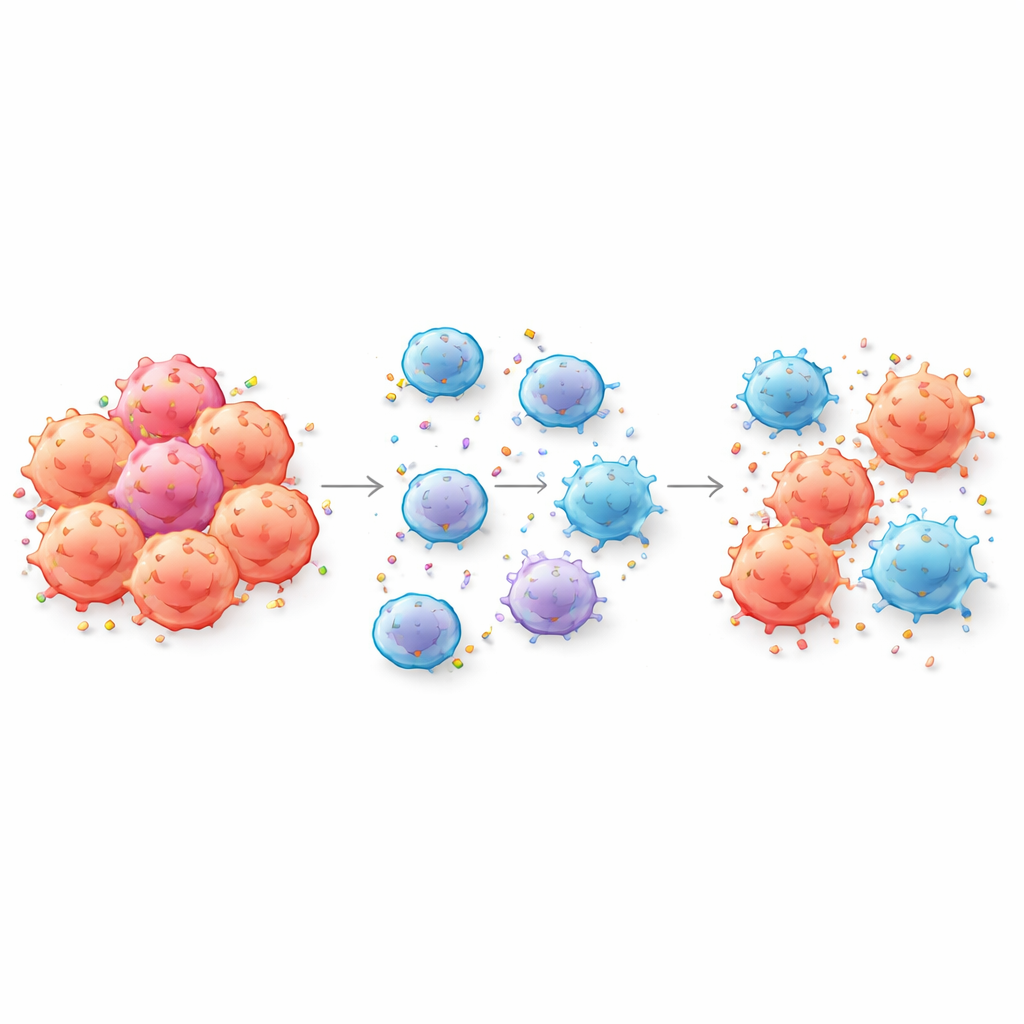
Quando le cellule tumorali consegnano i loro tag identificativi
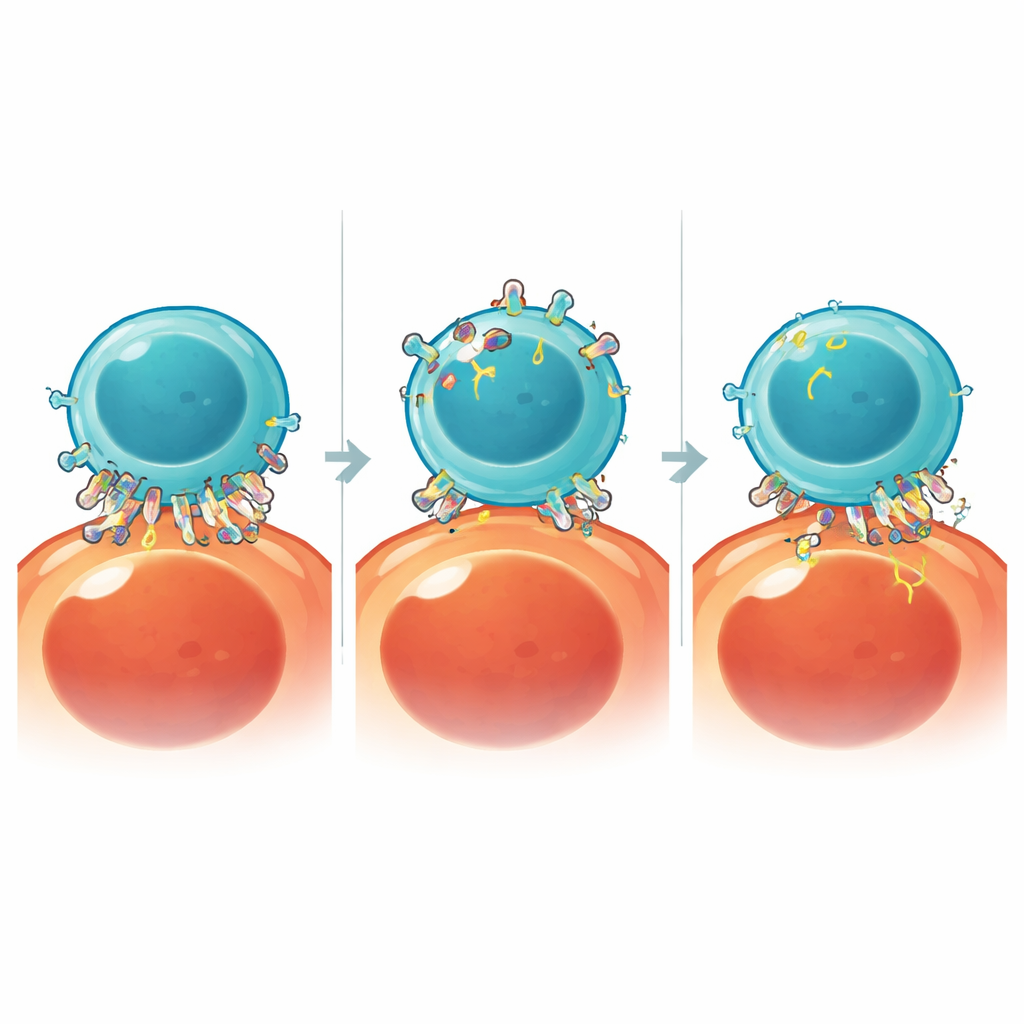
Le cellule CAR T sono progettate per riconoscere il cancro agganciandosi a marcatori specifici, o antigeni, sulla superficie della cellula tumorale. Gli autori dimostrano che, durante il contatto ravvicinato, le CAR T possono letteralmente strappare frammenti della membrana del tumore e incorporare quegli antigeni nella propria superficie — un processo chiamato trogocitosi. Nell’evento, le cellule tumorali perdono i marcatori che le CAR T usano per individuarle, mentre le CAR T stesse si rivestono di antigeni tumorali. Il gruppo ha confermato questo scambio per diversi bersagli clinicamente importanti, tra cui CD19 e BCMA, sia nei tumori ematologici sia nei modelli di tumore solido, e lo ha rilevato perfino nel sangue di pazienti dopo il trattamento con CAR T.
Danni collaterali: come la trogocitosi indebolisce le CAR T
Una volta che le CAR T portano antigeni tumorali sulla propria superficie, cominciano a riconoscersi reciprocamente come bersagli. Questo porta alla “fratricidio”, in cui le CAR T uccidono altre CAR T, e a una auto-stimolazione cronica che le spinge in uno stato di esaurimento con funzionalità ridotta. Per dimostrare che la trogocitosi era la causa diretta, i ricercatori hanno ingegnerizzato un sistema "degradatore di antigeni trogocitici" che distrugge selettivamente l’antigene trasferito sulle CAR T senza influenzare i loro bersagli normali. Rimuovere questi antigeni acquisiti ha ridotto nettamente la fratricidio e l’accumulo di marcatori di esaurimento, e ha permesso alle CAR T di controllare le cellule leucemiche in modo più efficace durante sfide ripetute in laboratorio.
Tracciare e analizzare il processo di furto degli antigeni
Per studiare la trogocitosi in tempo reale, il team ha sviluppato un saggio split-luciferasi in cui si produce luce solo quando frammenti di antigene si spostano dalle cellule tumorali alle CAR T. Questo lettore sensibile ha permesso uno screening rapido dei processi cellulari che potrebbero guidare il trasferimento degli antigeni. Utilizzando inibitori di piccole molecole, hanno scoperto che l’enzima cathepsina B, una proteasi normalmente coinvolta nella degradazione delle proteine, è un protagonista chiave. La cathepsina B si concentra rapidamente nella zona di contatto dove le CAR T interagiscono con le cellule tumorali, e la sua attività extracellulare è sufficiente a promuovere il distacco e l’assorbimento di frammenti di membrana ricchi di antigeni. Sorprendentemente, bloccare la cathepsina B ha ridotto fortemente la trogocitosi senza compromettere in modo significativo la capacità delle CAR T di uccidere le cellule tumorali.
Usare freni naturali per proteggere le CAR T
Il corpo contiene già inibitori naturali della cathepsina B, noti come cistatins. I ricercatori hanno aumentato uno di questi, la cistatina A, all’interno delle CAR T e hanno dimostrato che ciò riduceva in modo sicuro l’attività della cathepsina B e riduceva nettamente la trogocitosi in diversi modelli tumorali, incluse cellule leucemiche primarie di un paziente. Con meno furti di antigeni, le CAR T sono sopravvissute meglio, si sono accumulate in numero maggiore e hanno mantenuto un controllo tumorale a lungo termine più forte sia in colture che in modelli murini. Tuttavia, l’espressione cronica di cistatina A ha inaspettatamente attivato un freno interno separato — l’aumento dell’espressione della proteina regolatoria CISH — che ha favorito segnali di esaurimento delle cellule T. Eliminando CISH mentre si sovraesprimeva la cistatina A, il gruppo è riuscito a conservare i benefici della ridotta trogocitosi e fratricidio minimizzando l’esaurimento, estendendo ulteriormente la persistenza delle CAR T.
Cosa potrebbe significare per i pazienti
Questo lavoro fornisce prove chiare che il furto di antigeni da parte delle CAR T non è solo un curioso effetto collaterale ma un fattore diretto di insuccesso terapeutico, causando sia la fuga tumorale sia l’autodistruzione delle cellule terapeutiche. Mostra inoltre che la trogocitosi dipende dalla cathepsina B e può essere disaccoppiata selettivamente dall’attività citotossica mediante farmaci o stratagemmi genetici come la sovraespressione di cistatina. In futuro, prodotti CAR T pre-ingegnerizzati per limitare la trogocitosi — o combinati con inibitori mirati della cathepsina B — potrebbero restare attivi più a lungo, esercitare una pressione migliore sulle cellule tumorali e ridurre il rischio di recidiva.
Citazione: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
Parole chiave: Terapia con cellule CAR T, trogocitosi, cathepsina B, cistatina A, immunoterapia del cancro