Clear Sky Science · pt
Prevenir a trogocitose pela inibição da catepsina B aumenta a função das células CAR T
Por que esta pesquisa importa para terapias futuras contra o câncer
A terapia com células CAR T transformou o tratamento de certos cânceres hematológicos, levando muitos pacientes a remissões profundas. Ainda assim, uma grande parte desses pacientes eventualmente recai, frequentemente porque as células tumorais encontram formas de se esconder dessas células imunes modificadas. Este estudo revela uma rota de escape antes obscura — a "trogocitose", um processo em que células tumorais cedem marcadores de superfície essenciais para as células CAR T — e mostra como bloquear uma única enzima pode tornar as células CAR T mais duráveis e eficazes.
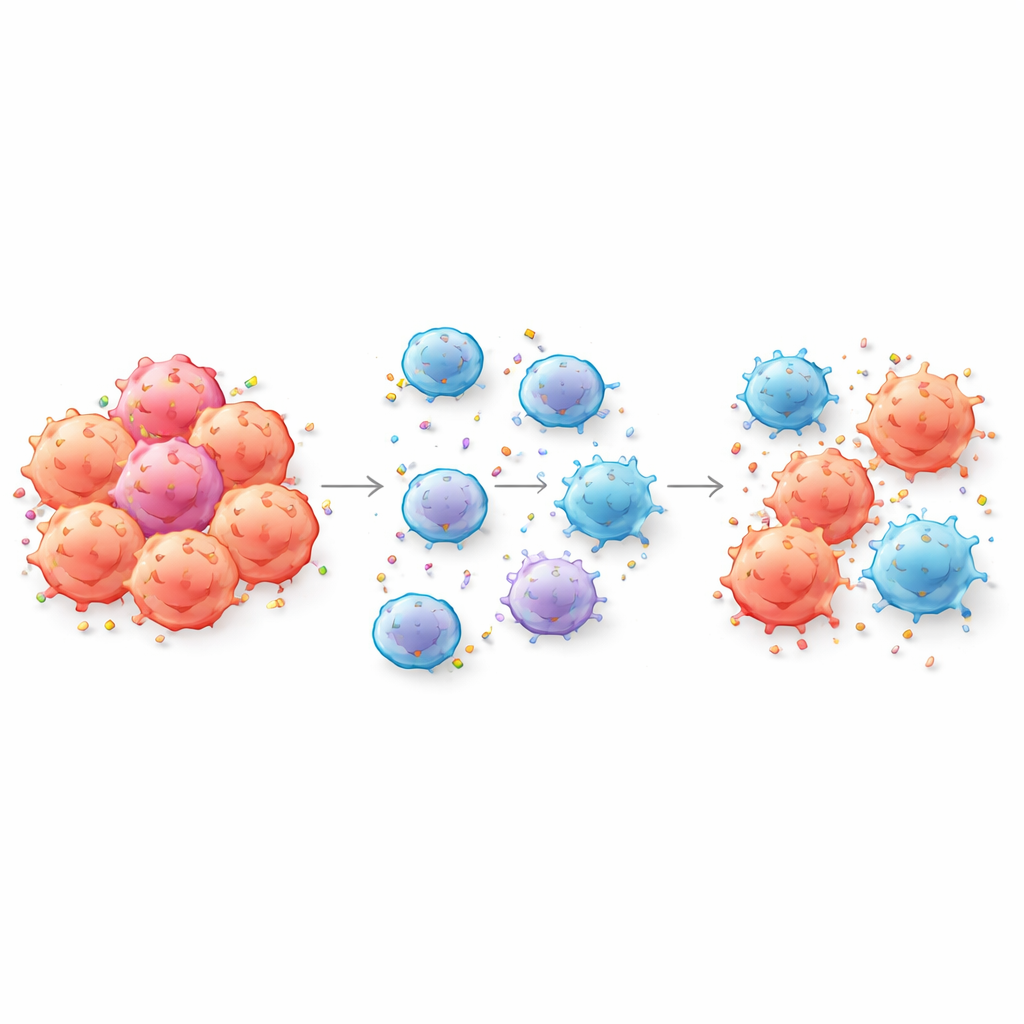
Quando as células tumorais entregam suas etiquetas de identificação
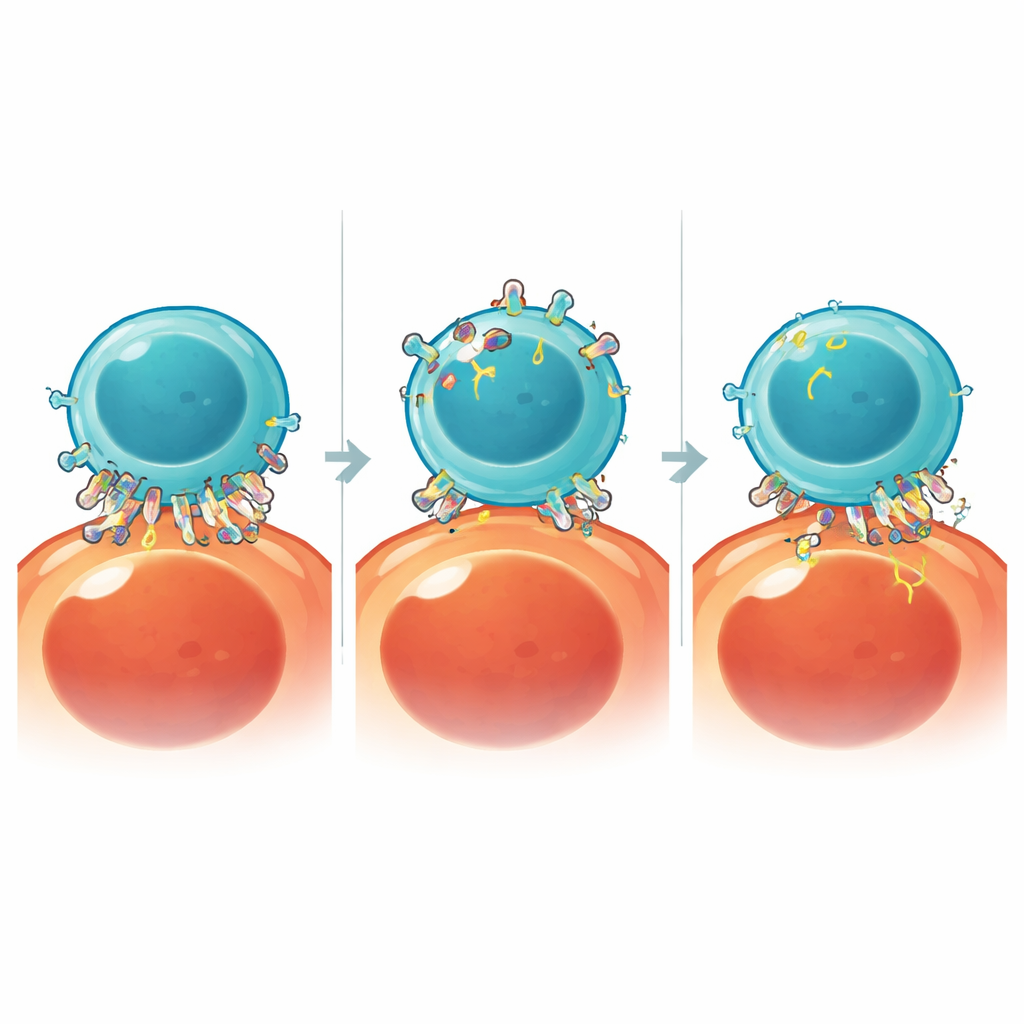
As células CAR T são projetadas para reconhecer o câncer ao se ligarem a marcadores específicos, ou antígenos, na superfície das células tumorais. Os autores mostram que, durante o contato íntimo, as células CAR T podem literalmente arrancar pedaços da membrana do tumor e incorporar esses antígenos à sua própria superfície — um processo chamado trogocitose. À medida que isso ocorre, as células tumorais perdem os próprios marcadores que as células CAR T precisam para detectá‑las, enquanto as CAR T ficam revestidas de antígenos tumorais. A equipe confirmou essa troca para vários alvos clinicamente importantes, incluindo CD19 e BCMA, tanto em cânceres sanguíneos quanto em modelos de tumores sólidos, e até a detectou no sangue de pacientes após o tratamento com CAR T.
Tiro amigo: como a trogocitose enfraquece as células CAR T
Uma vez que as células CAR T carregam antígenos tumorais em sua própria superfície, elas começam a se reconhecer umas às outras como alvos. Isso leva à “fratricida”, em que células CAR T matam outras células CAR T, e à autoestimulação crônica que as conduz a um estado exausto e menos funcional. Para provar que a trogocitose era a causa direta, os pesquisadores projetaram um sistema “degradador de antígeno trogocítico” que destrói seletivamente o antígeno transferido nas células CAR T sem afetar seus alvos normais. Remover esses antígenos adquiridos reduziu fortemente a fratricida e o acúmulo de marcadores de exaustão, e permitiu que as células CAR T controlassem células leucêmicas de forma mais eficaz em desafios repetidos no laboratório.
Rastreando e dissecando o processo de roubo de antígenos
Para estudar a trogocitose em tempo real, a equipe construiu um ensaio de luciferase dividida em que a luz é produzida apenas quando fragmentos de antígeno se movem das células tumorais para as células CAR T. Essa leitura sensível permitiu triagens rápidas dos processos celulares que poderiam impulsionar a transferência de antígeno. Usando inibidores de pequenas moléculas, descobriram que a enzima catepsina B, uma protease normalmente envolvida na degradação de proteínas, é um jogador-chave. A catepsina B movimenta-se rapidamente para a zona de contato onde as CAR T engajam as células tumorais, e sua atividade fora da célula é suficiente para promover o descolamento e a captação de fragmentos de membrana ricos em antígenos. Notavelmente, bloquear a catepsina B reduziu fortemente a trogocitose sem prejudicar significativamente a capacidade das CAR T de matar células tumorais.
Usando freios naturais para proteger as células CAR T
O organismo já contém inibidores naturais da catepsina B, conhecidos como cistatinas. Os pesquisadores aumentaram um desses inibidores, a cistatina A, dentro das células CAR T e mostraram que isso reduziu com segurança a atividade da catepsina B e diminuiu drasticamente a trogocitose em múltiplos modelos tumorais, incluindo células leucêmicas primárias de um paciente. Com menos roubo de antígenos, as células CAR T sobreviveram melhor, se acumularam em maior número e mantiveram um controle tumoral de longo prazo mais robusto tanto em pratos de laboratório quanto em modelos murinos. No entanto, a expressão crônica de cistatina A desencadeou inesperadamente um freio interno distinto — a regulação positiva da proteína reguladora CISH — que promoveu sinais de exaustão das células T. Ao eliminar CISH enquanto superexpressavam cistatina A, a equipe conseguiu reter os benefícios da redução da trogocitose e da fratricida, minimizando a exaustão e prolongando ainda mais a persistência das CAR T.
O que isso pode significar para pacientes
Este trabalho fornece evidência clara de que o roubo de antígenos pelas células CAR T não é apenas um efeito colateral curioso, mas um motor direto de falha do tratamento, causando tanto a fuga tumoral quanto a autodestruição das células terapêuticas. Mostra também que a trogocitose depende da catepsina B e pode ser separada seletivamente da atividade mata‑câncer usando tanto fármacos quanto artifícios genéticos, como a superexpressão de cistatina. No futuro, produtos CAR T pré‑engenheirados para limitar a trogocitose — ou combinados com inibidores inteligentes da catepsina B — poderiam permanecer ativos por mais tempo, manter maior pressão sobre as células tumorais e reduzir as chances de recaída.
Citação: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
Palavras-chave: Terapia com células CAR T, trogocitose, catepsina B, cistatina A, imunoterapia contra o câncer