Clear Sky Science · de
Verhinderung von Trogocytose durch Hemmung von Cathepsin B verbessert die Funktion von CAR-T-Zellen
Warum diese Forschung für künftige Krebstherapien wichtig ist
Die CAR-T-Zelltherapie hat die Behandlung bestimmter Blutkrebsarten revolutioniert und viele Patientinnen und Patienten in tiefe Remissionen gebracht. Dennoch erleidet ein großer Teil dieser Patienten später ein Rezidiv, oft weil Krebszellen Wege finden, sich vor diesen gentechnisch veränderten Immunzellen zu verbergen. Diese Studie beschreibt eine zuvor unklare Fluchtstrategie — die „Trogocytose“, ein Prozess, bei dem Krebszellen wichtige Oberflächenmarker an CAR-T-Zellen abgeben — und zeigt, wie die Blockade eines einzelnen Enzyms CAR-T-Zellen haltbarer und wirksamer machen kann.
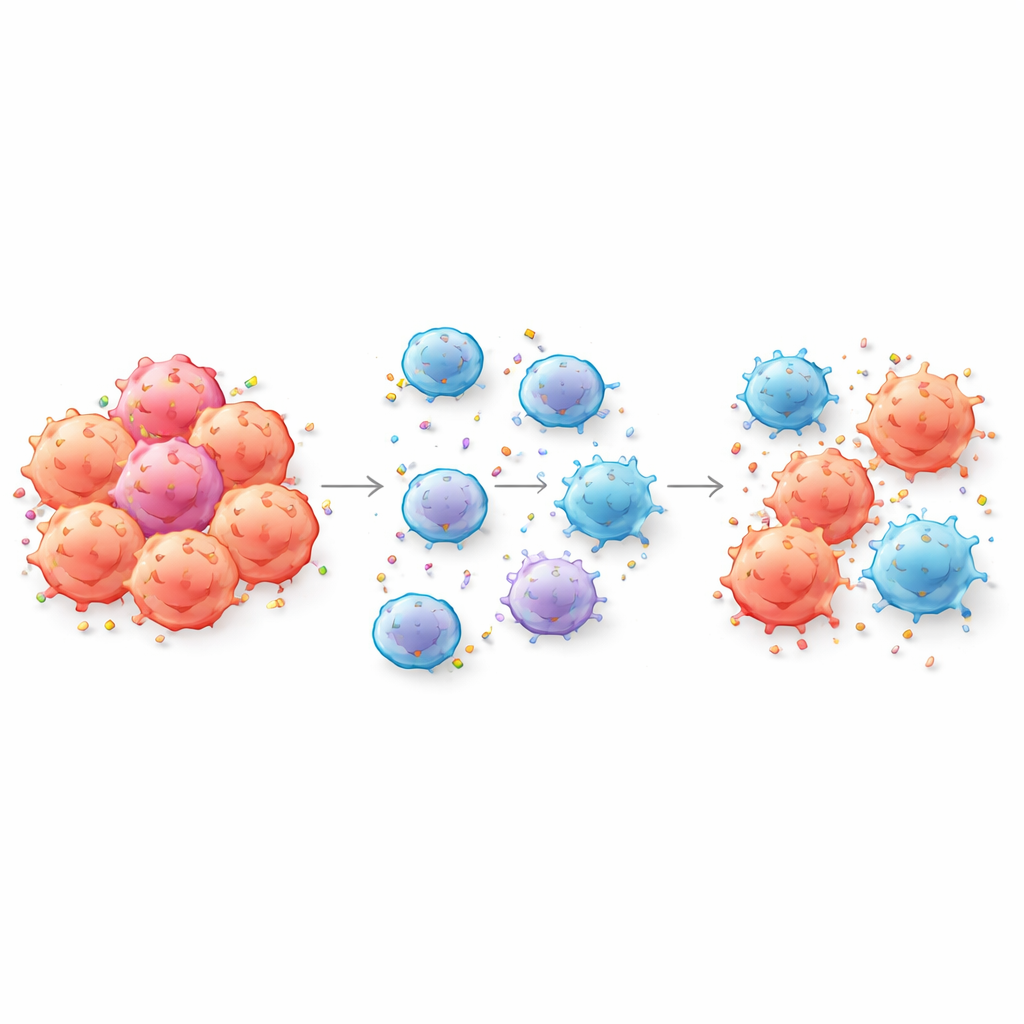
Wenn Krebszellen ihre Ausweise weitergeben
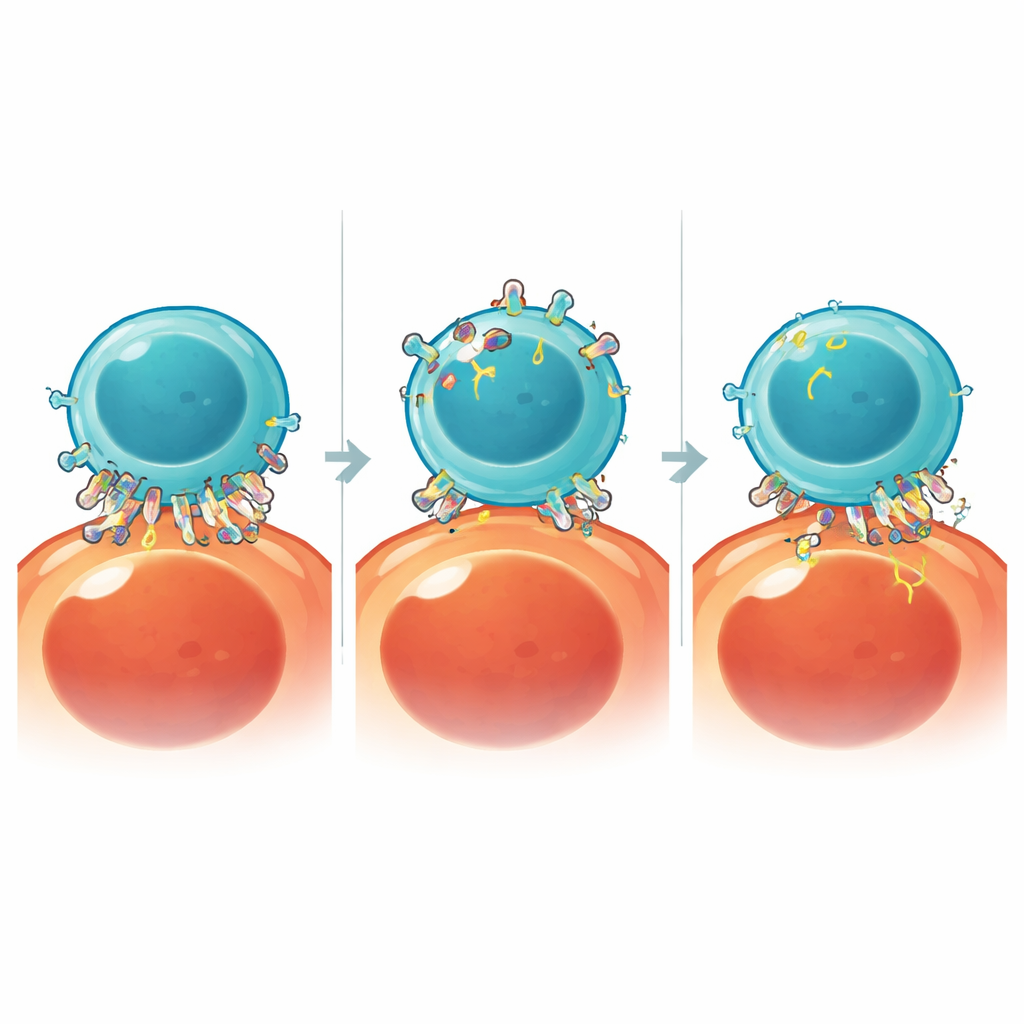
CAR-T-Zellen sind so konstruiert, dass sie Krebs erkennen, indem sie an spezifische Marker oder Antigene auf der Tumorzelloberfläche andocken. Die Autoren zeigen, dass CAR-T-Zellen bei engem Kontakt buchstäblich Stücke der Tumormembran abreißen und diese Antigene in ihre eigene Oberfläche integrieren können — ein Vorgang, der als Trogocytose bezeichnet wird. Dabei verlieren Tumorzellen genau die Marker, die CAR-T-Zellen zu ihrer Erkennung benötigen, während CAR-T-Zellen selbst mit Tumorantigenen bedeckt werden. Das Team bestätigte diesen Austausch für mehrere klinisch relevante Ziele, darunter CD19 und BCMA, sowohl in Blutkrebs- als auch in Modellen solider Tumoren und detektierte ihn sogar im Blut von Patientinnen und Patienten nach CAR-T-Behandlung.
Friendly fire: wie Trogocytose CAR-T-Zellen schwächt
Sobald CAR-T-Zellen Tumorantigene auf ihrer eigenen Oberfläche tragen, beginnen sie, einander als Ziele zu erkennen. Das führt zu „Brudermord“ (fratricide), bei dem CAR-T-Zellen andere CAR-T-Zellen töten, und zu chronischer Selbststimulation, die sie in einen erschöpften, weniger funktionalen Zustand treibt. Um zu beweisen, dass Trogocytose die direkte Ursache ist, entwickelten die Forscher ein System eines „trogocytischen Antigen-Degraders“, das selektiv das übertragene Antigen auf CAR-T-Zellen zerstört, ohne ihre normalen Ziele zu beeinträchtigen. Das Entfernen dieser erworbenen Antigene verringerte Brudermord und die Anhäufung von Erschöpfungsmarkern deutlich und erlaubte CAR-T-Zellen, Leukämiezellen bei wiederholten Herausforderungen im Labor effektiver zu kontrollieren.
Verfolgen und auseinandernehmen des Antigen-Diebstahls
Um Trogocytose in Echtzeit zu untersuchen, bauten die Wissenschaftler einen Split-Luciferase-Assay, bei dem Licht nur dann erzeugt wird, wenn Antigenfragmente von Tumorzellen in CAR-T-Zellen wandern. Dieser empfindliche Messwert ermöglichte ein schnelles Screening zellulärer Prozesse, die den Antigen-Transfer antreiben könnten. Mithilfe von kleinmolekularen Inhibitoren entdeckten sie, dass das Enzym Cathepsin B, eine Protease, die normalerweise am Proteinabbau beteiligt ist, eine Schlüsselrolle spielt. Cathepsin B bewegt sich schnell in die Kontaktzone, in der CAR-T-Zellen Tumorzellen begegnen, und seine Aktivität außerhalb der Zelle reicht aus, um das Ablösen und Aufnehmen von antigenreichen Membranstückchen zu fördern. Bemerkenswerterweise reduzierte die Blockade von Cathepsin B die Trogocytose stark, ohne die Fähigkeit der CAR-T-Zellen, Tumorzellen zu töten, wesentlich zu beeinträchtigen.
Natürliche Bremsen einsetzen, um CAR-T-Zellen zu schützen
Der Körper verfügt bereits über eingebaute Inhibitoren von Cathepsin B, sogenannte Cystatine. Die Forscher verstärkten eines davon, Cystatin A, in CAR-T-Zellen und zeigten, dass dies die Cathepsin-B-Aktivität sicher herunterregelt und die Trogocytose in mehreren Tumormodellen, einschließlich primärer Leukämiezellen eines Patienten, deutlich reduzierte. Mit weniger Antigendiebstahl überlebten CAR-T-Zellen besser, häuften sich in größerer Zahl an und hielten eine stärkere langfristige Tumorkontrolle sowohl in Zellkultur als auch in Mausmodellen aufrecht. Allerdings löste die chronische Cystatin-A-Expression unerwartet eine separate interne Bremse aus — die Hochregulierung des regulatorischen Proteins CISH —, die Anzeichen von T-Zell-Erschöpfung förderte. Durch das Entfernen von CISH bei gleichzeitiger Überexpression von Cystatin A konnten die Forschenden die Vorteile reduzierter Trogocytose und verringerten Brudermords beibehalten und gleichzeitig die Erschöpfung minimieren, was die Persistenz der CAR-T-Zellen weiter verlängerte.
Was das für Patientinnen und Patienten bedeuten könnte
Diese Arbeit liefert klare Belege, dass der Antigen-Diebstahl durch CAR-T-Zellen nicht nur ein kurioses Nebenphänomen ist, sondern ein direkter Treiber von Therapieversagen — sowohl durch Tumorflucht als auch durch Selbstzerstörung der therapeutischen Zellen. Sie zeigt außerdem, dass Trogocytose von Cathepsin B abhängt und selektiv vom Krebsabtötungsmechanismus entkoppelt werden kann, sei es durch Medikamente oder genetische Eingriffe wie Cystatin-Überexpression. Zukünftig könnten CAR-T-Produkte, die vorab so konstruiert sind, dass sie Trogocytose begrenzen — oder in Kombination mit gezielten Cathepsin-B-Inhibitoren — länger aktiv bleiben, den Druck auf Krebszellen aufrechterhalten und die Wahrscheinlichkeit eines Rezidivs verringern.
Zitation: Dietze, K.A., Nguyen, K., Pathni, A. et al. Preventing trogocytosis by cathepsin B inhibition augments CAR T-cell function. Sig Transduct Target Ther 11, 149 (2026). https://doi.org/10.1038/s41392-026-02654-z
Schlüsselwörter: CAR-T-Zelltherapie, Trogocytose, Cathepsin B, Cystatin A, Krebsimmuntherapie